
第一作者:Yijing Liu
通訊作者:戴志飛、陳小元
通訊單位:北京大學、美國國立衛生研究院
核心內容:
1. 總結了不同類型的PTAs材料和提高PTT效率的策略。
2. 結合其他療法,討論了聯合治療的實例,并介紹了PAI在癌癥相關研究中的應用。
3. 討論了PTT和PAI對抗癌癥的前景和挑戰。
癌癥仍然是目前人類健康所面臨的一個嚴峻問題。全球每年大約有1400萬新癌癥患者和800萬人死于癌癥相關疾病。因此世界各地的研究人員一直在努力開發更精確、更快速的診療方法來對抗癌癥。
在不同的治療方法中,光熱治療(PTT)具有一定的優勢:使用可調節劑量的外部激光照射可以精確定位腫瘤,從而使最小化對周圍健康組織的損傷。作為一種有效的非侵入性治療方法,PTT能夠治療多種類型的癌癥。理想的光熱治療試劑(PTA)應該有高的光熱轉換效率(PCE),并且在腫瘤中有良好的積累。其中納米PTAs可以通過EPR效應或者主動靶向在腫瘤中積累,并且可以將多種成像方式和治療功能整合到一個平臺上。
而PTT與其他療法的組合也顯示了更好的治療效果。聯合療法的治療結果并不是單純的相加,而是一種協同效應。PTT可以通過提高藥物傳遞效率、刺激藥物釋放、調節腫瘤微環境(TME)、激發腫瘤特異性抗原釋放等等。
PTT最大的問題是光的穿透深度有限,這導致在輻射范圍之外的腫瘤的不能完全治愈。除此之外,在腫瘤中PTAs的積累效率相對較低;過熱會對正常組織造成不必要的損害;由于某些癌癥中熱休克蛋白的過度表達而對PTT產生耐性都是PTT所面臨的挑戰。
除了殺死癌細胞外,光熱效應還能產生聲波,可以被探測并轉化為成像信號,這被稱為光聲成像(PAI)。這項技術不僅為人們提供了腫瘤診斷的另一種成像方式,而且還能在TME中檢測出與生物學相關的信號,比如酸性pH,酶和活性氧(ROS)。此外,PAI提供的即時診斷功能也可以幫助手術的操作。并且在大多數情況下,PTAs可以同時用于PTT和PAI。
有鑒于此,北京大學戴志飛教授課題組和美國國立衛生研究院(NIH)陳小元教授團隊對最新的光熱治療癌癥和PAI診斷的工作進行了綜述。
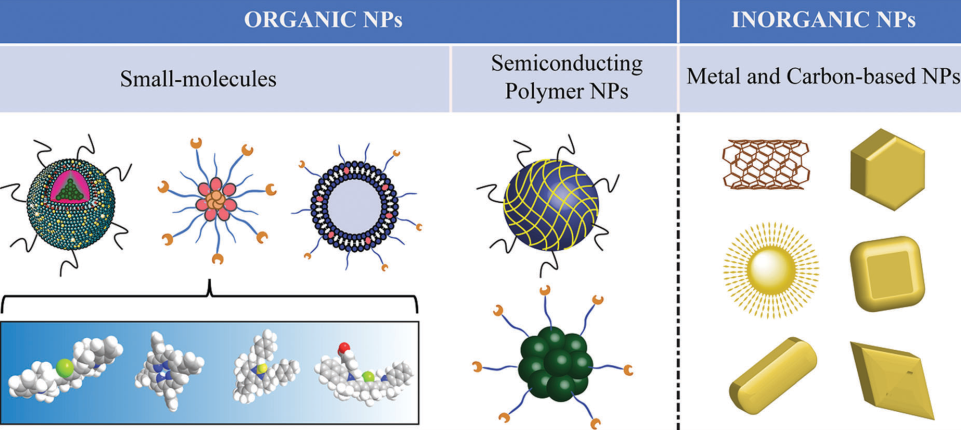
圖1 納米光熱轉化材料的分類
1. PTAs的分類和特征
PTAs可以將吸收的光的能量轉化為熱能,從而提高周圍環境的溫度。理想情況下,PTAs只會在局部增加溫度,以減少對健康組織的損害。為了實現這個目標,PTAs的吸收通常會被調整到波長在750到1350 nm之間的區域,包括NIR-I區和NIR-II區。
而PTAs一般可分為無機材料和有機材料(圖1)。無機材料包括貴金屬材料、金屬硫化物、碳納米材料(如石墨烯和碳納米管)和其他二維(2D)材料(如黑磷、納米片、氮化硼和石墨化碳氮化物)。有機PTAs包括小分子和半導體聚合物NPs(SPNPs)。
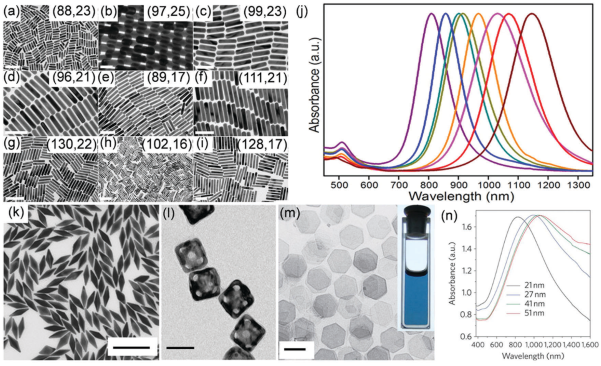
圖2 PTAs中的貴金屬材料
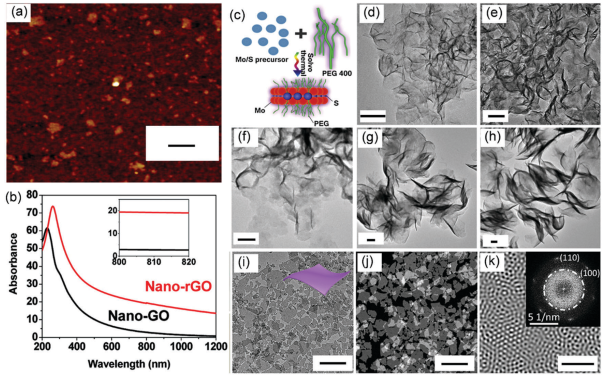
圖3 PTAs中非金屬材料的代表

圖4 基于小分子的PTAs
一般來說,無機PTAs擁有更高的PCE和更好的光熱穩定性。但是有機的PTAs可能會在生物降解性和生物相容性方面勝出。因此也沒有哪種類型的PTA是最好的這樣一種結論。而克服不同類型材料的缺點,也是科學家們一直以來努力研究的方向。
2. 提高光熱治療效果的方法
光熱治療的效果與許多問題有關,包括使用適當的輻射劑量;確定最佳治療時間;增強PTAs的PCE和腫瘤積累等。激光照射過量可能會對正常組織造成過熱和不必要的損害,而激光功率強度也會影響細胞死亡得機制。
根據PTAs結構和物理性質,它們在體內的行為和在腫瘤中的積累差異很大。因此,應該結合成像技術以確定最佳的治療時間點。而且,激光的強度隨著深度的加深會顯著減弱,導致更深層的腫瘤的溫度上升很慢。因此提高PTAs的PCE和開發NIR-II區 PTAs對改善治療腫瘤是很有益的。最后,了解PTAs在腫瘤中的濃度對于確定PTT結果至關重要,因為在腫瘤中增加PTAs的積累也會使得治療更加有效。
其中,確定合適的治療窗口非常重要。在許多臨床前研究中發現,PTAs通過血液循環系統時會利用 EPR效應在腫瘤中積累。但是由于其物理性質的不同,PTAs的藥物動力學行為各不相同。通常情況下,如果PTAs在腫瘤中達到最高的積累,那么治療效果會更好。
考慮到PTAs通常也具有成像功能,可以在實時監測腫瘤中NPs的積累來為PTT提供指導,這被稱為成像指導的治療。許多成像方式,如正電子發射斷層掃描(PET)、單光子發射計算機斷層掃描(SPECT)、MRI、熒光成像、余輝熒光成像、PAI,超聲成像、CT與PTAs相結合來協助治療。在某些情況下,還多種成像模式結合在一起,共同為腫瘤診斷和治療監測提供更多的幫助信息。
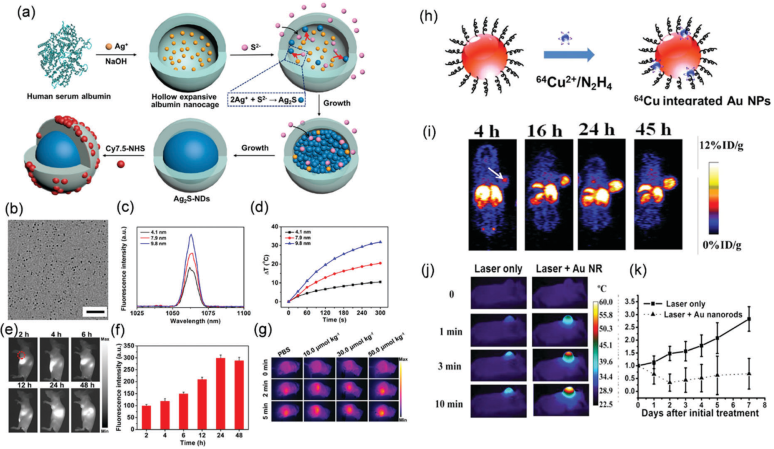
圖5 熒光、熱、PET成像指導的PTT
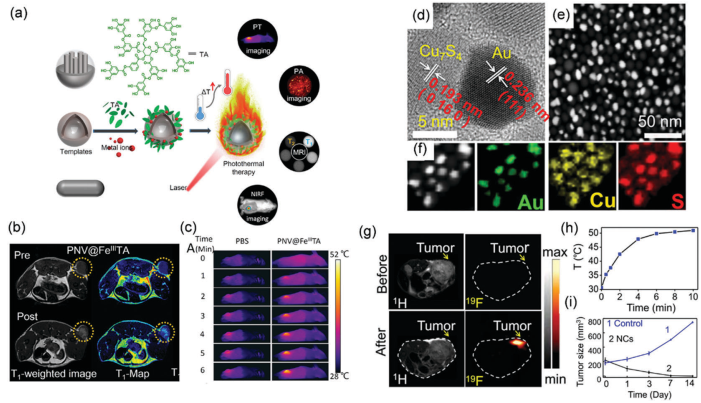
圖6 MRI、多模式成像結合指導的PTT
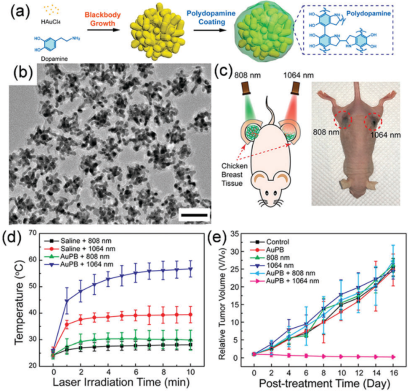
圖7 NIR-II區PTAs
另外,成功的PTT的關鍵是提高在腫瘤中PTAs的積累效率。一般來說,腫瘤中納米材料的積累是建立在EPR效應的基礎上的,即利用腫瘤的不正常的血管來增強NPs進入腫瘤和由于淋巴系統受損而延長NPs在腫瘤中的滯留。
然而,在到達腫瘤開始進行PTT之前,NPs還會遇到許多生物障礙。這些障礙包括單核吞噬細胞系統(MPS)的清除以及由于內部壓力升高而將NPs從腫瘤中驅逐出去等等。許多策略已被研究用于改善在腫瘤中PTAs的積累,其中包括改變NPs外的保護層、在NPs中引入靶向配體、優化NPs大小和形狀以及調節TME等。
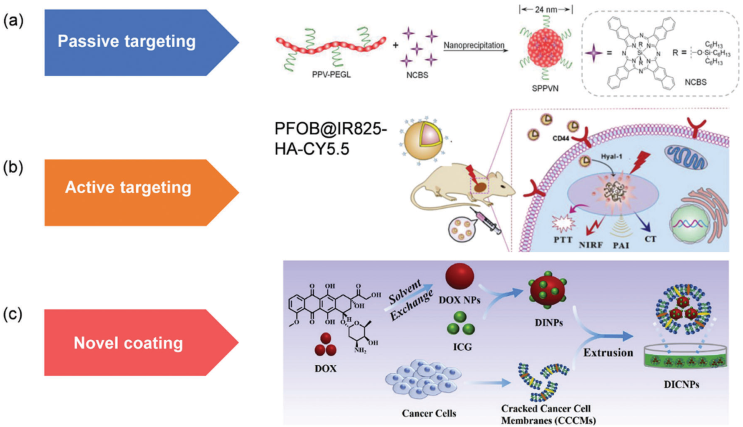
圖8 納米材料靶向腫瘤的不同策略
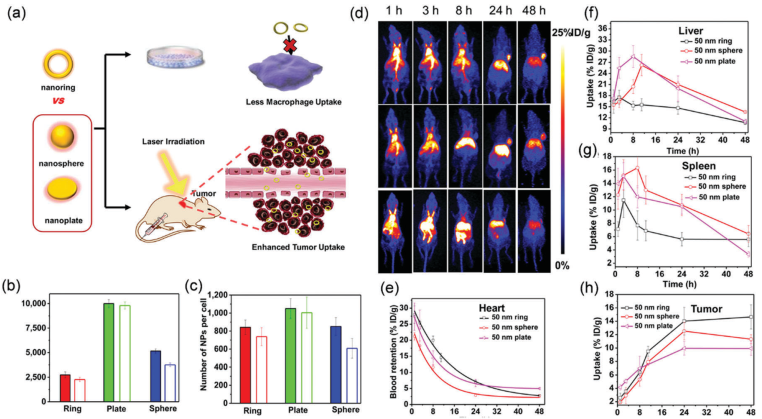
圖9 形貌對于PTAs的腫瘤積累效率的影響

圖10 利用TME增強PTAs靶向腫瘤
3. 以PTT為基礎的聯合治療
單一療法通常不足以完全治愈腫瘤,PTT也并不例外。即使有它很好的治療效果,但是其自身的局限性也會導致癌細胞的不能被完全消除,進而導致腫瘤復發和在遠處器官的轉移。而PTT和其他療法相結合則可以改善整體治療效果。在許多情況下,不同療法的結合不只是一個簡單的補充,而是會達到協同治療的效果。例如PTT可以用來增強腫瘤內NPs或藥物載體的積累和滲透。
此外,研究表明根據激光劑量的不同,PTT也可以促進藥物載體的細胞吸收,觸發輻射區域的載體去釋放藥物,來克服耐藥性并抑制DNA修復,這對藥物治療來說是很有利的。此外,PTT還可以增加氧氣灌注以改變腫瘤缺氧微環境,這就有利于改善依賴氧的治療方法,如PDT或放射治療。同時腫瘤細胞的熱凋亡也可以促進PTT與免疫療法的結合,因為這一過程十分有助于腫瘤特異性抗原的釋放。
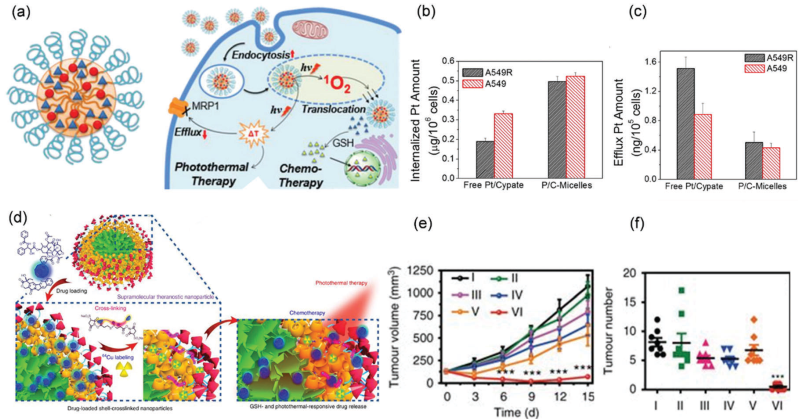
圖11 PTT與化學治療相結合
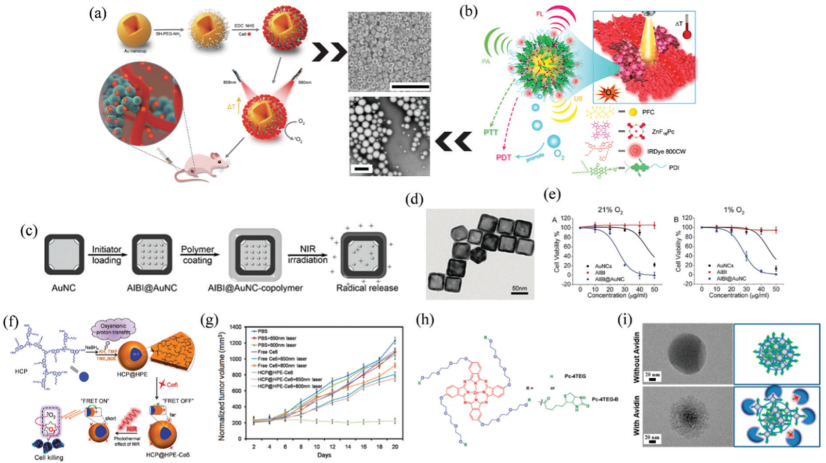
圖12 PTT與PDT相結合
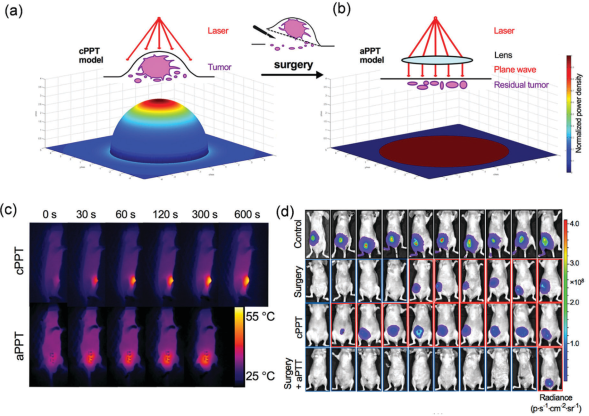
圖13 PTT與手術切除相結合
4. 利用PAI改善腫瘤診療
在活體生物系統中實現可視化解剖結構可以大大增強日常臨床實踐的治療效果。其中使用光源或熒光染料的成像方式很多是在細胞和分子水平上。然而,光學成像模式在很大程度上受到在生物介質中信號的丟失或散射的影響,導致圖像分辨率大大降低。
而PAI結合了光學和聲學特性,突破了光學檢測的極限。與光學成像不同的是,PAI主要依賴于生物分子的熱彈性膨脹來產生聲波,從而產生光子的入射波。這些聲波的散射最小,因此可以從深層組織中被感知到,信號強度也沒有任何損失,并且可以實時地轉換成圖像。
一般來說,PAI系統主要使用脈沖激光源來激發生物樣本和超聲波傳感器來感知生成的聲波。但是,根據功能的不同,PAI的設備可能會有所不同:光聲內窺鏡(PAE),聚焦掃描光聲學顯微鏡(PAM),以及光聲層析成像(PAT)/光電計算機斷層掃描(PACT)是目前的三種主要類型。其中,PAT/PACT對深層組織成像特別有用,更具有應用于臨床的機會。
同時,PAI技術可以從內在的生物吸收劑中獲取與生物功能、解剖、分子/基因過程和體內代謝相關的對比效果。這種內源性吸收劑存在于諸如血紅蛋白、DNA/RNA、水、黑色素和脂質中,并且可以被光子照亮來獲得PAI的對比效果,并且不會改變它們的生物特性。利用這些優勢,許多工作利用PAI進行了多種成像造影的嘗試,例如用于腫瘤診斷,TME內細胞變化的成像和淋巴節點成像等。
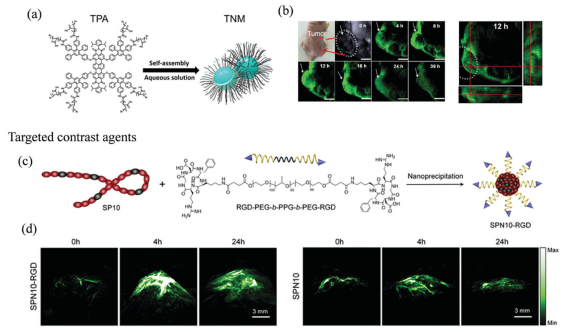
圖14 PAI用于腫瘤診斷

圖15 PAI用于淋巴結成像和細胞示蹤

圖16 PAI用于TME成像
綜上所述,納米技術的快速發展極大地促進了PTT和PAI在癌癥治療和診斷方面的進步,并且也成功發展了多模成像指導PTT和基于PTT的聯合治療。PAI在非侵入性監測疾病、腫瘤進展和治療效果方面也具有很高的臨床意義。
目前這一領域所面臨的挑戰在于如何大規模合成安全的PTAs以及推動它們的臨床轉化。這就需要開發更精確、更靈敏的實時溫度監測技術,并且需要對它們的長期細胞毒性和相關的免疫反應進行仔細評估。而在開發下一代PAI材料時應該從根本上解決成像的精確程度問題。這些嚴峻的挑戰就需要全球各領域科學家的共同努力和緊密合作才能解決。
參考文獻:
LiuY, Bhattarai P, et al. Photothermal therapy and photoacoustic imaging via nanotheranostics in fighting cancer[J]. Chemical Society Reviews, 2018.
DOI:10.1039/c8cs00618k
https://pubs.rsc.org/en/content/articlelanding/2018/cs/c8cs00618k#!divAbstract











