
特別說明:本文由米測技術中心原創撰寫,旨在分享相關科研知識。因學識有限,難免有所疏漏和錯誤,請讀者批判性閱讀,也懇請大方之家批評指正。
現存問題
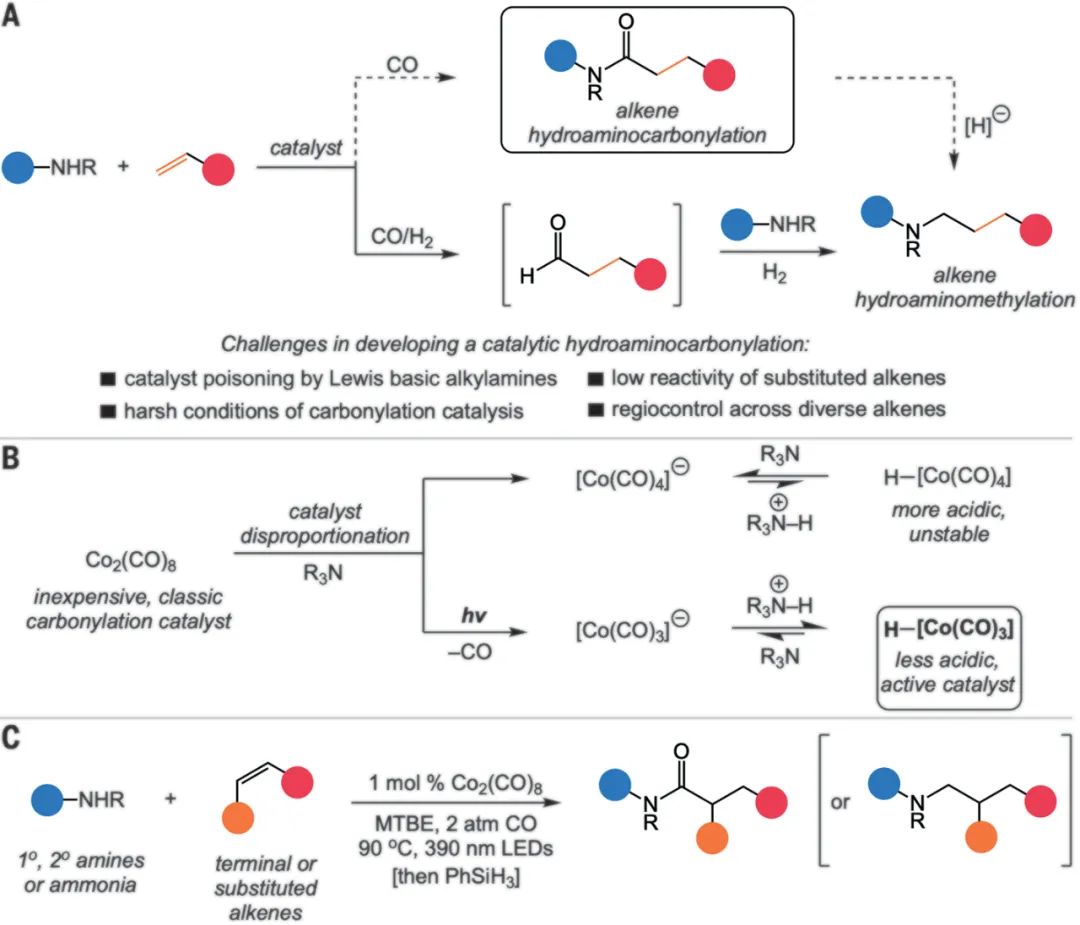
烯烴和胺的偶聯催化轉化具有廣泛的應用價值,目前常用的技術方案為過渡金屬和光氧化還原催化(圖1A),已取得了長足的進步,如:烯烴氫氨基羰基化(包括末端和多取代烯烴與胺原料的直接羰基化偶聯反應)方法是一種100%原子經濟的合成酰胺的方法,但氫氨基羰基化反應在烯烴和胺的范圍內都是有限的,且需要在高溫高壓下使用貴金屬催化劑進行。烷基胺的路易斯堿度在目前的方法中尤其成問題,因為金屬催化劑中毒和必要的催化中間體(金屬氫化物)的抑制。在溫和的條件下,利用地球上豐富的金屬將胺與各種烯烴有效偶聯,開發氫氨基羰基化反應仍然是催化領域的主要挑戰。
解決思路
20世紀30年代,Roelen發現了以Co2(CO)8為催化劑的氫甲酰化(氧)反應,在與H2反應后原位生成HCo(CO)4。而三羰基物質HCo(CO)3的生成對于烯烴配位十分重要,而紫外線光就可以促進配體解離生成HCo(CO)3。研究小組也使用未修飾的Co2(CO)8作為預催化劑也成功實現了光促進氨基羰基化。基于此,北卡羅來納大學教堂山分校Erik J. Alexanian團隊研究發現:當用390 nm紫色LED照射時,只需要1.0 mol %的未經修飾的Co2(CO)8催化劑和低CO壓力即可實現高效的氫氨基羰基化(圖1B),且反應僅使用當量的烯烴和烷基胺偶聯伙伴,不需要額外的試劑,選擇性和原子經濟性均達到100%。此外,該工藝還可以在添加有機硅烷還原劑的情況下實現烯烴氫胺甲基化(圖1C)。相關結果以《Cobalt-catalyzed synthesis of amides from alkenes and amines promoted by light》為題發表在Science上。 研究首先對反應底物的適用范圍進行了探索(圖2)。結果發現末端烯烴(如丙烯(1-8)、環和非環1,1-和1,2-二取代烯烴(9-13)、三取代烯烴和四取代烯烴(如β-香樟醇、1-甲基環己烯和四甲基乙烯,14-16)等均是良好的偶聯配體,得到良好到優異的酰胺收率。在多種不飽和天然反應物中(如1,1-二取代烯烴、膽固醇和奎寧,17-23)也展現出優異的反應性和選擇性,此外,各種伯、仲、無環胺都能與乙烯基環己烷高效反應,具有很高的區域選擇性(24-34)。因此Co2(CO)8催化的氫氨基羰基化反應與復雜烯烴(含有未保護極性官能團的分子)的相容性較高,且該催化體系具有通過功能化甚至是最具挑戰性的烯烴來提供酰胺的特殊能力。
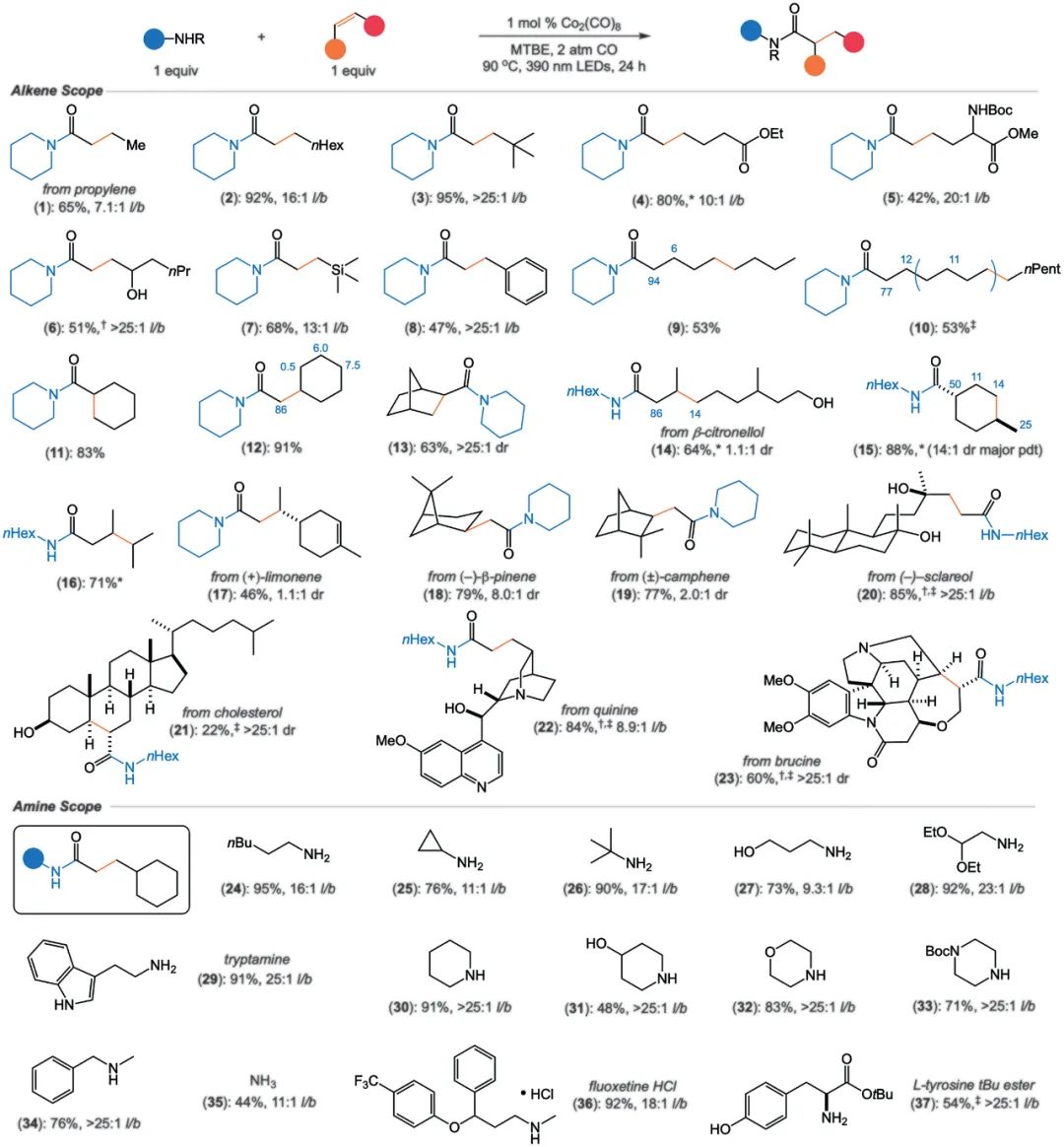
合成烷基胺是氫氨基羰基化反應后續有意義的反應,但通常也依賴于貴金屬催化劑和在高壓合成氣。標準的催化氫胺甲基化反應由于烯烴或必要的醛中間體可能發生氫化反應,存在化學選擇性問題,以及醛縮副產物的形成。而我們研究發現,在氫氨基羰基化完成后,簡單地將PhSiH3添加到反應混合物中,就能得到所需的烷基胺,總體收率很高(圖3)。該方法用Co作為催化劑可以很容易地獲得仲胺和叔胺,避免了化學選擇性問題。使用分離的酰胺進行的對照實驗表明,CO氣氛和390 nm LDE都提高了酰胺還原的效率。此外,以工業辛烯的生產的底物(四種辛烯同分異構體組成的等量反應混合物)探索該方法的實用性。以與1-辛烯反應相似的產率和選擇性產生酰胺2,證明了氫氨基羰基化的高度區域收斂性質(圖4A),支持了氫氨基羰基化的可擴展性(圖4B)。
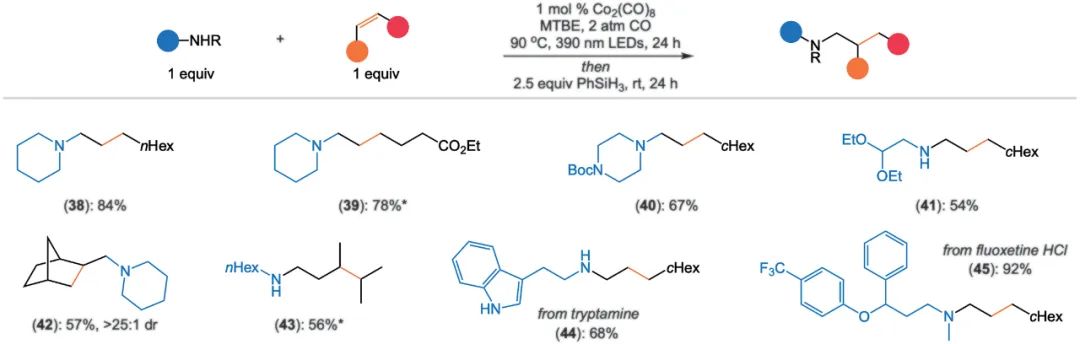
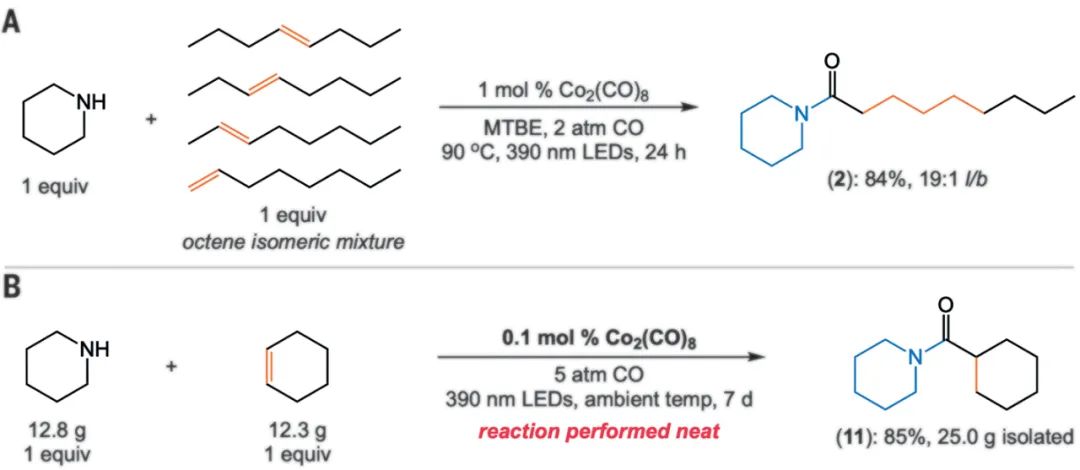
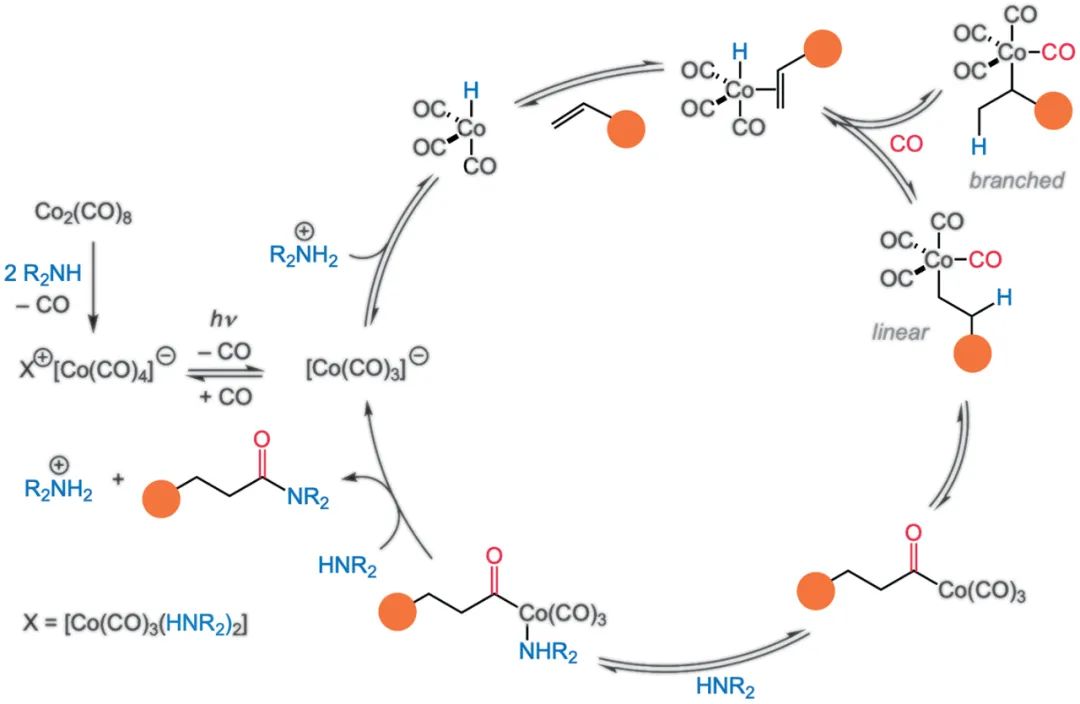
[CO(CO)3]的質子化在低反應壓力下優于CO配位,有利于形成對路易斯堿胺穩定的氫化鈷,并有利于烯烴配位。這種配位隨后是氫鈷化,導致區域異構的烷基鈷中間體能夠通過順序的β-氫化物消除和重新插入過程異構化,有利于具有無環底物的末端烷基鈷。隨后發生CO配體的遷移插入,形成酰基鈷三羰基。然后,胺親核試劑配位到金屬中心,隨后協同加成和/或還原消除生成酰胺產物[Co(Co)3]-,最后該產物經過質子交換再生HCo(Co)3。
總結
研究提出的未經修飾的Co2(CO)8的光溫和催化模式使烯烴的一般氫氨基羰基化成為可能,具有100%原子經濟的優勢。且適用于從丙烯到復雜生物堿天然產物的烯烴的轉化,以及從氨到藥物化合物的胺的轉化,具有多功能性,預計這種方法將在制備與醫學相關的、功能化的小分子到工業規模的化學生產等背景下具有廣泛應用前景。https://www.science.org/doi/10.1126/science.adk2312Mason S. Faculak et al. Cobalt-catalyzed synthesis of amides from alkenes and amines promoted by light. Science (2023). DOI:10.1126/science.adk2312












