ctDNA全稱為circulating-tumor DNA,是指人血液中腫瘤細(xì)胞體細(xì)胞DNA經(jīng)脫落或者當(dāng)細(xì)胞凋亡后釋放進(jìn)入循環(huán)系統(tǒng),故被稱為循環(huán)腫瘤DNA,包含著癌癥早期診斷和預(yù)后監(jiān)測等重要信息。然而,ctDNA的精準(zhǔn)檢測面臨著三大問題:① 臨床樣本(如血液、尿液、糞便)等成分復(fù)雜;② ctDNA的半衰期較短(<2小時(shí));③ ctDNA豐度極低,僅占循環(huán)游離DNA (cfDNA)總量的0.5~ 10%。傳統(tǒng)ctDNA富集和純化通常是基于磁珠和二氧化硅膜,然而,當(dāng)處理大量樣品時(shí),這些技術(shù)難以實(shí)現(xiàn)快速、高效的富集,并且操作復(fù)雜,檢測靈敏度有限。因此,迫切需要一種創(chuàng)新的ctDNA富集與分析技術(shù),以提高臨床診斷的靈敏度。
針對這一需求,北京航空航天大學(xué)樊瑜波、常凌乾、王楊等人在《ACS NANO》(IF: 17.1)期刊上發(fā)表了 “An ion concentration polarization micro-platform for efficient enrichment and analysis of ctDNA” 的研究文章。開發(fā)了一種基于離子濃度極化的微平臺(tái),能夠在30秒內(nèi)從血清、尿液和糞便等各種臨床樣品中,快速、高效地富集和純化ctDNA。并集成等溫?cái)U(kuò)增模塊,將ctDNA的檢測靈敏度提高了100倍,顯著消除了因ctDNA豐度低而導(dǎo)致的樣本假陰性結(jié)果。
離子濃度極化(ICP)是一種新興的原位分子富集和純化方法,在陽離子選擇性的Nafion膜上施加垂直電場,根據(jù)帶電分子的電滲透力和電泳力進(jìn)行分離和純化。同時(shí)結(jié)合“自由流動(dòng)”的概念,形成基于“自由流動(dòng)ICP(FF-ICP)”的連續(xù)分離方法。對于帶有負(fù)電荷的核酸分子,受到向下的電滲透力(EO)和不斷增加的向上的電泳力(EP)的共同作用,被電動(dòng)力學(xué)捕獲,形成離子富集區(qū)。同時(shí),施加連續(xù)的水平驅(qū)動(dòng)力,使被富集到的核酸或蛋白分子水平推進(jìn)并收集,從而進(jìn)行后續(xù)的擴(kuò)增分析(圖1)。
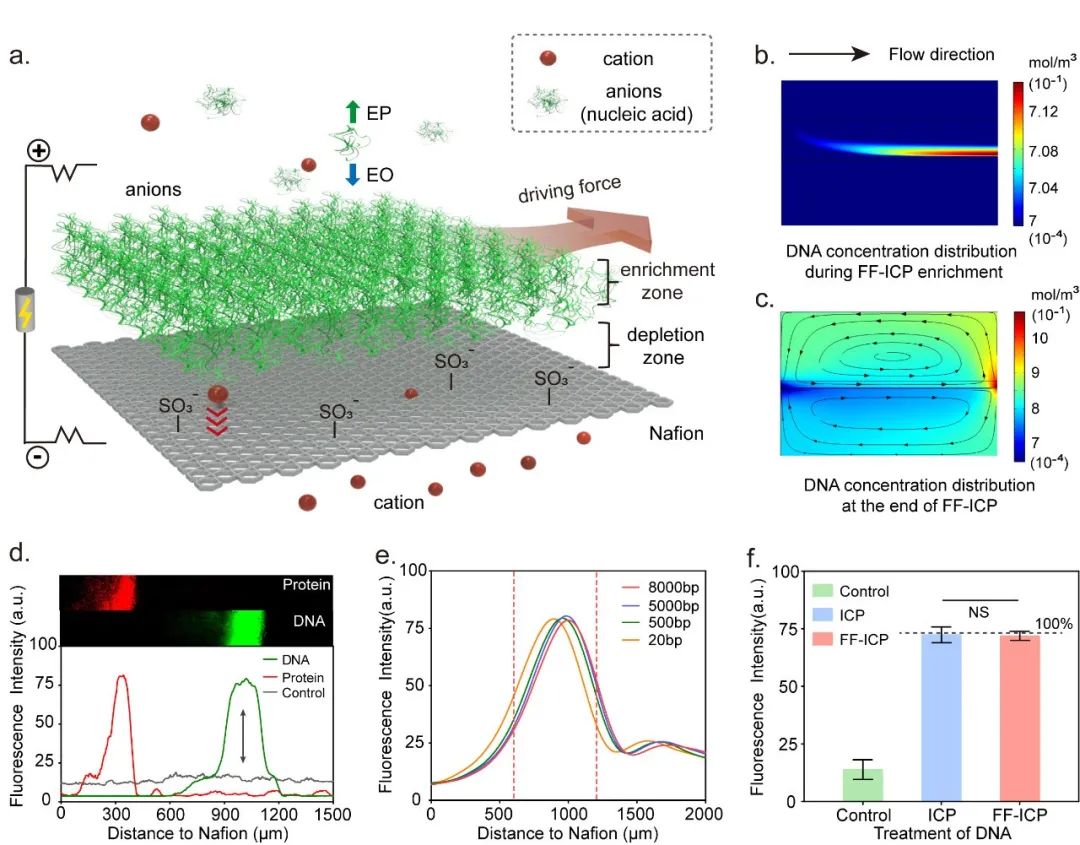
圖 1. “自由流動(dòng)ICP”的原理圖。
基于FF-ICP的DNA富集策略,研究團(tuán)隊(duì)設(shè)計(jì)了一種自供電、集成的微流控芯片,用于高靈敏度的核酸檢測。微平臺(tái)有兩個(gè)功能區(qū):核酸富集區(qū)、核酸等溫?cái)U(kuò)增檢測區(qū)(圖2a)。兩個(gè)區(qū)域由一個(gè)“y形”提取通道連接。富集區(qū)內(nèi)固定了陽離子選擇性的Nafion膜。在垂直電場和水平驅(qū)動(dòng)力作用下,液體樣品中的核酸被富集,形成“陰離子流”,然后在“y”形提取通道處收集(圖2b)。隨后,“陰離子流”進(jìn)入檢測區(qū),經(jīng)等溫?cái)U(kuò)增后進(jìn)行定量分析(圖2c)。剩余的溶液收集在廢液池中(圖2d)。
富集后的核酸進(jìn)入到核酸擴(kuò)增區(qū)之后,在含有100個(gè)微孔的檢測區(qū),用LAMP法進(jìn)行等溫?cái)U(kuò)增(65℃)。采用陽性微孔總數(shù)和每個(gè)微孔的熒光強(qiáng)度作為雙參數(shù)指示,使分析更加準(zhǔn)確和穩(wěn)定。
為了給FF-ICP提供穩(wěn)定的水平驅(qū)動(dòng)力,團(tuán)隊(duì)在生物芯片中集成了一個(gè)自供電真空電池系統(tǒng),電池使用預(yù)脫氣的PDMS,通過液體通道和真空通道之間的氣體交換提供“電力”,從而推動(dòng)液體樣品流動(dòng)(圖2e)。使得整個(gè)平臺(tái)能夠在不需要外部泵的情況下,連續(xù)地向下游輸送和富集核酸分子,并進(jìn)行核酸擴(kuò)增,具有用戶友好的性能。

圖2. 基于FF-ICP的集成微平臺(tái)用于連續(xù)的核酸富集和擴(kuò)增。
利用微平臺(tái)檢測臨床患者血清中的ctDNA。與未處理樣品相比,該裝置的富集效果和純化能力明顯高于試劑盒(圖3a-3c)。同時(shí),最終的擴(kuò)增結(jié)果也顯示,該微平臺(tái)能夠達(dá)到100拷貝/mL的靈敏度,比傳統(tǒng)方法(基于二氧化硅/磁珠的DNA提取與PCR擴(kuò)增)提高了100倍(圖3d)。
在臨床應(yīng)用中,對北京大學(xué)腫瘤醫(yī)院提供的38例非小細(xì)胞肺癌患者的血清樣本進(jìn)行EGFR外顯子19缺失突變的檢測。結(jié)果表明,微平臺(tái)的靈敏度顯著高于傳統(tǒng)PCR技術(shù),達(dá)到了100%,能夠大大避免了因ctDNA濃度不足而造成誤診的風(fēng)險(xiǎn)(圖3e和3f)。此外,該裝置檢測到的早期患者血清中ctDNA的含量明顯低于中晚期患者,證明該平臺(tái)的定量判斷能力可以預(yù)測患者的腫瘤發(fā)展(圖3g和3h)。通過將分析物的提取和富集(FF-ICP)與進(jìn)一步的生物分析技術(shù)進(jìn)行無縫集成,為超低豐度生物標(biāo)志物的檢測帶來巨大的好處。與傳統(tǒng)檢測技術(shù)相比,該平臺(tái)的靈敏度顯著提高了兩個(gè)數(shù)量級,能夠避免因濃度不足導(dǎo)致的誤診風(fēng)險(xiǎn),尤其有利于臨床感染篩查或者早期腫瘤診斷。

圖3. 用FF-ICP裝置檢測血清中ctDNA。
該研究第一單位為北航生物與醫(yī)學(xué)工程學(xué)院和生物醫(yī)學(xué)工程高精尖創(chuàng)新中心。通訊作者包括北航生物與醫(yī)學(xué)工程學(xué)院常凌乾教授,樊瑜波教授,王楊副教授,上海感染與免疫科技創(chuàng)新中心徐高連研究員。核心作者包括北航博士生王之瑩(第一作者)、碩士生劉明(共一)、北京大學(xué)腫瘤醫(yī)院吳楠教授、北京大學(xué)第三醫(yī)院林成浩主任(共一)等。
文章鏈接:https://pubs.acs.org/doi/full/10.1021/acsnano.3c07137











