鈀納米材料是目前被研究的最多的貴金屬納米材料之一,尤其是在催化領域。而今天,我們要介紹則是鈀納米材料不為人知的另一面:腫瘤光熱療。
光熱治療(Photothermal therapy, PTT)是近年來用于治療包括腫瘤在內的一些疾病的新型治療方法。以癌癥治療為例,光熱治療是指將具有較高光熱轉換效率的材料注射入體內,利用靶向技術使得材料聚集在腫瘤組織附近,從而在外部光源(一般是近紅外光)的照射下將光能轉化為熱能,來殺死癌細胞和抑制腫瘤生長。
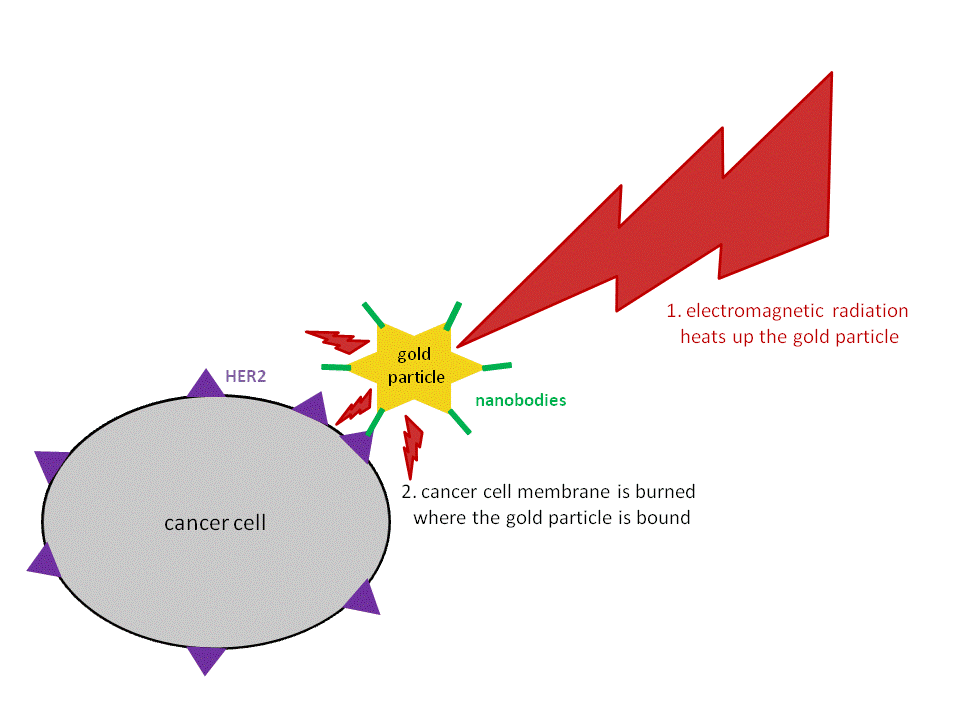
圖1. 腫瘤光熱療示意圖
光熱療材料可以分為有機和無機材料兩大類。其中,無機貴金屬納米材料由于具有以下兩大優勢,而被廣泛應用。
優勢1):表面等離子共振效應賦予其良好的近紅外吸收和光熱轉化效率;
優勢2):尺寸精確可控,合適尺寸的材料可以利用腫瘤內部血管結構的特殊性造成的EPR效應被動靶向富集在腫瘤中。
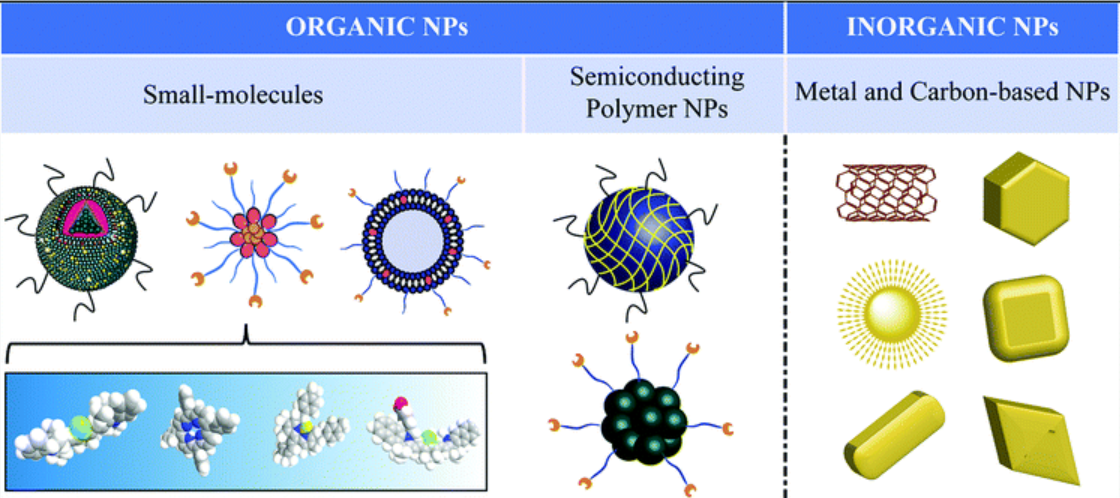
圖2. 光熱療材料分類匯總
Photothermal therapy and photoacousticimaging via nanotheranostics in fighting cancer(Chem. Soc. Rev, DOI: 10.1039/c8cs00618k )
https://pubs.rsc.org/en/content/articlehtml/2018/cs/c8cs00618k
在所有光熱療貴金屬納米材料中,金納米材料無疑是最成熟和最為人所知的,而新興的鈀納米材料則正在生物醫藥領域異軍突出。

2011年,廈門大學鄭南峰教授課題組成功制備了一種超薄(1.8nm)的藍色二維鈀納米片。均一的尺寸和良好的近紅外吸收性能使得“鈀藍”很快成為光熱治療試劑中的杰出代表。

圖3. 藍色鈀納米片:尺寸在5-200 nm均勻可控,厚度始終保持1.8 nm不變
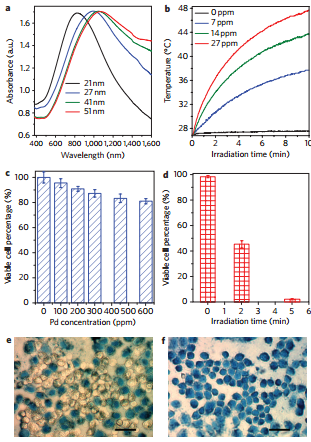
圖4. 鈀納米片優異的光熱治療效果
2014年,鄭南峰課題組通過改變溶劑和調控溫度等策略,進一步實現了對二維鈀納米片尺寸的更精確控制。其中,超小的(4.4nm)鈀納米片SPNS由于其可由尿液從體內代謝清除的特點,具備重大的臨床轉化應用價值。

Tang等人根據體內外系列實驗結果證明,利用SPNS良好的腫瘤積累和光熱效果,可以實現對小鼠皮下腫瘤的有效治療;更重要的是,SPNS的尺寸小于腎臟尿液代謝的閾值,使得其可以在完成治療任務后從體內被清除,大大降低了一直以來困擾人們的光熱試劑長期滯留體內帶來的毒性風險問題。
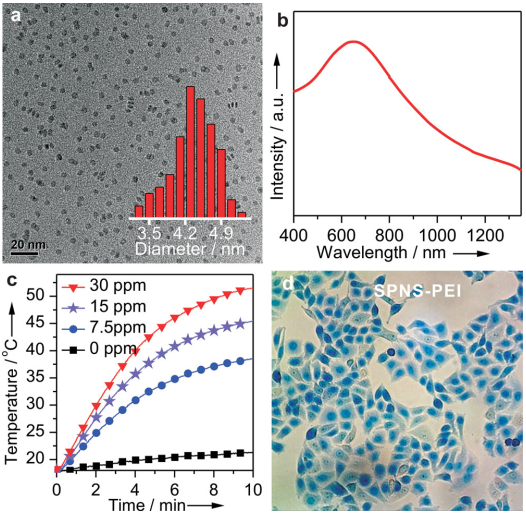
圖5. SPNS的表征和光熱效果
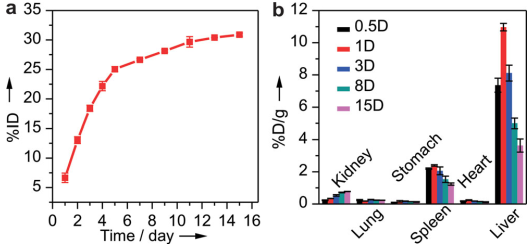
圖6. SPNS的體內清除(尿液)和15天生物分布
除了實現對二維鈀納米片的尺寸的精確控制,鄭南峰課題組及其合作者還利用其作為“種子”,通過加入不同金屬前驅體來制備不同組成的二維鈀基納米材料。譬如Chen等人在2014年報道的核殼結構Pd@Au納米材料。

Pd@Au不僅保留了作為“晶種”的鈀片的良好近紅外吸收,同時其在腫瘤部位的積累也更高,靜脈注射24小時后可到79 %ID/g。利用Pd@Au高效地被動靶向富集腫瘤的特點,研究人員通過光聲成像指導的體內光熱治療實現了在低功率密度條件下完全治愈小鼠皮下腫瘤。
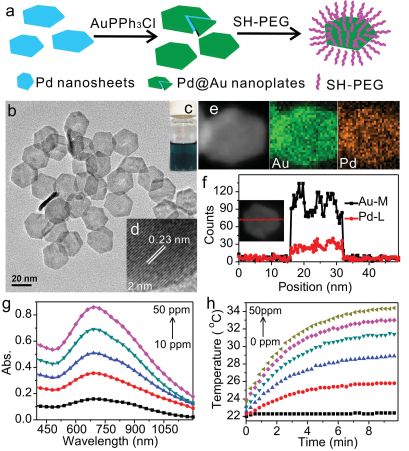
圖7. Pd@Au納米材料的表征和光熱性能
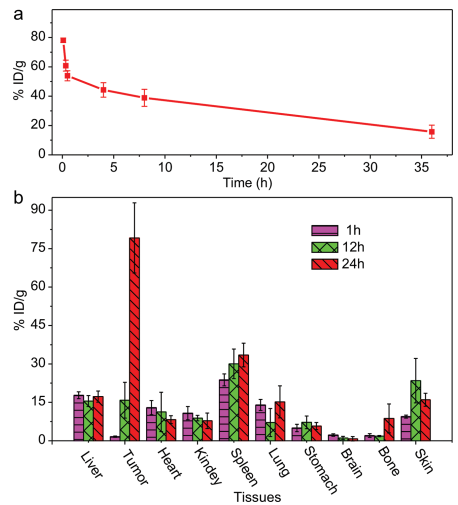
圖8. Pd@Au出色的被動靶向腫瘤能力
將光熱治療和其他療法相結合的協同治療是目前研究的重要方向之一,例如將同樣是光學治療的光動力治療(PDT)常常和PTT聯合用于對抗腫瘤。由于表面易被功能化和修飾,二維鈀基納米材料在協同治療領域同樣大放異彩。

2018年,鄭南峰課題組報道了將Pd@Pt-PEG-Ce6納米復合物用于改善實體瘤內部乏氧微環境的PTT+PDT聯合治療。研究人員利用Pd@Pt的光熱性能、過氧化氫酶活性及靶向腫瘤的能力,通過表面聚乙二醇化和負載光敏劑成功實現了對腫瘤內部對抗治療的不利因素的克服,發揮了PTT和PDT的協同促進效應,取得了非常好的治療效果。

圖9. Pd@Pt-PEG-Ce6納米復合物用于PTT+PDT聯合治療
2018年,東北師范大學Zhang等人制備了具有 Janus結構的CD-Pd 納米片/ ZIF-8納米顆粒。其中,CD-Pd納米片和PAA-ZIF-8分別用于裝載疏水性的10-羥基喜樹堿(HCPT)和親水性阿霉素(Dox)進行協同化療,而Pd納米片具有的較寬的近紅外(NIR)吸收帶,光熱轉化性能突出。體外和體內實驗結果表明,激光輻照組的雙藥治療腫瘤的效率最高。

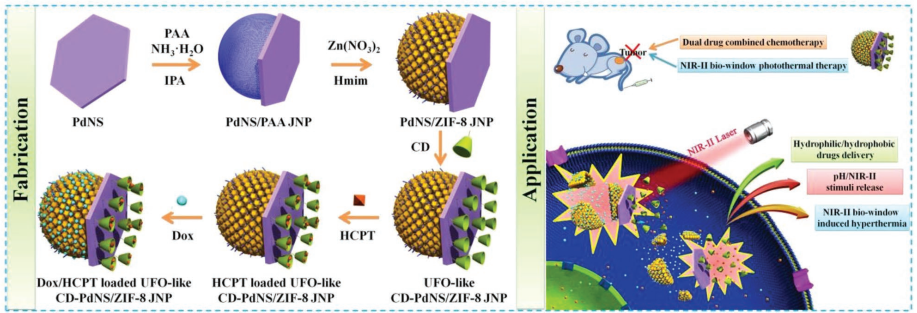
圖10. CD-Pd 納米片/ ZIF-8納米顆粒腫瘤治療示意圖
PS:鄭南峰教授課題組在Pd基納米材料光熱療領域進行了系統深入的研究,更多內容請查看鄭南峰課題組網站:http://nfzheng.xmu.edu.cn/
新發現
在光熱治療中,開發新材料固然重要,而如何將其他領域的知識融入其中以獲得好的效果也同樣具有重要的意義。隨著研究的不斷深入,對光熱治療的研究也越來越趨向于如何實現其臨床應用和拓展與其他治療方法結合的協同性治療。最近的兩篇Nature Communications報道的工作就把鈀納米材料的PTT“玩”出了新花樣。

2018年,深圳大學何前軍團隊和UCLA顧臻團隊聯合開發了一種將納米產氫材料用于PTT的新策略。傳統的氫化鈀納米材料具備很好的儲氫,自催化產氫和近紅外吸收性能。除了最后一點,其他的貌似都和PTT靠不上邊。正是這種看似沒有用的性能,被研究人員創新地利用于進行協同PTT的所謂“氫熱治療”。實驗通過制備PdH0.2納米材料并利用其具備的靶向腫瘤、近紅外光控制的釋放生物還原性氫及光熱轉化能力實現了低毒性的光聲成像指導的協同光熱治療,同時這一研究也為提高光熱治療試劑的多功能性用以增強抗腫瘤提供了全新的思路。(Nature. Commun, DOI: 10.1038/s41467-018-06630-2 )
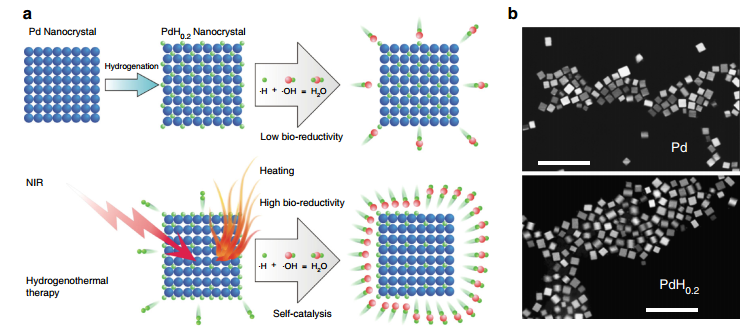
圖11. PdH0.2納米材料用于氫熱協同治療的模式示意圖
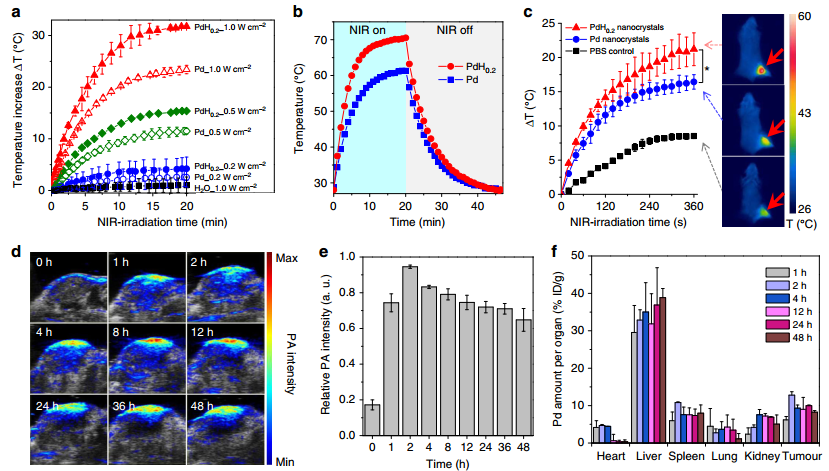
圖12. PdH0.2納米材料用于體內光聲成像診斷
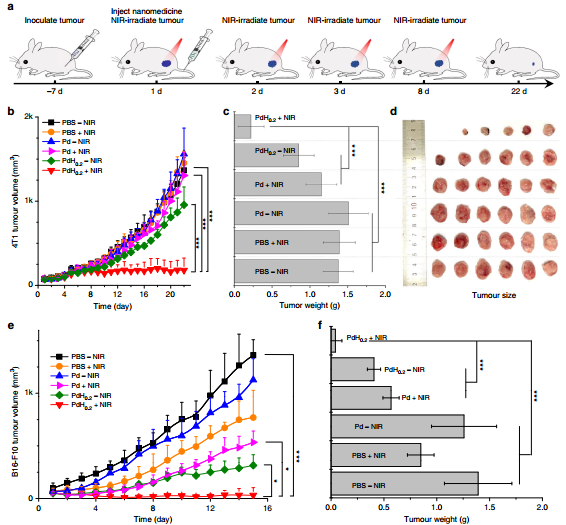
圖13. PdH0.2用于氫熱協同治療的優異效果

同樣是將光熱治療和其他療法相結合,南方科大Zhang等人最近也在對傳統的化學治療聯合PTT這種新老搭配的方法的研究上有了新的突破和進展。化療是目前臨床應用較為廣泛的一種療法,但是其療效常常不令人滿意的原因就在于有些腫瘤的耐藥性很強,對化療很不“感冒”。
研究人員發現,合金Pd-Cu四交叉納米材料特有的尖端位點結構可以大幅增強其光熱轉換效率,同時也會引發對腫瘤細胞存活有利的細胞自噬效應,并且這種效應的激發與材料的組成和形貌有關。例如,同樣組分的球形納米顆粒,或者同樣形貌的非合金四交叉則不具有類似效果。在進一步引入具有協同效應的自噬抑制劑例如3-甲基腺嘌呤或者氯喹作為化學治療藥物,實驗證明了通過化學-光熱聯合治療可以有效地治愈4T1及耐藥性的MCF7/MDR腫瘤,也揭示了光熱試劑材料自身的形貌和組成對于治療效果的重大影響。(Nature. Commun, DOI: 10.1038/s41467-018-06529-y)

圖14. 不同形貌的Pd-Cu合金納米材料
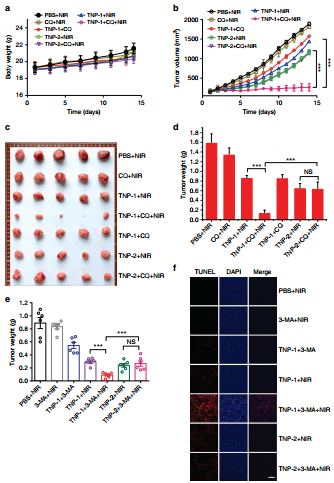
圖15. 合金Pd-Cu四交叉納米材料用于光熱-化學聯合治療4T1腫瘤的效果
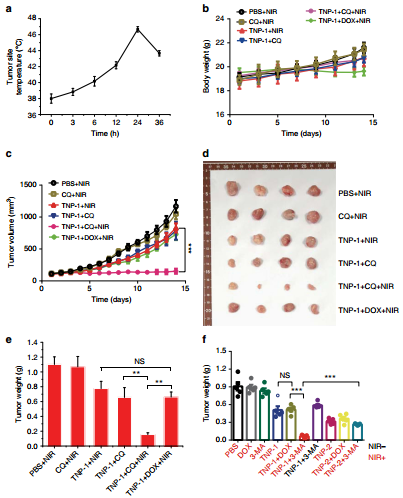
圖16. 合金Pd-Cu四交叉納米材料用于光熱-化學聯合治療耐藥腫瘤的效果
行文至此,小編想說:回顧傳統,更加有利于我們拓寬研究的思維,找到創新的法門;堅持創新,才能讓我們勤學多思,真正地把傳統發揚光大。不僅對PTT的研究是這樣,每一個研究課題其實都是有如此規律的存在。其實不管傳統也好,創新也罷;每一位從事光熱治療研究的人員的最終心愿都是希望早日克服腫瘤癌癥帶來的健康威脅;而每一位從事其他研究的人員的目標也都是能為這個領域做出自己的貢獻。我們相信,堅持傳統與創新齊頭并進,才能百花齊放,百家爭鳴!











