
第一作者:Daniel M Chevrier、Lluis Raich
通訊作者:張鵬
第一單位:加拿大達爾豪斯大學
研究亮點:
1. 發現在分子尺度上配體效應如何顯著影響巰基-金納米團簇的結構和性質;該發現可能將直接影響金納米團簇在催化和生物檢測方面的應用。
2. 用同步輻射X射線吸收譜和理論計算系統研究了不同巰基配體對金納米團簇在固相與溶液中原子/分子結構、配體溶劑化及團簇電子性質的變化。
研究背景
巰基保護的Au納米團簇由于具有優異的穩定性,獨特的核殼結構,小尺寸與大表面積等特性,在生物醫藥與催化領域表現出了重要的應用前景。其中,巰基配體對于Au納米團簇結構和性質的調節,發揮了關鍵的作用。然而,至今為止,巰基配體是如何在原子/分子尺度調節Au納米團簇的結構性質仍是未解之謎。
成果簡介
有鑒于此,加拿大達爾豪斯大學張鵬課題組實現了從分子尺度對小型巰基-金納米團簇中配體效應的分析與解釋。
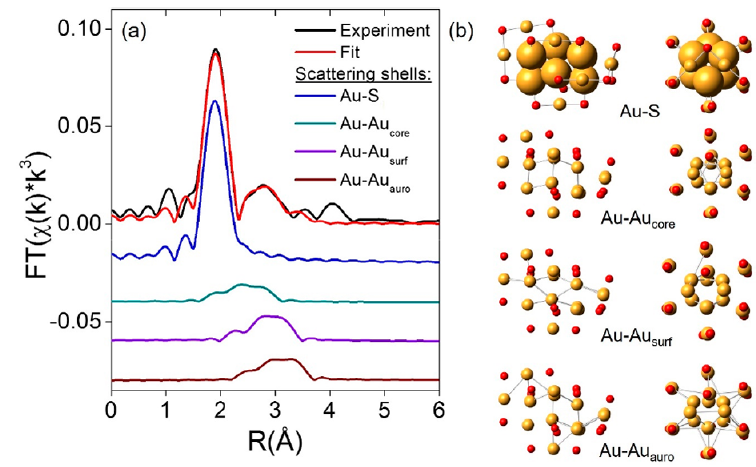
圖1 Au-巰基納米團簇[Au18(SC6H11)14]的FT-EXAFS多層擬合
研究思路與具體研究結果討論
作者使用了分別以環己硫醇(-SC6H11脂肪族小分子、疏水)與谷胱甘肽(-SG大分子、親水)作為配體的金納米團簇[Au18(SR)14],研究這兩種納米團簇在不同狀態(固相與溶液中)的原子結構變化。
結合同步輻射(X射線光譜)、理論計算(量子力學/分子力學模擬)與電子態密度的分析結果,作者發現谷胱甘肽相對于與環己硫醇能夠更好的保護Au納米團簇,其結構更穩定且剛性。同時證明了谷胱甘肽配體分子中存在大量的氫鍵,能夠有效的封裝Au納米團簇,同時其外殼上的S與Au原子極性更強,在溶液狀態下能夠給內核的Au納米團簇提供電子,保護其免受溶劑效應的影響。
光致發光光譜(溶液中)則顯示,相比于Au18(SC6H11)14,Au18(SG)14具有更強的發光能力。這種差別的原因也來源于谷胱甘肽配體對于Au納米團簇的更好保護導致Au納米團簇結構更穩定且剛性。相比之下,環己硫醇配體對金納米團簇[Au18(SC6H11)14]的保護程度很低。在溶液中,其配體形成的團簇外殼出現很大的空洞(cavity), 并導致其金屬核鍵長相對于固相明顯收縮。
這些結果預示,谷胱甘肽配體保護的金納米團簇,其剛性結構更適合于生物環境下的應用(如生物原位檢測);環己硫醇配體保護的金納米團簇,其表面配體殼的空洞結構和收縮的金屬內核則更適合于催化方面的應用。
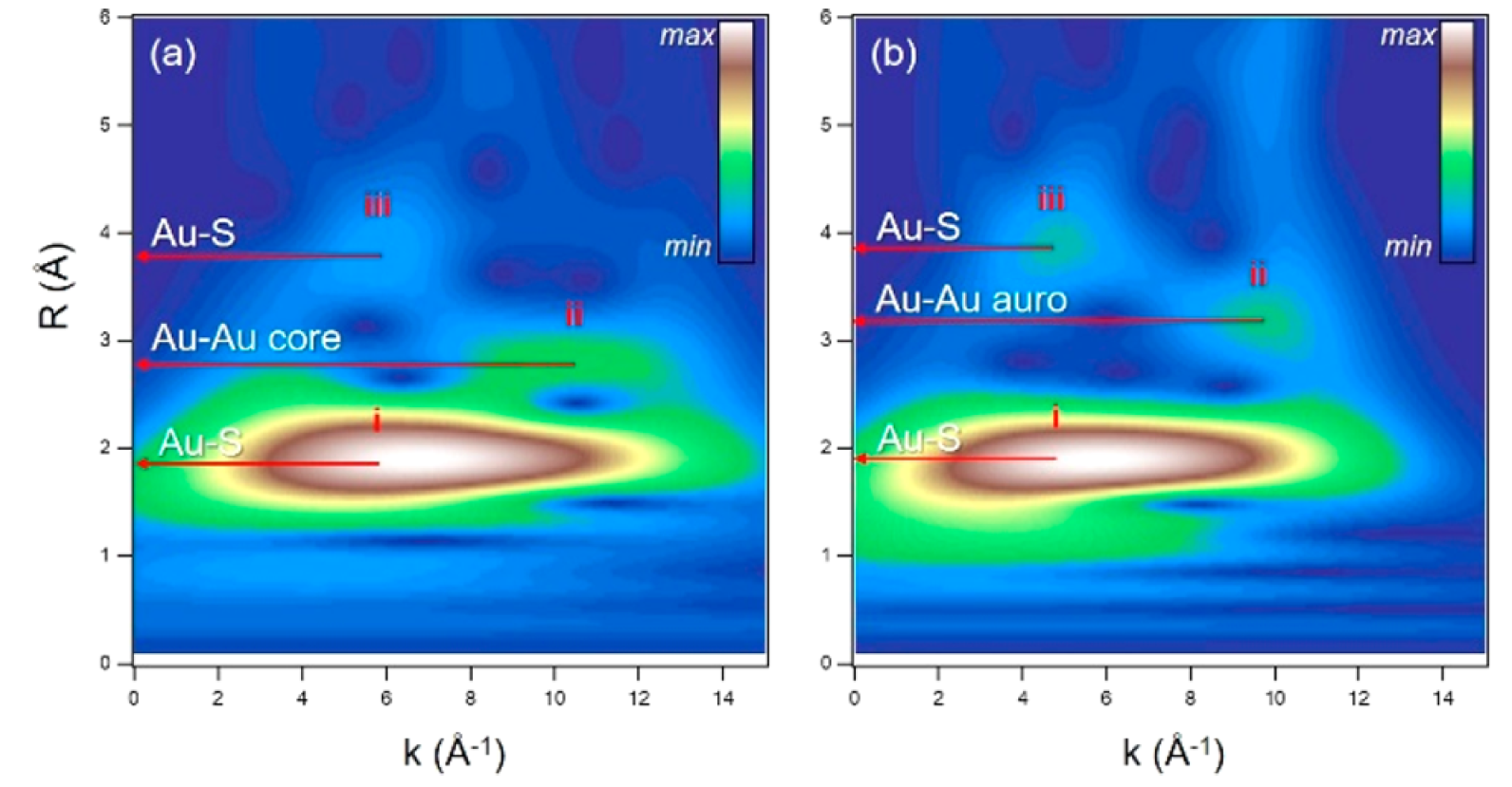
圖2 兩種Au-巰基納米團簇在溶液中的小波二維EXAFS
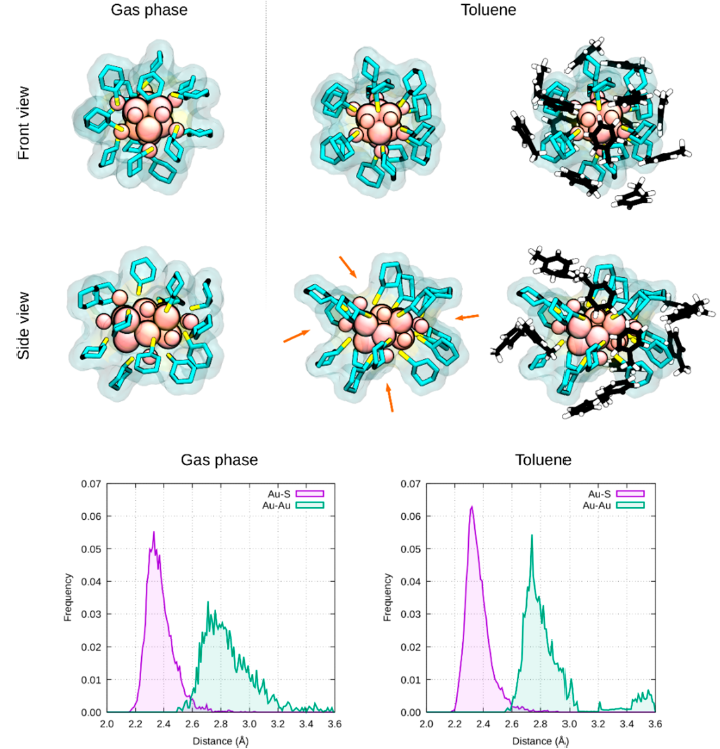
圖3 Au-巰基納米團簇(環己硫醇)的量子力學/分子力學模擬
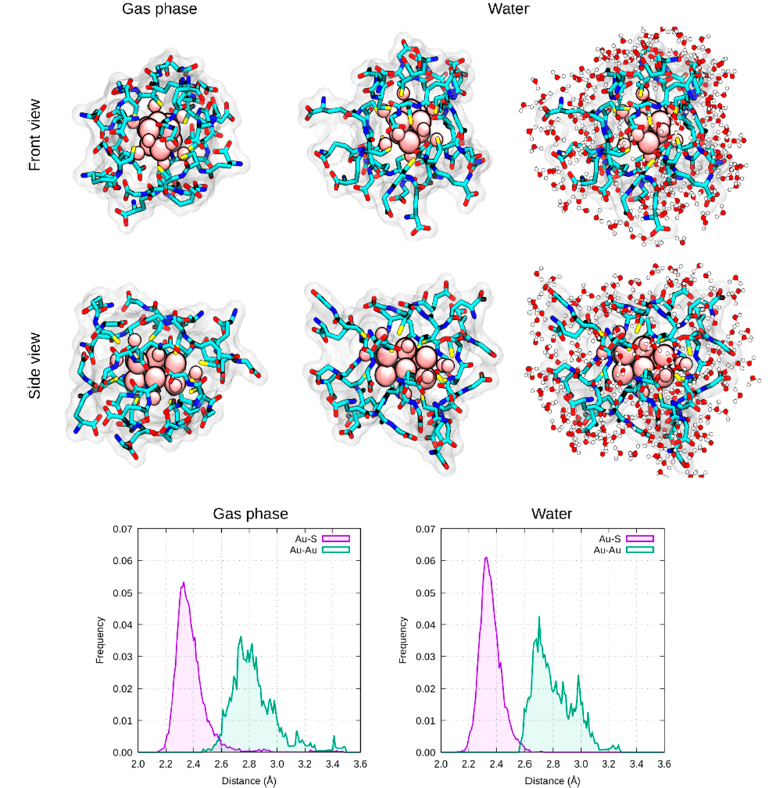
圖4 Au-巰基納米團簇(谷胱甘肽)的量子力學/分子力學模擬
總之,本工作系統的研究了不同巰基配體對金納米團簇在固相與溶液中的結構和性質的影響。從分子尺度,多角度解釋了巰基配體對金納米團簇中的配體效應(原子結構、溶劑影響與電子效應)。這些發現預計將對金納米團簇在催化和生物檢測方面的應用產生直接影響。
參考文獻:
Chevrier D M, Zhang P, et al. Molecular-scaleligand effects in small gold-thiolate nanoclusters[J]. Journal of the American Chemical Society, 2018.
DOI: 10.1021/jacs.8b09440
https://pubs.acs.org/doi/pdf/10.1021/jacs.8b09440











