電極電勢與物種的吸附脫附
電極表面物種的吸附、脫附與電極電勢有著密切的聯系。以光滑多晶Pt電極催化甲醇氧化為例,如圖1A所示。Pt表面甲醇氧化反應總是在高于一定電勢停止,而低于某一電勢時又發生,該過程主要與特定電極電勢下形成的含氧物種OHads有關(0.6~0.8Vvs. SHE)。圖1B示出,甲醇氧化發生在Pt表面欠電勢沉積的Hupd原子脫附(0. 4Vvs. SHE)之后。甲醇吸附后,并未出現甲醇的電化學氧化,電極電勢達到0.65V vs. SHE時,水離解,形成能使甲醇氧化與中間物種CO氧化的含氧物種此外,CO在Pt表面的強吸附,系Pt向其間的σ-π鍵反饋電子,顯然,隨著電極電勢正移,Pt向外輸出電子的能力減弱,這種反饋能力不斷削弱,σ-π鍵斷裂。因此,高電勢下,CO不能在Pt表面吸附。該過程說明電極電勢的變化直接影響著電極表面物種的形成、吸附與脫附。
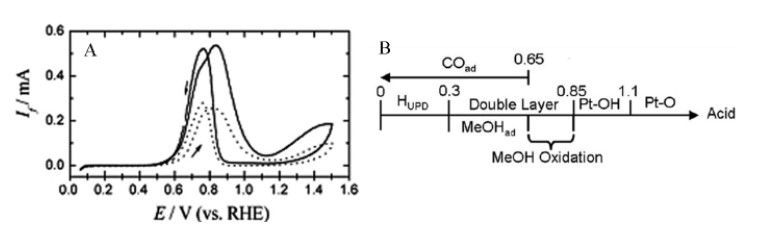
圖1. A. 光滑的多晶Pt在0.1mol·L-1甲醇+ 0.5 mol·L-1H2SO4溶液(虛線)與0.1mol·L-1甲醇+ 0.5 mol·L-1HClO4溶液(實線)室溫25℃下的循環伏安曲線,掃描速率10mV·s-1;B.酸性介質中Pt表面甲醇吸附氧化過程示意圖
電極電勢與物種吸附脫附間的關系,可據甲醇電化學氧化雙途徑機理,利用電極電勢(E),毒性中間體CO的表面覆蓋度(x)和含氧物種H2Oa的表面覆蓋度(y)三個主要的變量,建立能夠表征甲醇電化學氧化過程電勢振蕩的非線性動力學模型。甲醇氧化過程中毒性中間體CO的產生是電勢振蕩的誘因;含氧物種H2Oa的生成與消失是維系振蕩的直接原因;電極電勢E對CO和含氧物種H2Oa所參與反應的耦合反饋作用是甲醇電化學氧化呈現電勢振蕩的根本原因。電流密度較小時,電極電勢E對CO和含氧物種H2Oa所參與反應的耦合反饋作用并不強烈,CO的覆蓋度x和含氧物種H2Oa的覆蓋度y達到穩定態后不再隨時間變化,因而無電勢振蕩。隨著外控電流密度的增大(電勢正移),電極電勢E對CO和含氧物種H2Oa所參與反應的耦合反饋作用增強,即Pt表面CO的集聚使表面活性位的減少,相應電極電勢升高,含氧物種H2Oa產生速率增加促進CO的氧化,隨之電極電勢降低,至此產生電勢振蕩。當電流密度進一步增大時,甲醇電化學氧化按不生成毒性中間體CO的途徑進行,反應不存在產生電化學振蕩的誘因,即CO的形成與去除,因而無電勢振蕩現象。

圖 2. Pt(100),Pt(110)-1×1 和 Pt(111)晶面上 CO 在 0.5mol·L-1 H2SO4 溶液中的溶出伏安曲線
催化劑電子構型與物種的吸附脫附
除電極電勢的變化影響電極表面物種的形成、吸附與脫附外,催化劑本身的電子構型直接決定著物種吸脫附的難易程度,相同催化劑不同晶面因結構差異而有完全不同的催化活性。圖2示出,Pt低指數晶面對CO有不同的催化氧化活性,其因是Pt低指數晶面上物種的形成和吸附差異促進或阻礙了CO的電催化氧化。Markovic組發現,只有當電勢高于0.8V(vs. SHE)時,Pt(110)-(1×1)對弱吸附的COad,w才具有催化活性,而Pt(111)、Pt-(110)-(1×2),和Pt(100)在0.5V,即能夠催化氧化COad,w.低電勢下,Pt各低指數晶面催化氧化COad,w的活性順序:Pt(110)-(1×1)<<Pt(111)<<Pt(110)-(1×2)<<Pt(100)。表面形成的OHad主要控制COad,w的氧化移除。OHad可優先在Pt(100)、Pt(110)-(1×2)、Pt(111)晶面上吸附形成,因而,催化氧化COad,w的活性高。對高電勢下強吸附COb的氧化,各Pt晶面的催化活性順序發生變化:Pt(100)<Pt(110)-(1×2)<Pt(111)<Pt(110)-(1×1)。當電勢高于0.95V時,該電勢下各晶面催化活性的取決于CO、OHad和電解質中陰離子的競爭性吸附差異。
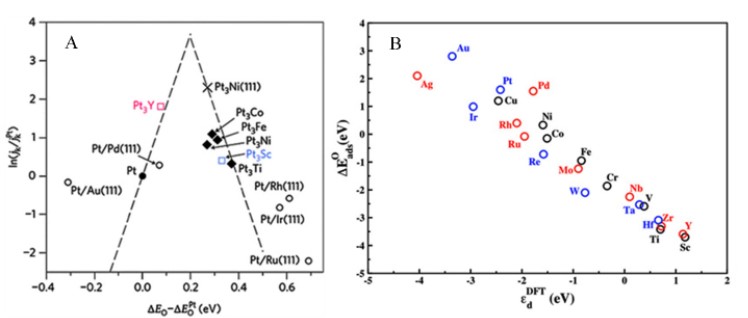
圖3. A. 金屬催化劑的催化活性與中間物種O吸附強度關系圖; B. 金屬催化劑的d帶中心值與O吸附強度的變化關系
催化劑對反應物種的吸附強度差異,同樣影響著其催化活性。圖3顯示,金屬催化劑的氧還原催化活性與氧還原中間物種氧原子的吸附強度呈火山型關系。催化劑對物種的吸附太弱使反應難以進行;太強則脫附困難,催化劑活性中心不容易釋放;只有其吸附強度在適宜范圍時,才具有最優催化活性。Norskov小組發現金屬催化劑對物種的吸附強度與金屬表面原子d帶中心值呈線性關系(如圖3B),即d帶中心理論。據此,可將金屬催化劑電子構型(d帶中心)與催化活性關聯起來,通過調節金屬催化劑電子構型改變物種的吸附強度,即可調控催化劑的催化活性。
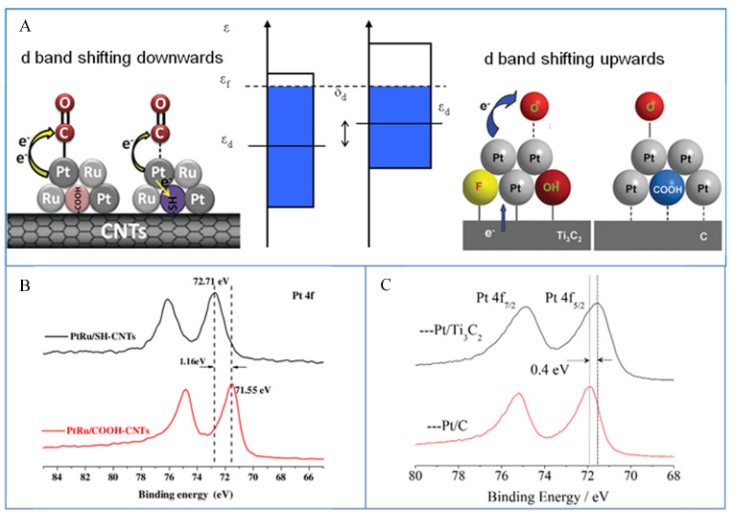
圖4. 催化劑載體間相互作用對催化劑d帶中心的調節示意圖(A)以及Pt在不同載體上XPS(B,C)譜圖
依據上述關系,作者課題組利用催化劑-載體間相互作用,通過改變載體來調節催化劑d帶中心。圖4示出,以巰基化修飾的碳納米管(SH-CNTs)為載體,因-SH中S有較大的電負性,致使Pt將電子轉移給載體SH-CNTs,增強了Pt與SH-CNTs間的相互作用,降低了金屬催化劑的d帶中心(XPS結合能變大),減弱了Pt與CO間的反饋π鍵,從而提高了催化劑的催化活性和抗CO中毒性。以Ti3C3為載體,Ti將電子轉移給Pt,增加了Pt的電子密度,此時,Ti—Pt間的強相互作用,使Pt以原子形式分散在載體表面,削弱了Pt—Pt鍵,從而相對于Pt/C,升高了Pt的d帶中心(XPS結合能降低)。
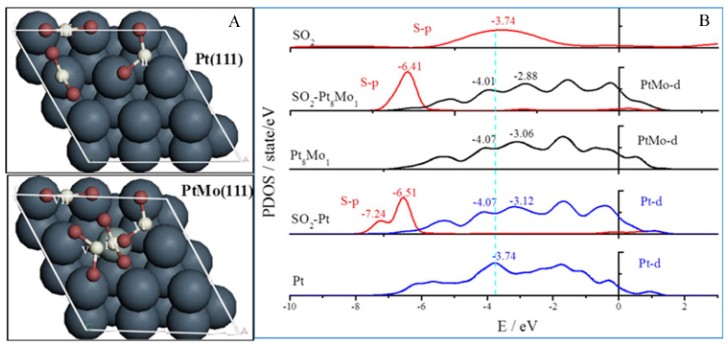
圖5. Pt、PtMo上SO2吸附構型(A)和Pt、PtMo吸附SO2前后的分態密度圖(B)
此外,合金也可有效的調節催化劑d能帶結構。密度泛函理論計算發現,PtMo合金中Mo將電子轉移給鄰近的Pt,增加了表面Pt原子的過剩電子,有效的維持了PtMo在毒性物種SO2吸附前后d能帶結構(如圖5所示)。Pt在SO2吸附前后d帶中心向Fermi能級方向移動了0.49eV,而PtMo的d帶中心僅向Fermi能級方向移動了0.19eV,證實Mo通過調節Pt的d能帶結構,提高了PtMo的抗SO2毒性。
參考文獻:
1. Kucernak A R, Offer G J. The role ofadsorbed hydroxyl species in the electrocatalytic carbon monoxide oxidationreaction on platinum[J]. Physical Chemistry Chemical Physics, 2008, 10(25):3699-3711.
2. Markovi? N M, Ross Jr P N. Surfacescience studies of model fuel cell electrocatalysts[J]. Surface ScienceReports, 2002, 45(4-6): 117-229.
3. 李莉, 魏子棟. 電化學催化的密度泛函研究[J]. 電化學, 2014, 20(4): 307-315. MLA
4. Baraldi A, Lizzit S, Comelli G, et al.Spectroscopic link between adsorption site occupation and local surfacechemical reactivity[J]. Physical review letters, 2004, 93(4): 046101.
5. XIA M R, LI L, QI X Q, et al. DFT studyon the mechanism of PtMo resistance to SO2 poisoning[J]. SCIENTIA SINICAChimica, 2011, 41(12): 1826-1832.











