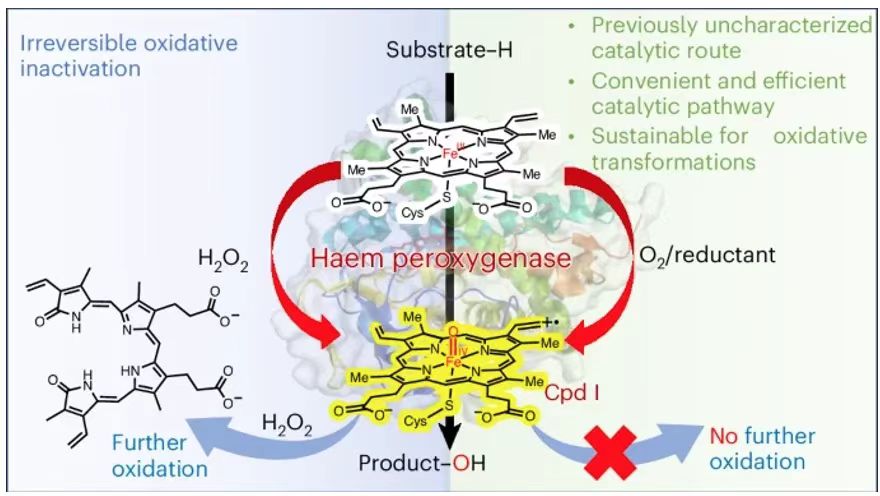
血紅素過氧化物酶(Haem peroxygenases)能夠使用H2O2向有機分子中修飾氧原子,是受到廣泛關注的生物催化劑。但是血紅素過氧化酶的應用受制于使用外源性H2O2導致不可逆的氧化失活。有鑒于此,廈門大學王斌舉教授、湖北大學李愛濤教授等報道血紅素過氧化物酶的一種新型催化反應,這種新型催化反應使用O2和小分子還原劑(抗壞血酸、脫氫抗壞血酸(DHA))實現反應。實驗和理論計算的結果表明DHAA(脫氫抗壞血酸DHA的水化物分子)是關鍵的共反應物分子,用于活化O2分子產生催化活性的鐵氧(oxyferryl)血紅素化合物I。此外,這項研究展示了這種O2/還原劑依賴性反應能夠用于多種多樣的血紅素過氧化酶,展示了這種生物催化方法是重要的單氧酶功能。這種策略避免使用H2O2,因此避免了酶的不可逆失活問題。最后,反應能夠以優異的產量大量的合成手性、高附加值產物,揭示了這種過氧化酶策略在可持續化學轉化中的應用前景。圖1. 血紅素氧化酶的各種催化反應生成鐵氧(oxyferryl)血紅素化合物I(CpdI)
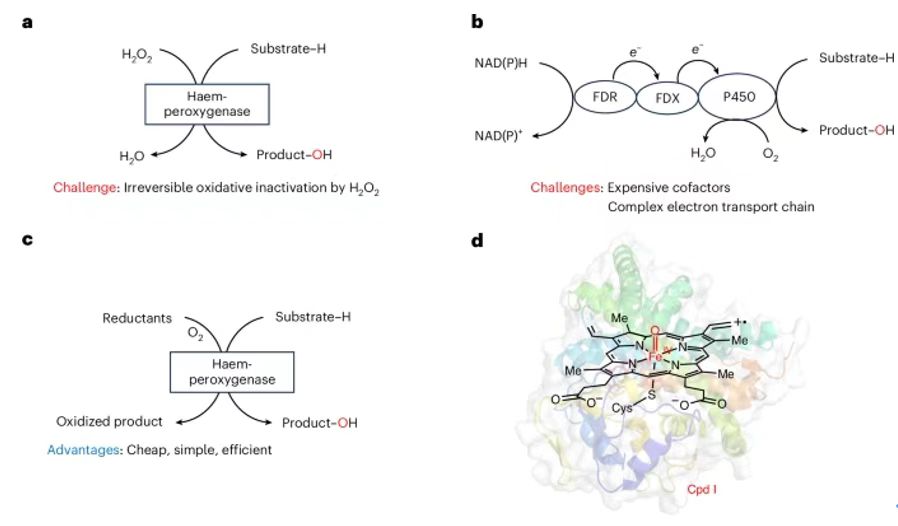
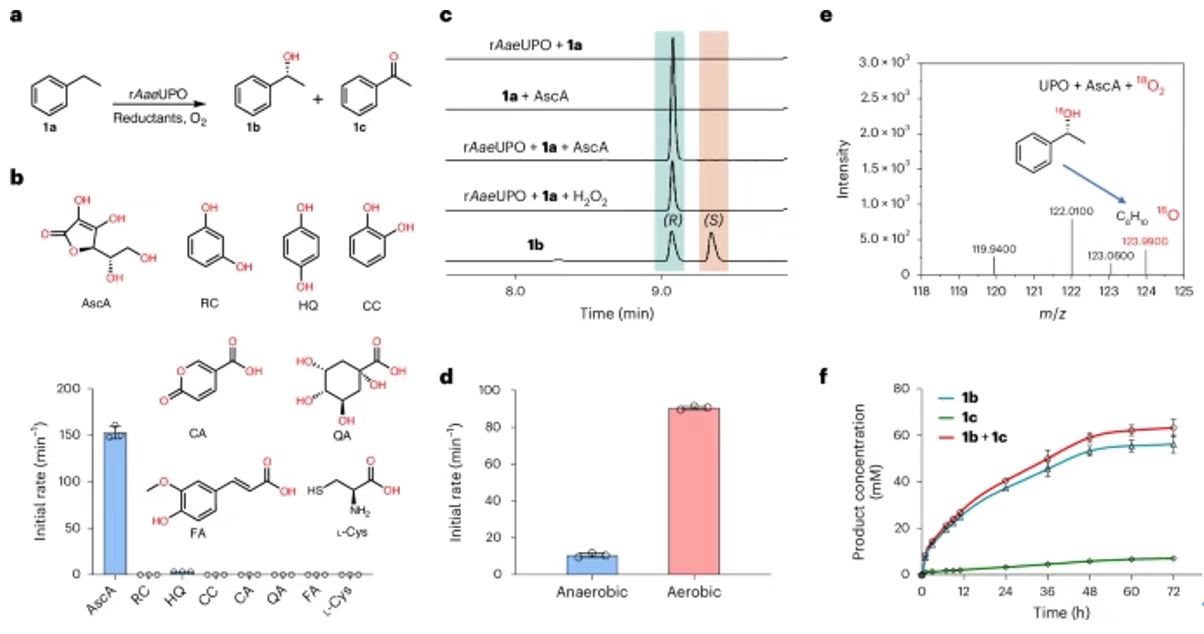
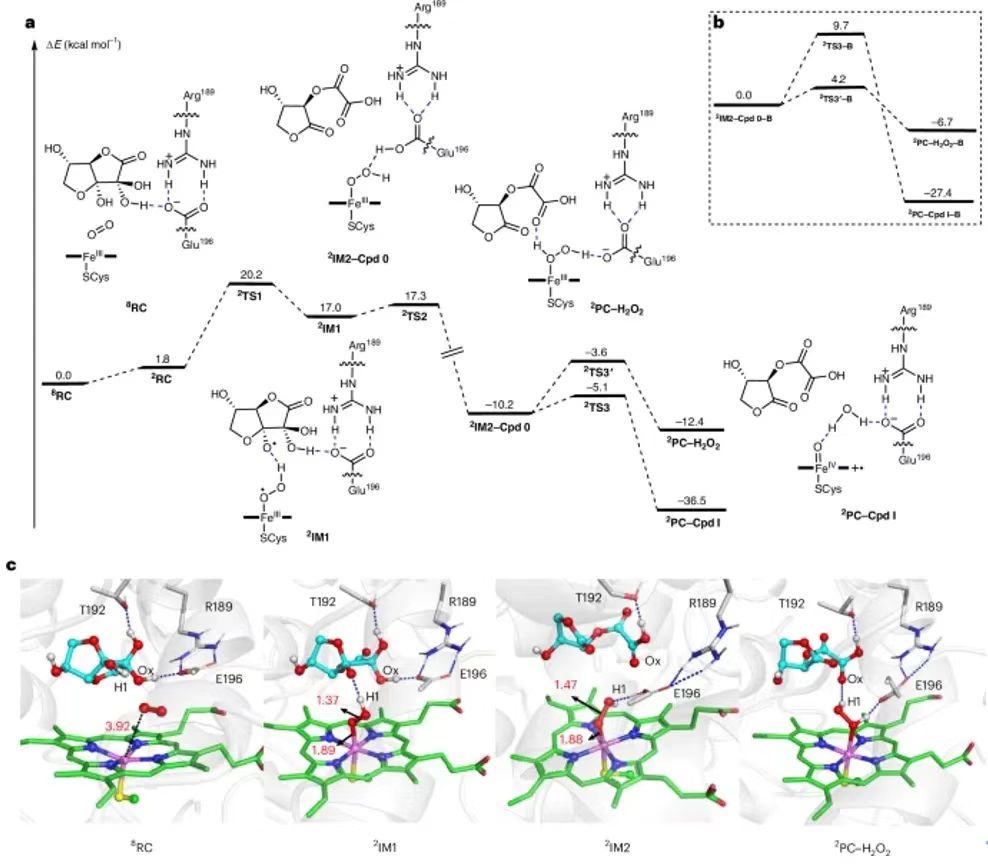
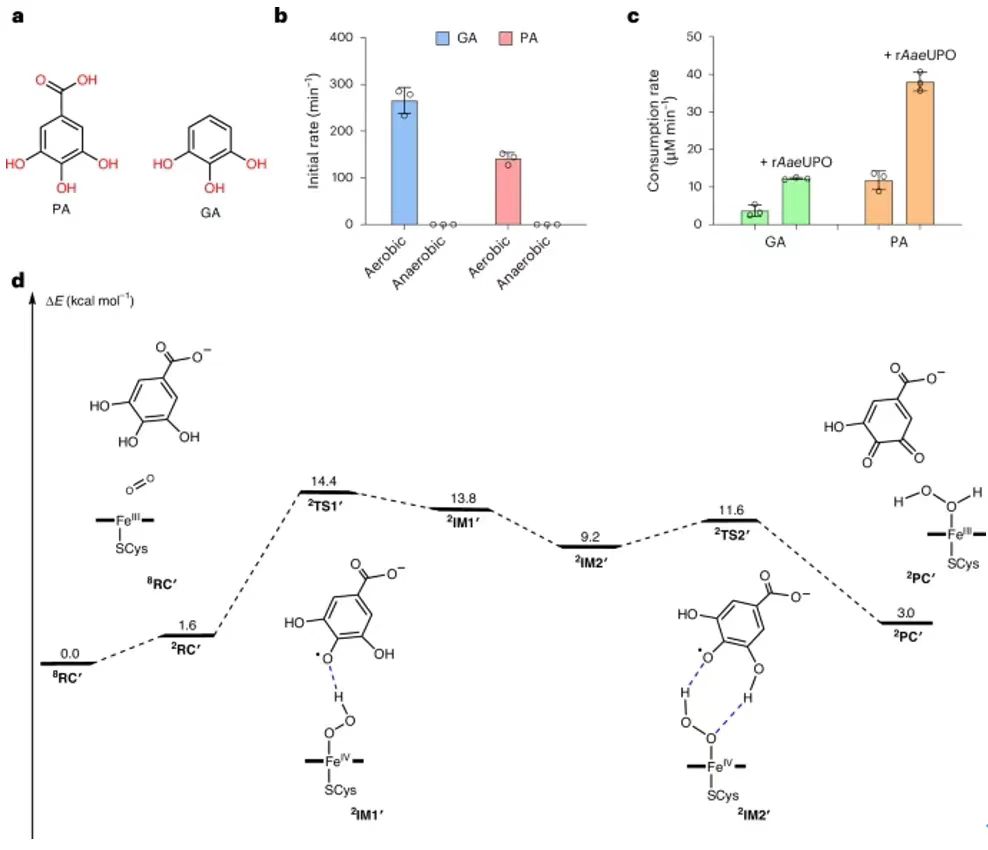
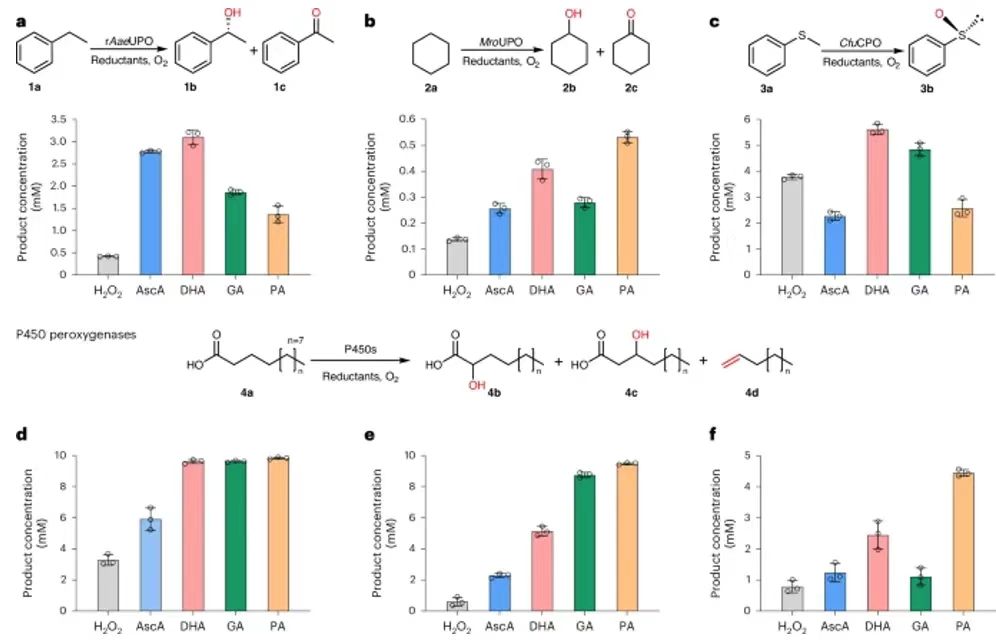
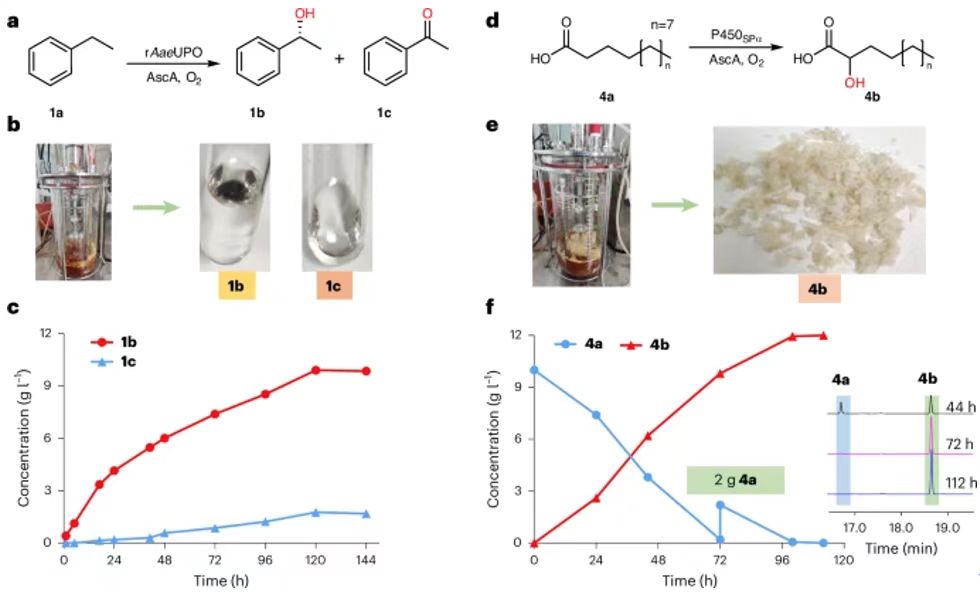
在各種血紅素過氧化酶中,非特異性過氧化酶(UPO)能夠使用H2O2作為氧化劑,向含有惰性C-H化學鍵的有機化學物引入氧原子(圖1a)。除了UPOs之外,一些細胞色素P450s(比如CYP152過氧化酶,OleTJE、P450SPα、P450BSβ)同樣是H2O2依賴性過氧化酶(圖1a)。此外,除了經典P450單氧化酶需要使用氧化還原配合物以及還原劑(DAD(P)H)活化O2分子(圖1b),UPOs和P450過氧化酶具有更簡單的結構,能夠與H2O2直接生成活性鐵氧血紅素化合物I(CpdI),避免了復雜的電子轉移鏈(圖1d)。雖然UPOs和P450過氧化酶是具有選擇性的氧官能團化催化劑,催化反應需要加入外源性H2O2,這導致酶催化劑的不可逆氧化失活。這個問題嚴重限制了其在選擇性氧官能團化的工業應用。圖2. 體系含有小分子還原劑的rAaeUPO催化1a羥基化反應為了研究UPOs是否能夠利用O2作為氧化反應的氧化劑,研究了一種研究非常廣泛的rAaeUPO,以乙基苯(1a)的羥基化反應作為模型反應。向反應體系加入不同小分子還原劑(圖2a,b)。測試結果表明,只有當反應體系同時具有rAaeUPO、反應物、AscA,能夠生成(R)-1-苯乙醇(1b)(圖2c)。為了進一步研究反應是否是O2依賴性,對無氧、有氧體系的反應情況都進行研究。研究結果表明反應在有氧條件下具有非常好的反應活性,但是在無氧條件下的反應活性非常低(圖2d)。這個現象表明rAaeUPO的催化氧化反應是AscA和O2都具有依賴性。此外,通過18O2同位素標記驗證了氧化產物中的氧原子來自18O2(圖2e)。最后,測試了rAaeUPO酶催化劑,以1a作為反應物,在AscA存在情況的催化反應,反應生成了60 mM的產物,反應的TON達到632,100?±?37,073(圖2f)。圖3. 鑒定rAaeUPO催化反應中的真實反應物DHA人們研究發現,在溶液相中,AscA能夠氧化生成DHA,隨后水解生成2,3-二酮-L-古洛糖酸(DKG)。此外,DHA在水中主要以水化形式存在(圖3a)。作者認為DHA或者水化DHAA或者DKG有可能是反應中的真實氧化劑。因此,分別使用AscA、DHA、DKG作為還原劑,分別測試rAaeUPO催化反應的催化反應活性(起始反應速率)。測試結果表明,當體系加入DHA還原劑,起始反應速率達到144 min-1,起始反應速率比AscA快58 %。當體系加入的還原劑是DKG,反應沒有產生生成。實驗結果表明DHA(或DHAA)可能是UPO催化反應的真正還原劑(圖3b)。之后,分別在有氧和無氧條件測試反應,發現只有在有氧條件下實現顯著的催化活性,這個結果表明反應的發生同時需要DHA和O2。這項研究發現了DHA在UPO催化反應中的關鍵作用,當使用還原性更強的DTT時,加入10 mM DTT導致反應完全無法發生(圖3d)。當使用DHA作為還原劑,加入DTT導致酶催化活性明顯降低(圖3e),這是因為DTT影響了DHA恢復到AscA。以上結果驗證了DHA(或者DHAA)在反應中起到真正的還原劑,而不是AscA。隨后,研究DHA的消耗與rAaeUPO的依賴性關系。研究結果表明,當rAaeUPO存在時,DHA的反應速率提高6倍(圖3f)。對比的結果表明,AscA的消耗速率明顯低于DHA(圖3f)。研究實驗發現,催化反應與外源性H2O2不相關(圖3g)。理論計算研究。通過理論計算研究UPOs在DHA還原劑存在的催化反應機理。如圖4a所示,反應物可能是水化的縮醛DHA、DHAA。DFT理論計算結果表明水化DHA生成DHAA是放熱過程,表明DHA能夠以水化形式在溶液相存在。如圖4b所示,通過分子動力學模擬計算,發現DHAA能夠穩定的結合在UPO的活性位點,但是DHAA通過E196、R189、T192之間具有氫鍵相互作用。這個結果表明,DHAA是UPO催化反應的還原劑。并且計算結果與實驗結果相符。圖5. 驗證rAaeUPO催化反應中,GA和PA分子是共同反應物除了在新鮮植物組織中發現的DHA和AscA,本研究認為木質素組織中豐富的多酚化合物能夠作為UPO催化氧化反應的還原劑。因此,在rAaeUPO催化1a羥基化反應中分別加入GA或PA,測試催化反應(圖5a)。實驗結果表明,GA和PA都能夠作為共同反應物,表現優異的催化活性,起始反應速率分別達到265 min-1和141 min-1(圖5b)。這個性能甚至超過了DHA作為共同反應物的催化反應速率。當加入UPO酶,顯著加快GA和PA的消耗速率(圖5c)。這些結果表明GA和PA是UPO催化氧化反應的還原劑。理論計算研究。通過理論計算研究多酚還原劑在UPO酶催化氧化活化O2機理。使用GA作為還原劑,發現GA與DHAA非常類似,O2與GA摘取的氫之間耦合,生成·OOH自由基并且與Fe(III)配位(圖5d)(中間體2IM1′)。然后,GA自由基的OH官能團與·OOH形成氫鍵相互作用,產生更加穩定的中間體2IM2′。研究發現·OOH自由基容易與相鄰酚自由基的OH官能團發生摘氫原子反應,生成Fe(III)-H2O2中間體。圖6. UPO-過氧化酶和P450-過氧化酶分別使用不同還原劑的催化反應性能分別測試了AscA、DHA、GA、PA作為還原劑,各種血紅素過氧化酶的O2/還原劑依賴性反應。結果表明,MroUPO(環己烷羥基酶,Marasmius rotula來源)、CfuCPO(苯甲硫醚的磺氧化酶,Caldariomyces fumago來源)、P450過氧化酶(月桂酸氧化酶,分別為P450SPα(Sphingomonas paucimobilis來源)、P450BSβ(Bacillus subtilis來源)、OleTJE(Jeotgalicoccussp. ATCC 8456來源)五種代表性的過氧化酶在加入還原劑之后,都表現更高的催化活性(圖6a,b)。對于CfuCPO(對H2O2的容忍性更高),只有DHA和GA兩種還原劑能夠比H2O2-催化活性更強(圖6c)。P450SPα和P450BSβ對月桂酸的羥基化反應中,各種還原劑都表現比H2O2-催化活性更高(圖6c,e)。特別是,以GA和PA作為還原劑,實現了100 %的轉化。在P450OleTJE催化的脫羧反應,加入還原劑后表現比H2O2-催化活性更好的效果(圖6f)。這些研究結果表明,血紅素過氧化酶的O2/還原劑依賴性催化反應具有廣泛的兼容性,展示了優異的催化活性。比較O2/還原劑依賴性催化反應和H2O2-依賴性催化反應圖7. 比較O2/還原劑-依賴性、H2O2-依賴性rAaeUPO催化體系為了進一步研究O2/還原劑依賴性比傳統H2O2-依賴性路線的優勢,通過光譜表征研究不同濃度的H2O2或者AscA的反應。發現rAaeUPO加入外源性H2O2,UV-Vis光譜表征的Soret峰(ferric Fe的停留態)強度逐漸降低,并且產生氣泡。相比的UPO/DHAA/O2體系,生成單一Fe(III)-H2O2中間體,避免了H2O2的結合和反應。因此,UPO/DHAA/O2體系的反應能夠非常好的控制Cpd I的生成以及反應物氧化,避免了血紅素鐵的損壞,避免酶的失活。此外,由于H2O2具有強氧化性,因此使用外源性H2O2的體系無法應用于容易H2O2氧化的反應物(圖7)。研究結果表明,O2/(AscA/DHA)-依賴性催化反應能夠避免使用外源性H2O2,因此適用于容易被H2O2氧化的反應物。圖8. 使用AscA作為還原劑的大量反應合成高附加值產物為了展示O2/還原劑依賴性過氧化酶催化體系的工業應用前景,通過放大實驗,加入還原劑制備高附加值產品(圖8)。從兩個反應進行驗證,分別是rAaeUPO催化芐基羥基化(1a)制備(R)-1-苯乙醇(1b)、P450SPα催化4a羥基化制備α-羥基月桂酸(4b)。使用價格便宜且容易得到的AscA作為還原劑。測試rAaeUPO催化1a的羥基化反應,當200 mM 1a、40 g AscA、0.25 μM rAaeUPO的反應,能夠生成9.9 g L-1的對映純1b((R)-1-苯乙醇)和1.8 g L-1的苯乙酮(1c),該反應的TON達到395,600,比H2O2-依賴性反應的性能(5 g L-1)更好。測試P450SPα催化4a的α-羥基化反應,當使用10 g4a,30 g AscA,1.5 μM P450SPα,反應的轉化率達到>99 %,生成11.82 g α-羥基化月桂酸(4b),分離產率達到91 %,TON達到43,760,這個結果比以往報道的結果高6倍。這些放大實驗結果表明使用還原劑的過氧化酶催化反應體系在制備高附加值化合物中的應用前景。這項研究展示了O2/還原劑-依賴性血紅素過氧化酶催化體系的高效催化性能。在這種酶催化反應過程中,新鮮植物組織還原劑(DHA、AscA)或者木質素組織常見的多酚化合物還原劑(GA、PA)能夠作為共同反應物用于催化氧化反應。對于AscA或者DHA作為還原劑的UPOs酶催化反應,通過實驗和理論計算研究表明DHAA是真正活化O2分子還原劑,產生鐵氧血紅素(Cpd I)。在這個反應過程中,在UPO的結合口袋內通過催化反應生成Fe(III)-H2O2中間體,這個過程避免過量H2O2,因此緩解血紅素催化位點的損害,避免酶的失活。使用GA和PA作為還原劑的情況與DHA和AscA不同,GA或PA還原劑在緩沖溶液產生過量H2O2(酶催化口袋外部),這在一定程度上阻礙了酶催化活性。作者發現O2/還原劑-依賴性酶催化反應過程能夠用于其他血紅素過氧化酶催化過程(包括UPO、CPO、CYP152)。此外,本文研究發現,AscA/DHA還原劑的體系對于容易被H2O2氧化的反應物展示了高效率和選擇性氧化。總之,這些研究結果表明血紅素過氧化酶能夠作為單氧化酶進行催化反應,取決于環境的O2以及外部供電子體(或小分子還原劑)。這種O2-依賴性催化反應對未來的生物催化體系的發展提供啟示,而且在脂肪酸的生理代謝、木質素降解、植物被致病菌感染等過程中起到作用。最后,這項研究通過擴大反應體系的量(rAaeUPO催化乙基苯的羥基化、P450SPα催化月桂酸的α-羥基化)展示了這種O2依賴性酶催化反應的實用前景。這項研究實現了優異的(R)-1-苯乙醇、α-羥基月桂酸產量(產物的量達到或超過10 g L-1)。這些產物是食品貧、化妝品、制藥領域極為常見。進一步,本研究將關注于推動這些先進技術用于工業量級制備更多高附加值產品。通過先進的突變技術進化技術增強反應的立體選擇性,有助于進一步提高這種催化氧化體系的功能。Deng, D., Jiang, Z., Kang, L.et al. An efficient catalytic route in haem peroxygenases mediated by O2/small-molecule reductant pairs for sustainable applications. Nat Catal 8, 20–32 (2025).
DOI: 10.1038/s41929-024-01281-7https://www.nature.com/articles/s41929-024-01281-7