編輯總結
在兩個鏡像異構體中僅形成一種取向的碳-氮鍵,對于制備眾多藥物和農用化學品至關重要。盡管已經開發出多種催化劑來實現這一目標,但它們通常依賴底物上的特定位點來引導反應過程。本文報道了在理論指導下,設計出一種包覆型錐狀配體,用于銅催化的碳-氮鍵構建,即使在缺乏明顯識別位點的烷基碘化物中也能實現該反應。這一方法可高選擇性地合成多種手性胺類化合物。——Jake S. Yeston
研究背景
在不對稱催化中,區分相似的烷基基團是一項重大挑戰。而對未活化的前手性烷基自由基實現對映選擇性控制更為困難,這是由于它們具有高反應性,且與手性催化劑之間的相互作用有限。
鑒于此,南方科技大學劉心元教授與浙江大學洪鑫教授合作在Science期刊上發表了題為“Asymmetric amination of alkyl radicals with two minimally different alkyl substituents”的最新論文。在本研究中,他們報道了一種銅催化的不對稱胺化反應,針對未活化的前手性仲烷基自由基,利用專門設計的手性陰離子多齒配體,通過自由基取代反應實現該轉化。該方法可高效地合成高對映純度的α-手性烷基胺,并成功實現了一系列重要藥物分子的對映選擇性正式合成。
機理研究表明,配體外圍的大體積修飾有助于構建出一個截錐形手性空腔,從而通過空間位阻和非共價相互作用實現精確的對映體區分。該策略在涉及多種未活化前手性烷基自由基和親核試劑的不對稱轉化中展現出廣闊的應用潛力。
研究亮點
(1)本研究首次實現了對未活化手性中心的二級烷基自由基進行催化不對稱胺化反應,合成出α-手性烷基胺產物,無需依賴鄰近或遠程官能團輔助,突破了長期以來不活化自由基對映選擇性控制的難題。
(2)實驗通過設計一類體積龐大的陰離子N,N,P型配體與銅催化劑形成錐狀手性囊袋結構,成功構建出具有空間限域和非共價相互作用的反應環境,從而實現了對兩個相似烷基基團之間的立體區分,顯著提高了反應的對映選擇性。此外,該方法具有以下顯著特點:
底物范圍廣泛:不僅適用于一級、二級、三級α-烷基碘代物,也適用于環烷基底物,表現出優異的對映選擇性;
無需官能團輔助:體系無需依賴α位或遠程導向基團,適用范圍更廣,提升了合成適用性;
擴展性強:該策略成功應用于對簡單烷烴底物的對映選擇性C–H胺化反應,顯示出其在C–H鍵官能團化領域的潛力;
實用價值高:該方法被用于高對映選擇性合成抗癌藥物伊布替尼的關鍵中間體,展示了在藥物合成中的實際應用前景。
圖文解讀
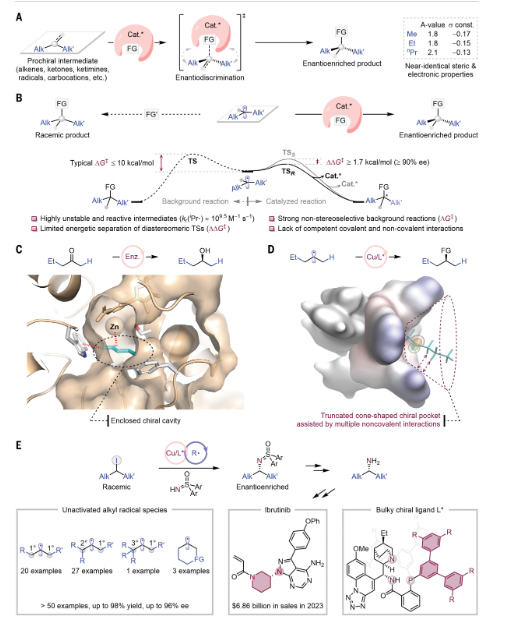
圖 1. 未活化前手性烷基自由基的催化不對稱官能化的開發背景
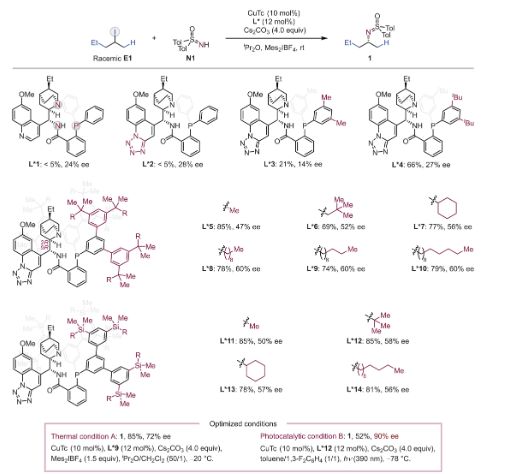
圖 2. 合理設計的配體和反應發展
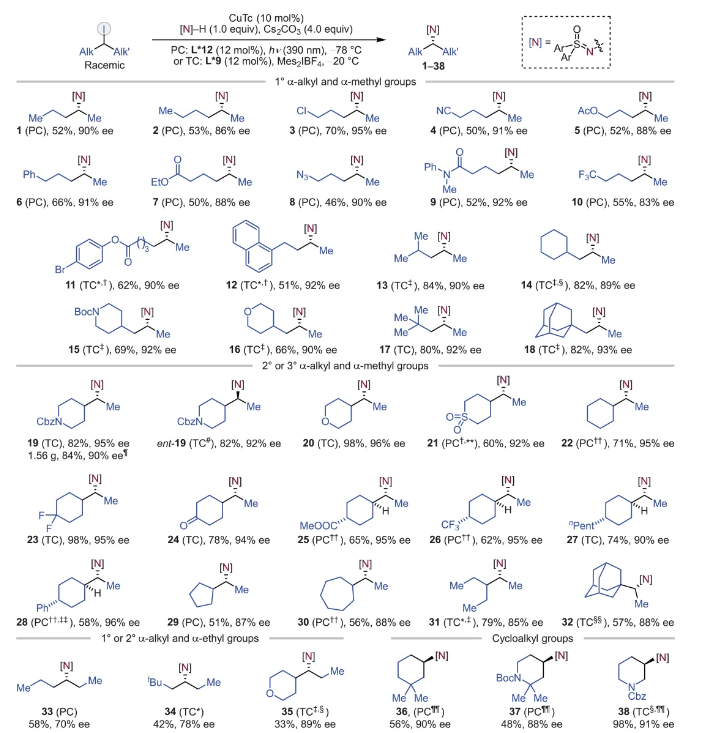
圖 3. 外消旋未活化烷基碘化物的范圍
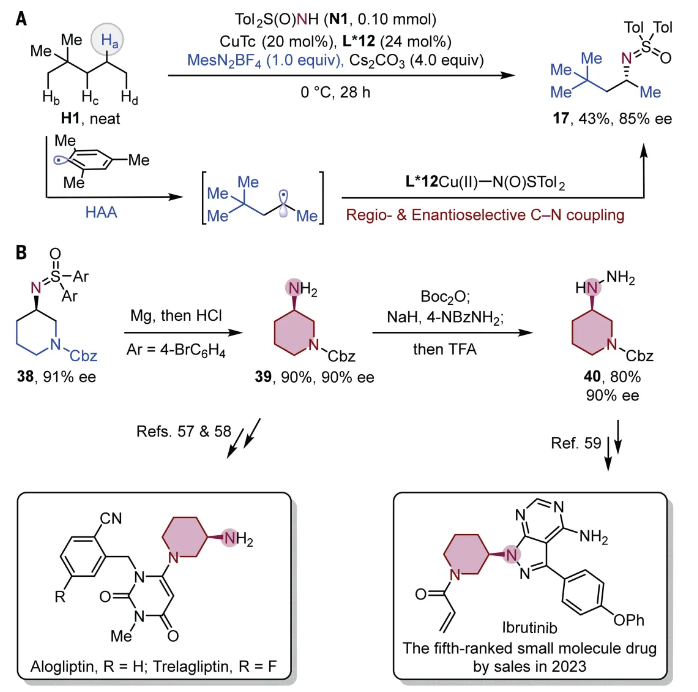
圖 4. 烷烴底物的不對稱自由基 C–H 胺化和合成轉化。
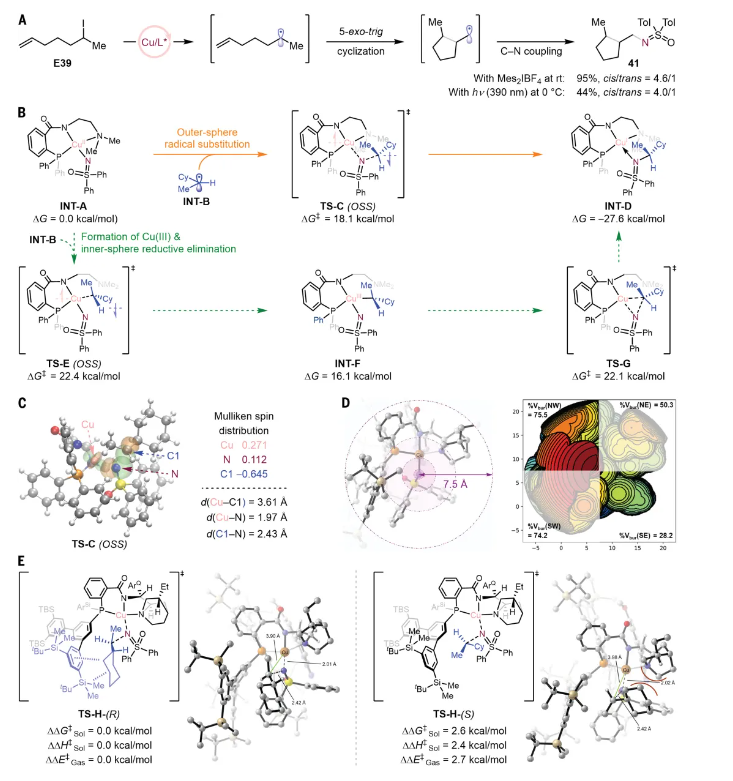
圖 5.機理研究
結論展望
本文開發了一種平臺,利用銅催化劑與手性陰離子型 N,N,P 配體協同作用,實現了非活化前手性仲烷基自由基的高度不對稱胺化反應。實現對兩個烷基基團之間高效對映選擇性的關鍵,在于精心設計的手性配體,這些配體構建了一個受限的反應環境。
該不對稱 C–H 胺化反應的成功,不僅為該領域的進一步發展奠定了初步基礎,也為引入其他自由基前體提供了可能。作者預期,這一策略將為未來涉及更復雜的非活化前手性烷基自由基及多樣親核試劑的不對稱反應開辟新路徑。
原文詳情:
Yu-Feng Zhang et al. ,Asymmetric amination of alkyl radicals with two minimally different alkyl substituents.Science388,283-291(2025).DOI:10.1126/science.adu3996












