1. JACS:可滲透膜、對(duì)環(huán)境敏感的染料用于在活細(xì)胞內(nèi)進(jìn)行生物傳感
具有對(duì)環(huán)境敏感特性熒光的染料對(duì)于研究活細(xì)胞中的蛋白質(zhì)活性的動(dòng)力學(xué)具有很好的幫助。當(dāng)染料連接到蛋白質(zhì)上后,其產(chǎn)生的熒光可以對(duì)蛋白質(zhì)的構(gòu)象變化、轉(zhuǎn)譯后的情況及蛋白質(zhì)的相互作用進(jìn)行反映。然而,這種染料-蛋白偶聯(lián)物的應(yīng)用目前還很有限,原因在于很難將它們裝入細(xì)胞中進(jìn)行進(jìn)一步的應(yīng)用。北卡羅萊納大學(xué)教堂山分校Klaus M. Hahn團(tuán)隊(duì)設(shè)計(jì)了一個(gè)可滲透膜的、對(duì)環(huán)境敏感的生物傳感器熒光團(tuán),它可以滲透穿過(guò)細(xì)胞膜并且可以通過(guò)非自然氨基酸(UAA)的誘變作用附著在活細(xì)胞內(nèi)的蛋白質(zhì)上。研究結(jié)果證明,mero166可以在細(xì)胞內(nèi)對(duì)UAA進(jìn)行標(biāo)記,由此對(duì)小GTP酶 Cdc42具有很好的生物傳感效果。而將mero166與小分子進(jìn)行結(jié)合則會(huì)得到一個(gè)可滲透膜的探針,從而可以在細(xì)胞中對(duì)DNA甲基轉(zhuǎn)移酶G9a進(jìn)行有效定位。
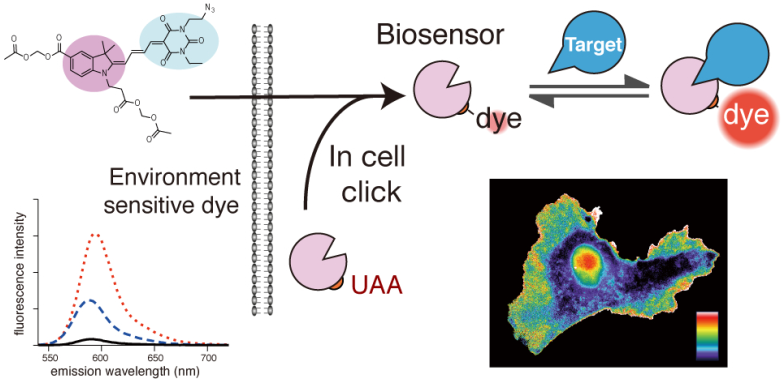
Christopher J. MacNevin, Takashi Watanabe, Klaus M. Hahn. et al. Membrane-permeant, environment-sensitive dyes generate biosensors within living cells. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.8b09841
https://pubs.acs.org.ccindex.cn/doi/10.1021/jacs.8b09841
2. Angew:在NaNdF4上包覆普魯士藍(lán)會(huì)產(chǎn)生新的交叉弛豫通路增強(qiáng)光熱效果
在熒光材料中,致敏劑之間的交叉弛豫通常被認(rèn)為是有害的,而在光熱劑中則是有利的。新加坡南洋理工大學(xué)Timothy Thatt Yang Tan團(tuán)隊(duì)和南京郵電大學(xué)范曲立教授團(tuán)隊(duì)合作,首次將普魯士藍(lán)(PB)包覆在NaNdF4納米顆粒上制備出核-殼納米復(fù)合物,結(jié)果發(fā)現(xiàn)在Nd3+離子的階梯狀能級(jí)與PB的連續(xù)能帶之間會(huì)產(chǎn)生新的交叉弛豫通路來(lái)提高光熱轉(zhuǎn)換效率,實(shí)驗(yàn)也對(duì)增強(qiáng)的光熱效應(yīng)的機(jī)理進(jìn)行了研究。體內(nèi)光聲成像和光熱治療結(jié)果則證實(shí)了這一增強(qiáng)的光熱試劑的應(yīng)用價(jià)值和潛力。這一工作提出了在不同材料間產(chǎn)生新的交叉弛豫路徑的策略,進(jìn)而為設(shè)計(jì)增強(qiáng)型光熱試劑提供了新的方法。

Zhongzheng Yu, Wenbo Hu, Quli Fan, Timothy Thatt Yang Tan. et al. Generating New Cross Relaxation Pathways by Coating Prussian Blue on NaNdF4 for Enhanced Photothermal Agents. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201904534
http://dx.doi.org/10.1002/anie.201904534
3. ACS Nano:納米粒子的體內(nèi)清除途徑
了解納米粒子是如何從體內(nèi)被清除的,是實(shí)現(xiàn)其臨床轉(zhuǎn)化必需條件。許多的納米制劑的尺寸較大(> 6 nm)也無(wú)法被生物降解,所以它們不能由腎臟進(jìn)行清除。那么,這些納米材料清除的重要途徑之一就是通過(guò)肝膽,但是目前人們對(duì)其中的轉(zhuǎn)運(yùn)機(jī)理還不是很清楚。多倫多大學(xué)Warren C. W. Chan教授團(tuán)隊(duì)探索了納米材料通過(guò)肝膽進(jìn)行體內(nèi)清除的機(jī)理。肝膽清除一般是通過(guò)以下幾種途徑:肝竇、竇周隙、肝細(xì)胞、膽管和腸道等。實(shí)驗(yàn)發(fā)現(xiàn),納米顆粒與肝非實(shí)質(zhì)細(xì)胞之間的相互作用決定了其清除的“命運(yùn)”,因?yàn)槠淝宄肪€的每一步中都含有細(xì)胞,這些細(xì)胞可以改變納米材料的物理化學(xué)特性,從而影響它們的糞便清除效率。研究發(fā)現(xiàn),若去除了枯否細(xì)胞,則納米材料通過(guò)糞便的排出量可以增加10倍以上。結(jié)合已有的研究結(jié)果,這一工作可以幫助人們對(duì)于納米材料的體內(nèi)清除途徑建立一個(gè)更加系統(tǒng)完善的認(rèn)識(shí)。
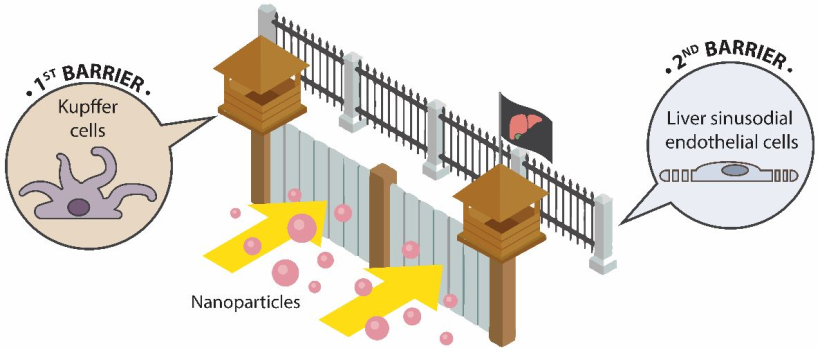
Wilson Poon, Warren C. W. Chan. et al. Elimination Pathways of Nanoparticles. ACS Nano. 2019
DOI: 10.1021/acsnano.9b01383
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsnano.9b01383
4. AM:比色多功能傳感方法用于構(gòu)建健康監(jiān)測(cè)系統(tǒng)
韓國(guó)成均館大學(xué)Sunkook Kim團(tuán)隊(duì)和韓國(guó)漢陽(yáng)大學(xué)Hanseung Lee團(tuán)隊(duì)合作研制了一種比色多功能基于光透射的耐久性健康監(jiān)測(cè)系統(tǒng)。該系統(tǒng)包括基于4個(gè)銦鎵氧化鋅(IGZO)的光電晶體管組成的陣列、一個(gè)發(fā)射波長(zhǎng)為405 nm的光源以及對(duì)pH和氯具有選擇性的變色膜組成。在405 nm波長(zhǎng)的光照下,處于應(yīng)力腐蝕狀態(tài)的膜會(huì)對(duì)pH和氯做出進(jìn)而出現(xiàn)顏色的改變,其透射光強(qiáng)度也會(huì)隨之變化,這種變化會(huì)被光電晶體管陣列以電流的形式接收。當(dāng)pH值在10到12之間時(shí),Ids和R (Ids/IpH 12)與pH值成反比,即當(dāng)pH值從12降到10時(shí),Ids和R增加約103倍。而對(duì)氯進(jìn)行檢測(cè)時(shí),隨著氯的濃度增加0.05 wt%,Ids和R (Ids/ICl 0 wt%)則會(huì)增加近50倍,當(dāng)氯濃度達(dá)到0.30 wt%時(shí),Ids和R則會(huì)增加103倍。該比色傳感系統(tǒng)具有較高的穩(wěn)定性、靈敏度和多種功能,是一種新型的健康診斷工具。
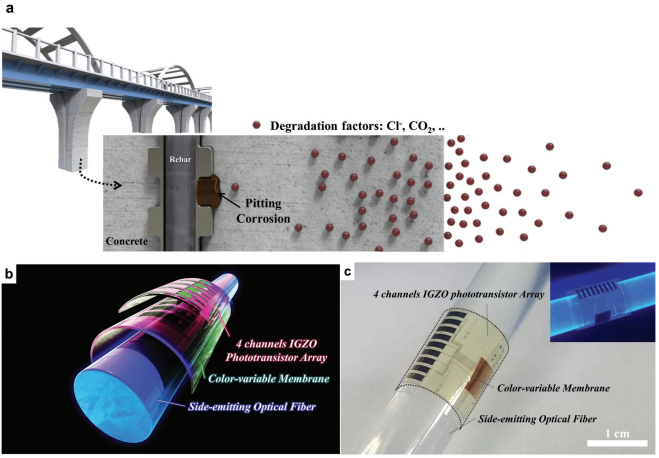
Healin Im, Hanseung Lee, Sunkook Kim. et al. A Colorimetric Multifunctional Sensing Method for Structural-Durability-Health Monitoring Systems. Advanced Materials. 2019
DOI: 10.1002/adma.201807552
https://doi.org/10.1002/adma.201807552
5. 浦侃裔Angew:有機(jī)光動(dòng)力納米抑制劑協(xié)同治療癌癥
光動(dòng)力療法(PDT)在癌癥治療中具有巨大的潛力,但它也會(huì)加劇腫瘤乏氧,進(jìn)而影響其治療的效果。南洋理工大學(xué)浦侃裔教授團(tuán)隊(duì)合成了一種有機(jī)光動(dòng)力納米抑制劑(OPNi),它具有中和碳酸酐酶IX (CA-IX)的能力,而碳酸酐酶IX是乏氧介導(dǎo)的信號(hào)級(jí)聯(lián)中的一個(gè)重要的分子靶點(diǎn)。OPNi是由作為光敏劑的半導(dǎo)體聚合物和CA-IX拮抗劑共軛的兩親性聚合物所組成。這種分子結(jié)構(gòu)使得OPNi不僅可以選擇性地結(jié)合CA-IX陽(yáng)性癌細(xì)胞,促進(jìn)其在腫瘤的積累,還可以對(duì)CA-IX的相關(guān)通路進(jìn)行調(diào)控。實(shí)驗(yàn)將CA-IX的抑制作用整合到靶向PDT過(guò)程中,證明其可以產(chǎn)生協(xié)同效應(yīng)并使得抗腫瘤效果優(yōu)于單純的PDT,同時(shí)也大大降低了乏氧誘導(dǎo)的腫瘤轉(zhuǎn)移的可能。
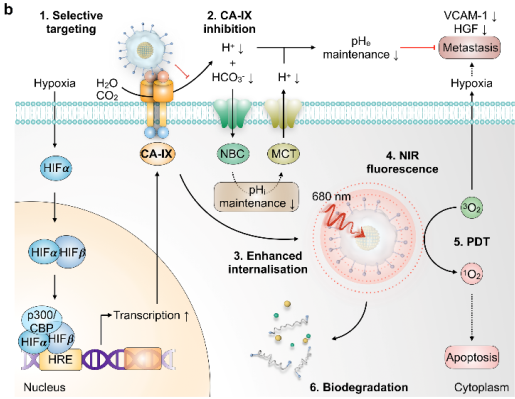
Yuyan Jiang, Kanyi Pu. et al. Organic Photodynamic Nanoinhibitor for Synergistic Cancer Therapy. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201903968
http://dx.doi.org/10.1002/anie.201903968
6. Angew:對(duì)光敏劑和前藥進(jìn)行精確集成以實(shí)現(xiàn)近紅外光激發(fā)的聯(lián)合治療
將光敏劑與對(duì)活性氧(ROS)敏感的前藥進(jìn)行協(xié)同遞送可以實(shí)現(xiàn)光觸發(fā)ROS的生成和級(jí)聯(lián)前藥。然而,目前還缺乏可行的方法來(lái)以精確的比例遞送這兩個(gè)組成部分,因此其應(yīng)用價(jià)值還有待挖掘。新加坡南洋理工大學(xué)趙彥利教授團(tuán)隊(duì)和中山大學(xué)梅林教授團(tuán)隊(duì)合作報(bào)告了主-客策略來(lái)構(gòu)建實(shí)現(xiàn)兩種成分比例最優(yōu)的納米遞送平臺(tái),并最大限度地提高聯(lián)合治療的效果。這一平臺(tái)的優(yōu)點(diǎn)在于:(1)光敏劑和對(duì)ROS敏感的前藥的比例可以很容易地被調(diào)整;(2)近紅外(NIR)光作為單一的外部刺激可以使光敏劑發(fā)揮作用并激活紫杉醇前藥的釋放;(3)其在腫瘤積累過(guò)程中可以利用近紅外光成像對(duì)其進(jìn)行跟蹤從而最大限度地提高光動(dòng)力和化療的療效。
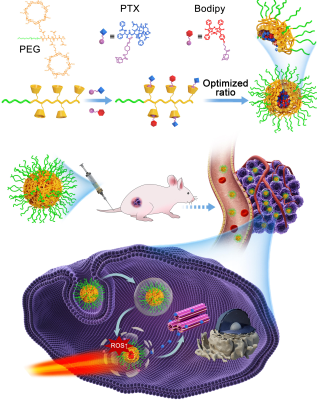
Hongzhong Chen, Lin Mei, Yanli Zhao. et al. NIR Light Activated Combination Therapy with Precisely Integrated Photosensitizer and Prodrug by a Host-Guest Strategy. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201900886
http://dx.doi.org/10.1002/anie.201900886
7. JACS:奧斯特瓦爾德熟化介導(dǎo)合成均勻可控的MXF
MXF是一種包含兩種以上組分的金屬有機(jī)骨架(MOF),如具有精確結(jié)構(gòu)的無(wú)機(jī)納米顆粒@MOF材料(NP@MOF),其在催化、能源和生物化學(xué)等領(lǐng)域具有重要的應(yīng)用價(jià)值。然而,人們對(duì)于MXF的生長(zhǎng)機(jī)制仍然不夠了解,這也大大阻礙了對(duì)納米級(jí)MXF配合物進(jìn)行可控設(shè)計(jì)的研究。湖南大學(xué)譚蔚泓教授團(tuán)隊(duì)報(bào)告了一種利用奧斯特瓦爾德熟化介導(dǎo)的將MOF通過(guò)異相成核嫁接到單個(gè)多齒狀無(wú)機(jī)膠體納米晶上以制備MXF的方法。該過(guò)程依賴于在膠體納米晶表面的羧酸基團(tuán)。實(shí)驗(yàn)結(jié)果證明利用這一方法可以獲得均勻的MXF,其中的NPs尺寸范圍很廣,并且MOF層的厚度也是可控的。研究由此制備了UCNP@ZrMOF并證明其可以實(shí)現(xiàn)近紅外光激發(fā)誘導(dǎo)的單態(tài)氧生成。這一工作提出的嫁接策略為MXF的可控設(shè)計(jì)提供了新的思路,為開(kāi)發(fā)先進(jìn)功能材料大有幫助。
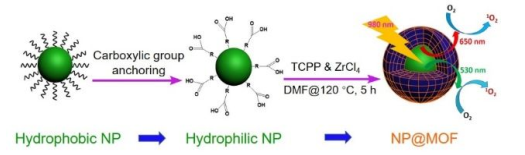
Yuan Liu, Weihong Tan. et al. Ostwald ripening-mediated grafting of metal-organic frameworks on a single colloidal nanocrystal to form uniform and controllable MXF. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.9b01563
https://pubs.acs.org.ccindex.cn/doi/10.1021/jacs.9b01563
8. AFM:二維MoSe2納米片用于光熱引發(fā)的癌癥免疫治療
在以納米藥物為基礎(chǔ)的癌癥治療中,納米材料在體內(nèi)循環(huán)過(guò)程中的非特異性吸收和快速清除是導(dǎo)致治療效率低下的主要原因。暨南大學(xué)陳填烽教授團(tuán)隊(duì)利用紅細(xì)胞(RBC)膜對(duì)具有高光熱轉(zhuǎn)換效率的二維MoSe2納米片進(jìn)行偽裝,可以阻止巨噬細(xì)胞對(duì)其吞噬從而達(dá)到增強(qiáng)其血液相容性和延長(zhǎng)循環(huán)時(shí)間的目的。RBC-MoSe2產(chǎn)生的光熱治療(PTT)在體內(nèi)具有非常好的抗腫瘤作用,可觸發(fā)腫瘤相關(guān)抗原的釋放去激活細(xì)胞毒性T淋巴細(xì)胞,同時(shí)也可以使得PD-1/PD-L1通路失活以避免免疫逃逸的發(fā)生。研究也發(fā)現(xiàn),PTT會(huì)使得腫瘤微環(huán)境中的腫瘤相關(guān)巨噬細(xì)胞被有效地重編程為M1表型,進(jìn)一步增強(qiáng)了其抗腫瘤的作用。因此,這種仿生功能化納米平臺(tái)也為設(shè)計(jì)PTT觸發(fā)的免疫治療提供新的策略。
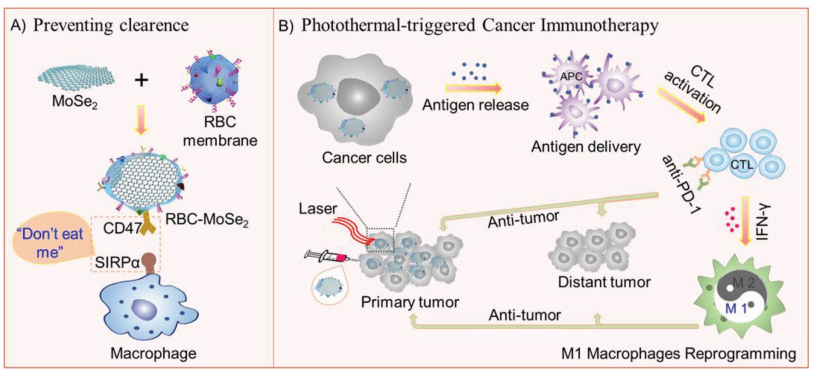
Lizhen He, Tianfeng Chen. et al. Designing Bioinspired 2D MoSe2 Nanosheet for Efficient Photothermal-Triggered Cancer Immunotherapy with Reprogramming Tumor-Associated Macrophages. Advanced Functional Materials. 2019
DOI: 10.1002/adfm.201901240
https://doi.org/10.1002/adfm.201901240
9. Adv. Sci.:富含鎂的三維培養(yǎng)系統(tǒng)可模擬骨發(fā)育微環(huán)境用于帶血管化骨再生
蠑螈胚基的斷肢再發(fā)育結(jié)果表明,通過(guò)模擬其發(fā)育微環(huán)境可以增強(qiáng)它的再生。鎂轉(zhuǎn)運(yùn)蛋白-1 (MagT1)是一種選擇性的鎂轉(zhuǎn)運(yùn)蛋白,在小鼠胚胎軟骨內(nèi)骨化區(qū)的表達(dá)會(huì)有顯著上調(diào)。上海交通大學(xué)蔣欣泉團(tuán)隊(duì)和張文杰團(tuán)隊(duì)合作設(shè)計(jì)了一種富含Mg的3D培養(yǎng)系統(tǒng)來(lái)為干細(xì)胞提供胚胎樣環(huán)境。實(shí)驗(yàn)首先評(píng)估了與干細(xì)胞成骨分化能力相對(duì)應(yīng)的MagT1表達(dá)水平,篩選出了適合構(gòu)建成骨微環(huán)境的最佳Mg2+的濃度。結(jié)果表明,Mg2+可以選擇性地激活絲裂原活化蛋白激酶/細(xì)胞外調(diào)節(jié)激酶(MAPK/ERK)通路來(lái)刺激成骨分化。隨后實(shí)驗(yàn)制備了具有適當(dāng)尺寸的富含Mg的微球以保證其中被包封細(xì)胞的生存。一系列實(shí)驗(yàn)結(jié)果表明,富含Mg的微環(huán)境不僅可以促進(jìn)干細(xì)胞的成骨分化,而且有助于新生血管的形成。而利用這些富含Mg的細(xì)胞載體則可以在體內(nèi)實(shí)現(xiàn)有效的帶血管化骨再生。
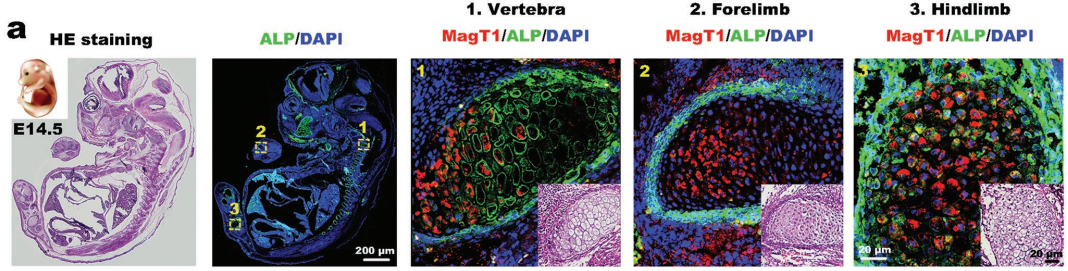
Sihan Lin, Wenjie Zhang, Xinquan Jiang. et al. A Magnesium-Enriched 3D Culture System that Mimics the Bone Development Microenvironment for Vascularized Bone Regeneration. Advanced Science. 2019
DOI: 10.1002/advs.201900209
https://doi.org/10.1002/advs.201900209
10. Angew:可生物降解的二氧化硅納米顆粒用于靶向線粒體進(jìn)行細(xì)胞內(nèi)蛋白遞送
線粒體是哺乳動(dòng)物細(xì)胞中的重要細(xì)胞器,其功能障礙也與多種疾病有關(guān)。因此,靶向線粒體蛋白的藥物為多種疾病的治療提供了一個(gè)非常有前途的策略。目前,靶向線粒體去遞送小分子藥物的方法是較為可行的,但并不適用于遞送蛋白質(zhì)、抗體等大分子。新加坡國(guó)立大學(xué)Shao Q. Yao團(tuán)隊(duì)和南京工業(yè)大學(xué)李林教授團(tuán)隊(duì)合作報(bào)告了一種利用可生物降解的二氧化硅納米顆粒(BS-NPs)進(jìn)行靶向線粒體地在細(xì)胞內(nèi)遞送天然蛋白和抗體的策略。這些載有蛋白的納米顆粒的表面由三苯基膦(TPP)和可穿透細(xì)胞的聚二硫化物(CPD)進(jìn)行修飾,因此能夠在不被內(nèi)溶酶體捕獲的情況下被細(xì)胞攝取并有效地靶向線粒體。隨后谷胱甘肽會(huì)引發(fā)其發(fā)生生物降解并釋放天然功能蛋白,從而參與后續(xù)的生物過(guò)程。
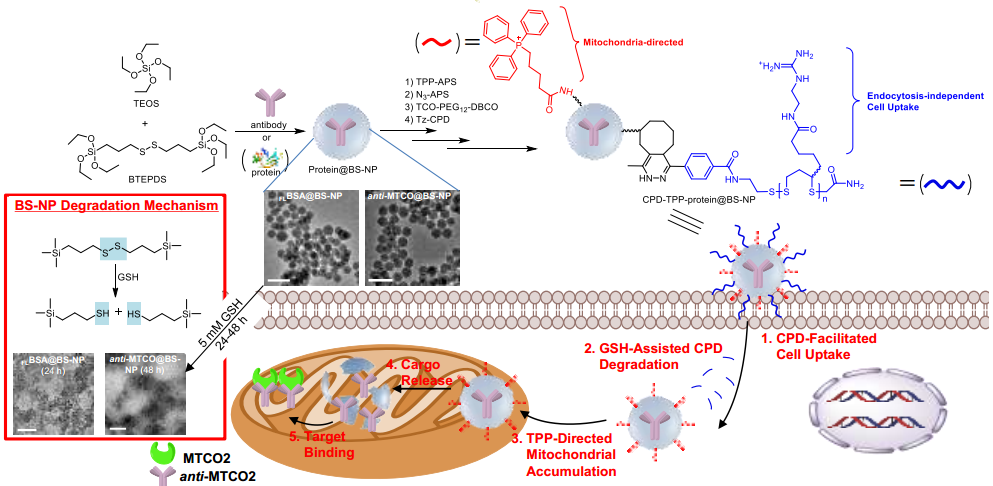
Peiyan Yuan, Lin Li, Shao Q. Yao. et al. Mitochondria-Targeting Intracellular Delivery of Native Proteins by Using Biodegradable Silica Nanoparticles.
Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201901699
http://dx.doi.org/10.1002/anie.201901699
11. 張凡Angew綜述:光學(xué)多路生物檢測(cè)技術(shù)改善生物醫(yī)學(xué)診斷
由于疾病的發(fā)展通常涉及多種化學(xué)物質(zhì)和生物分子,因此傳統(tǒng)地通過(guò)單次檢測(cè)來(lái)確定一種疾病的標(biāo)志物的分析方法通常是不夠準(zhǔn)確的。多靶點(diǎn)的同時(shí)分析在基礎(chǔ)生物醫(yī)學(xué)研究和臨床應(yīng)用中也發(fā)揮著越來(lái)越重要的作用。而要推動(dòng)多靶點(diǎn)同時(shí)分析的發(fā)展,就要開(kāi)發(fā)出高通量的多靶點(diǎn)生物分析技術(shù)。復(fù)旦大學(xué)張凡教授團(tuán)隊(duì)系統(tǒng)地綜述了近年來(lái)將光學(xué)多路復(fù)用分析技術(shù)應(yīng)用于生物醫(yī)學(xué)診斷領(lǐng)域的研究進(jìn)展;重點(diǎn)介紹了從多化學(xué)物質(zhì)的生物傳感和多色細(xì)胞示蹤技術(shù)發(fā)展到活體多路復(fù)用生物成像技術(shù)的發(fā)展歷程;最后也展望了生物多樣性分析所面臨的機(jī)遇和挑戰(zhàn)。
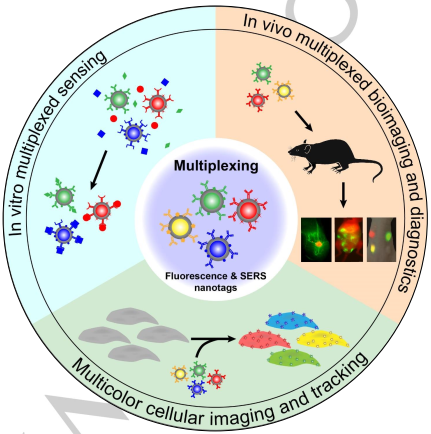
Yong Fan, Fan Zhang. et al. Optical multiplexed bioassays improve biomedical diagnostics. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201901964
http://dx.doi.org/10.1002/anie.201901964
12. CM:異質(zhì)結(jié)構(gòu)的共價(jià)有機(jī)納米片用于進(jìn)行對(duì)乏氧腫瘤的光動(dòng)力治療
光動(dòng)力治療(PDT)由于其依賴氧的特性,目前在治療乏氧腫瘤時(shí)效率較低。中科院長(zhǎng)春應(yīng)化所田華宇團(tuán)隊(duì)制備了具有供體-受體分子異質(zhì)結(jié)構(gòu)的共價(jià)有機(jī)納米片(CONs)。CON可通過(guò)I型PDT和I型PDT聯(lián)合光熱治療(PTT)兩種策略來(lái)治療乏氧腫瘤。首先,分子異質(zhì)結(jié)構(gòu)可以提供高效的電荷載體分離,從而獲得具有長(zhǎng)壽命的電子和空穴,電子可以將O2還原成O2?–同時(shí)空穴可以氧化水生成·OH,由此進(jìn)行I型PDT來(lái)克服于乏氧的限制。另外,上述由光激發(fā)產(chǎn)生物種會(huì)重新組合,由此產(chǎn)生了非輻射衰減并且散發(fā)熱量進(jìn)行PTT。實(shí)驗(yàn)結(jié)果證明,在單波長(zhǎng)照射下,經(jīng)靜脈注射CONS后可以利用I型PDT和PTT對(duì)裸鼠進(jìn)行有效的腫瘤治療。
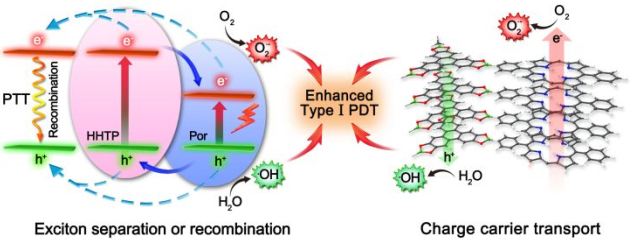
Kui Wang, Huayu Tian, Huayu Tian. et al. Covalent Organic Nanosheets Integrated Heterojunction with Two Strategies to Overcome Hypoxic-Tumor Photodynamic Therapy. Chemistry of Materials. 2019
DOI: 10.1021/acs.chemmater.9b00265
https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.chemmater.9b00265
13. 曲曉剛ACS Nano:MOF/酶納米結(jié)構(gòu)用于自激活的級(jí)聯(lián)反應(yīng)進(jìn)行體內(nèi)創(chuàng)傷愈合
基于金屬有機(jī)骨架(MOFs)的過(guò)氧化物模擬酶在生物醫(yī)學(xué)領(lǐng)域中的應(yīng)用較少,其中一個(gè)主要原因是它們的最佳反應(yīng)pH值為3-4的強(qiáng)酸環(huán)境中,這就嚴(yán)重限制了它們?cè)谥行詐H值的生命系統(tǒng)中的應(yīng)用。此外,若直接引入高濃度的H2O2也會(huì)對(duì)正常組織造成損傷。中科院長(zhǎng)春應(yīng)化所曲曉剛團(tuán)隊(duì)選用超薄的二維MOF (2D CuTCPP(Fe))納米片作為過(guò)氧化物酶并負(fù)載葡萄糖氧化酶(GOx)制備了這種混合型納米催化劑。其中,GOx會(huì)使得葡萄糖轉(zhuǎn)化為葡萄糖酸和H2O2,這樣可以避免直接使用高濃度的有毒H2O2所造成的副作用,而且生成的葡萄糖酸也可以將pH值從7降低到3-4,進(jìn)而激活二維Cu-TCPP(Fe)納米片的過(guò)氧化物模擬酶活性。生成的H2O2也能用于激活2D Cu-TCPP(Fe)納米片進(jìn)行后續(xù)的催化反應(yīng),高效地生成羥基自由基實(shí)現(xiàn)體內(nèi)抗菌。
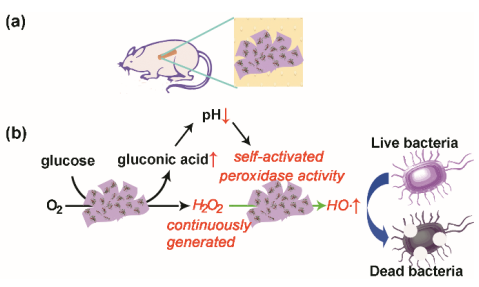
Xinping Liu, Xiaogang Qu. et al. 2D Metal-Organic Framework/Enzyme Hybrid Nanocatalyst as Benign and Self-Activated Cascade Reagent for in Vivo Wound Healing. ACS Nano. 2019
DOI: 10.1021/acsnano.8b09501
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsnano.8b09501
14. 鄭杰Angew:利用可由腎清除的金納米顆粒去改善抗癌藥物的體內(nèi)轉(zhuǎn)運(yùn)
利用納米粒子去精確地控制抗癌藥物在正常和癌變組織中的體內(nèi)轉(zhuǎn)運(yùn)是實(shí)現(xiàn)納米藥物臨床轉(zhuǎn)化的關(guān)鍵,這需要從根本上理解納米粒子是如何的抗癌藥物遞送過(guò)程中的“靶向-清除”和“滲透-保留”進(jìn)行影響的。德克薩斯大學(xué)達(dá)拉斯分校鄭杰教授團(tuán)隊(duì)以抗癌藥物阿霉素為模型,系統(tǒng)地研究了可由腎清除的金納米粒(AuNPs)對(duì)藥物在癌組織和正常組織中的滲透、分布和滯留的影響。實(shí)驗(yàn)結(jié)果表明,AuNPs既保持了游離藥物利用高腫瘤血管通透性去快速靶向腫瘤的優(yōu)勢(shì),而且也可以加速非靶向藥物的體內(nèi)清除。這一研究結(jié)果表明,利用納米粒子可以調(diào)和抗癌藥物在體內(nèi)遞送時(shí)存在的矛盾問(wèn)題。
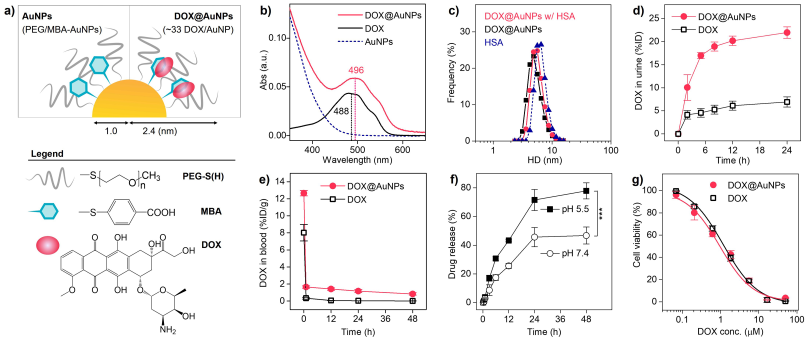
Chuanqi Peng, Jie Zheng. et al. Tuning in vivo transport of anticancer drugs with renal-clearable gold nanoparticles. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201903256
http://dx.doi.org/10.1002/anie.201903256
15. JACS:內(nèi)源性ROS觸發(fā)的形態(tài)改變可以增強(qiáng)其與線粒體的協(xié)同作用
國(guó)家納米科學(xué)中心喬增瑩、王浩團(tuán)隊(duì)報(bào)道了利用內(nèi)源性活性氧(ROS)去引發(fā)多肽類偶聯(lián)物(PPCs)發(fā)生形態(tài)改變,進(jìn)而可以與線粒體發(fā)揮協(xié)同作用實(shí)現(xiàn)更好的腫瘤治療效果。PPCs是由(1)與聚(乙二醇)共軛的多肽KLVFF(2)靶向線粒體的細(xì)胞毒性肽KLAK和(3)聚乙烯醇骨架等所組成的。因此PPCs納米顆粒可以進(jìn)入細(xì)胞并且靶向線粒體。由于大多數(shù)癌細(xì)胞的線粒體周圍的活性氧生成過(guò)多,PPCs中的硫代酮連接物會(huì)被裂解,導(dǎo)致納米顆粒轉(zhuǎn)化為纖維狀納米結(jié)構(gòu)。這種納米纖維會(huì)暴露KLAK進(jìn)而使得其與線粒體之間的多價(jià)協(xié)同作用增強(qiáng),在體內(nèi)產(chǎn)生對(duì)癌細(xì)胞具有選擇性的細(xì)胞毒性和顯著的腫瘤抑制作用。這一工作也是利用細(xì)胞內(nèi)的ROS觸發(fā)材料發(fā)生形態(tài)轉(zhuǎn)化的首例,表明這一策略可以通過(guò)增強(qiáng)與靶向位點(diǎn)的相互作用來(lái)為疾病的診斷和治療提供一個(gè)新的方法。
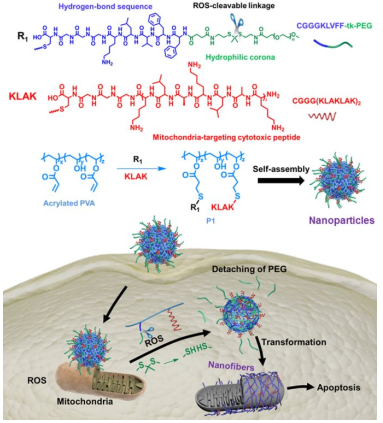
Dong-Bing Cheng, Zeng-Ying Qiao, Hao Wang. et al. Endogenous ROS-Triggered Morphology Transformation for Enhanced Cooperative Interaction with Mitochondria. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.8b07727
https://pubs.acs.org.ccindex.cn/doi/10.1021/jacs.8b07727
16. 張凡Angew:穩(wěn)定、波長(zhǎng)可調(diào)的近紅外II區(qū)熒光染料用于體內(nèi)生物成像和傳感
開(kāi)發(fā)在900-1700 nm波長(zhǎng)范圍內(nèi)有活性,具有可調(diào)諧的波長(zhǎng)和傳感性能的小分子有機(jī)熒光團(tuán)是目前生物體內(nèi)光學(xué)成像和生物傳感研究的熱點(diǎn)。復(fù)旦大學(xué)張凡教授團(tuán)隊(duì)開(kāi)發(fā)了一種新型熒光染料CX,其在生理環(huán)境中表現(xiàn)出良好的化學(xué)穩(wěn)定性和光穩(wěn)定性,并具有可調(diào)諧的光學(xué)性能,最大吸收/發(fā)射波長(zhǎng)為1089/1140 nm。實(shí)驗(yàn)結(jié)果證明CX可以被用于進(jìn)行高對(duì)比度的活體生物成像和多色檢測(cè),造成的光學(xué)串?dāng)_非常低。實(shí)驗(yàn)也研究了CX染料在深層組織中的福斯特共振能量轉(zhuǎn)移(FRET)過(guò)程,進(jìn)而證明它可以通過(guò)檢測(cè)OONO-來(lái)監(jiān)測(cè)藥物誘導(dǎo)產(chǎn)生的肝毒性。
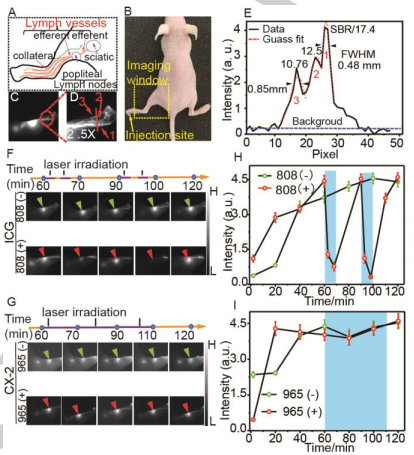
Zuhai Lei, Fan Zhang. et al. Stable, Wavelength-Tunable Fluorescent Dyes in the NIR-II Region for in-vivo High-Contrast Bioimaging and Multiplexed Biosensing. Angewandte Chemie International Edition. 2019
DOI: 10.1002/anie.201904182
http://dx.doi.org/10.1002/anie.201904182
17. ACS Nano:基于單壁碳納米管的實(shí)時(shí)熒光成像可改善卵巢癌手術(shù)后的存活率
對(duì)晚期卵巢癌(OC)的細(xì)胞減少手術(shù)進(jìn)行改善是該疾病治療所面臨的一個(gè)重要難題。而基于靶向的分子熒光成像則可以在顯微鏡下幫助實(shí)現(xiàn)完整的腫瘤切除。哈佛醫(yī)學(xué)院Lorenzo Ceppi團(tuán)隊(duì)和麻省理工學(xué)院Neelkanth M. Bardhan團(tuán)隊(duì)合作,利用反射/熒光成像系統(tǒng)和原位OC小鼠模型來(lái)對(duì)腫瘤的檢測(cè)進(jìn)行量化,并評(píng)估了熒光成像引導(dǎo)的手術(shù)對(duì)術(shù)后生存率的影響。實(shí)驗(yàn)使用的造影劑是一種可腹腔注射的納米分子探針,由單壁碳納米管與M13噬菌體偶聯(lián)組成,該噬菌體具有可與在OC中過(guò)表達(dá)的細(xì)胞外蛋白SPARC結(jié)合的修飾肽。結(jié)果表明,該成像系統(tǒng)能夠檢測(cè)到近紅外II區(qū)熒光(1000 - 1700 nm)并可實(shí)時(shí)顯示視頻圖像來(lái)指導(dǎo)手術(shù)的去瘤過(guò)程。原位OC小鼠模型的實(shí)驗(yàn)結(jié)果也證明,與常規(guī)手術(shù)相比,這種熒光成像指導(dǎo)的手術(shù)切除腫瘤會(huì)改善動(dòng)物的術(shù)后存活率。
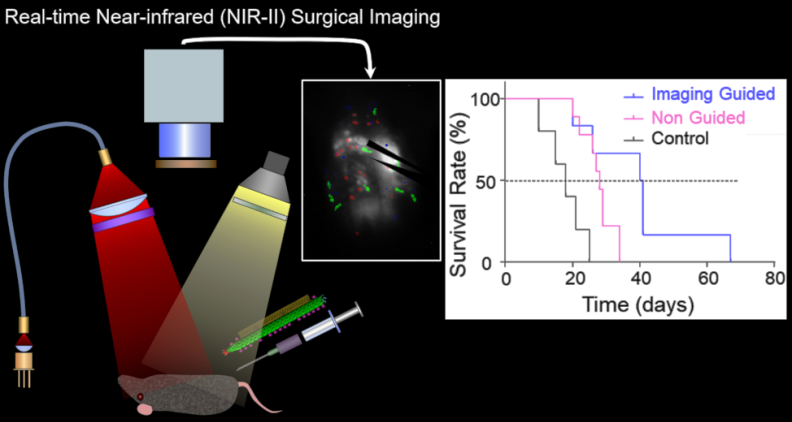
Lorenzo Ceppi, Neelkanth M. Bardhan. et al. Real-Time Single-Walled Carbon Nanotube-Based Fluorescence Imaging Improves Survival After Debulking Surgery In An Ovarian Cancer Model. ACS Nano. 2019
DOI: 10.1021/acsnano.8b09829
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsnano.8b09829
18. 北師大CM:利用光捕獲策略獲得的具有窄發(fā)射帶的AIE材料
聚集誘導(dǎo)發(fā)光材料(AIEgens)克服了傳統(tǒng)有機(jī)熒光團(tuán)的聚集猝滅(ACQ)現(xiàn)象,近年來(lái)受到越來(lái)越多的關(guān)注。盡管有機(jī)AIEgens具有顯著的優(yōu)點(diǎn)和巨大的發(fā)展科技,但大多數(shù)的AIEgens都有較寬的發(fā)射光譜,半峰全寬值(FWHM)超過(guò)100 nm,這很不利于它們的實(shí)際應(yīng)用。北京師范大學(xué)牛麗亞團(tuán)隊(duì)和楊清正團(tuán)隊(duì)合作,利用光捕獲技術(shù)設(shè)計(jì)了一種熒光強(qiáng)度更高、發(fā)射帶更窄的超分子聚合物AIE材料。這種AIE材料是一種由四氫鍵單體四苯乙烯(TPE)和硼-二吡咯亞甲基(BODIPY)組成的超分子聚合物。其中,TPE分子收集到的激發(fā)能量可以被有效地轉(zhuǎn)移到BODIPY中,其熒光強(qiáng)度提高了6倍并使得發(fā)射帶變窄,F(xiàn)WHM從148 nm減小到32 nm。研究結(jié)果表明,這種AIE材料可以成功地被應(yīng)用于體內(nèi)外的熒光和化學(xué)發(fā)光成像,并顯示出優(yōu)于傳統(tǒng)AIE材料的成像性能。
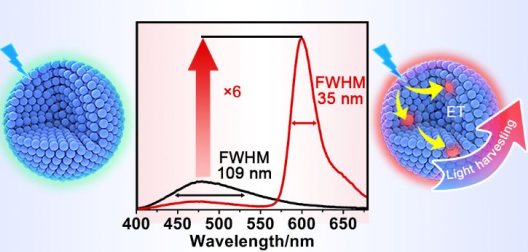
Xin Zhu, Li-Ya Niu, Qing-Zheng Yang. et al. AIE Materials with Narrowed Emission Band by Light-Harvesting Strategy: Fluorescence and Chemiluminescence Imaging. Chemistry of Materials. 2019
DOI: 10.1021/acs.chemmater.9b01338
https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.chemmater.9b01338
19. JACS:計(jì)算機(jī)指導(dǎo)的設(shè)計(jì)對(duì)pH響應(yīng)的有機(jī)光催化劑及其在雙控聚合的應(yīng)用
悉尼新南威爾士大學(xué)徐江濤團(tuán)隊(duì)、Cyrille Boyer團(tuán)隊(duì)和山東大學(xué)劉文劍團(tuán)隊(duì)合作,利用全計(jì)算機(jī)指導(dǎo)的策略發(fā)現(xiàn)了一種可切換的高效有機(jī)光催化劑(OPC),該催化劑在pH值為5時(shí)為無(wú)色,而在pH值為7時(shí)則恢復(fù)了較強(qiáng)的可見(jiàn)光吸收和光活性。這也是首次完全利用密度泛函理論(DFT)去設(shè)計(jì)OPC的例子。實(shí)驗(yàn)通過(guò)對(duì)設(shè)計(jì)的OPC進(jìn)行綜合表征,證實(shí)了計(jì)算預(yù)測(cè)的準(zhǔn)確性。隨后研究發(fā)現(xiàn)OPC在綠色LED下會(huì)在水相發(fā)生光誘導(dǎo)電子/能量轉(zhuǎn)移可逆加成-斷裂鏈轉(zhuǎn)移(PET-RAFT)聚合,并證明了pH值的輕微變化以及光的消失可以使得聚合停止。此外,研究也發(fā)現(xiàn)在可見(jiàn)光下,通過(guò)將二氧化碳鼓泡到反應(yīng)溶液中可以顯著降低其聚合速率,而如將其暴露在氮?dú)庵袆t可以完全恢復(fù)其聚合的速率。
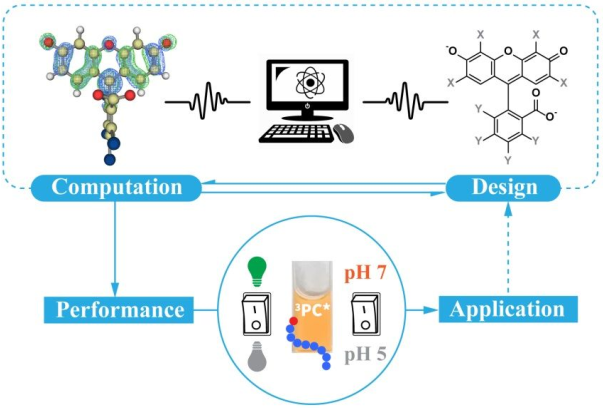
Chenyu Wu, Wenjian Liu, Jiangtao Xu, Cyrille Boyer. et al. Computer-Guided Discovery of a pH-Responsive Organic Photocatalyst and Application for pH and Light Dual-Gated Polymerization. Journal of the American Chemical Society. 2019
DOI: 10.1021/jacs.9b01096
https://pubs.acs.org.ccindex.cn/doi/pdf/10.1021/jacs.9b01096
20. ACS Nano:相互關(guān)聯(lián)的單細(xì)胞分析揭示納米材料放射增敏的生物學(xué)機(jī)制
納米粒子具有的放射增敏性能在提高放射治療效果、提高治愈率和降低腫瘤發(fā)病率等方面具有重要作用。但是人們目前由于其中的相關(guān)機(jī)制的認(rèn)識(shí)還很不足。南澳大利亞大學(xué)Ivan M. Kempson團(tuán)隊(duì)研究發(fā)現(xiàn)金納米粒子的存在會(huì)導(dǎo)致胸腺苷酸合成酶的下調(diào),而這對(duì)與耐輻射的S期細(xì)胞的DNA損傷修復(fù)過(guò)程來(lái)說(shuō)非常重要。實(shí)驗(yàn)通過(guò)開(kāi)發(fā)一種交叉相關(guān)的方法來(lái)研究細(xì)胞亞群對(duì)金納米顆粒的攝取概率以及與之相關(guān)的增敏作用。實(shí)驗(yàn)發(fā)現(xiàn),少數(shù)量的納米顆粒會(huì)產(chǎn)生脫敏的作用,而增敏作用會(huì)優(yōu)先影響S期細(xì)胞,并且同源重組是DNA損傷反應(yīng)的主要形式。這種小卻耐輻射的S期細(xì)胞群與其更強(qiáng)的增殖能力有關(guān)。這一工作表明放射增敏造成DNA損傷的增強(qiáng)不一定是由于DNA雙鏈斷裂(DSBs)數(shù)量的增加造成的,而是由于納米顆粒通過(guò)下調(diào)胸腺苷酸合成酶等修復(fù)蛋白所導(dǎo)致的損傷反應(yīng)。
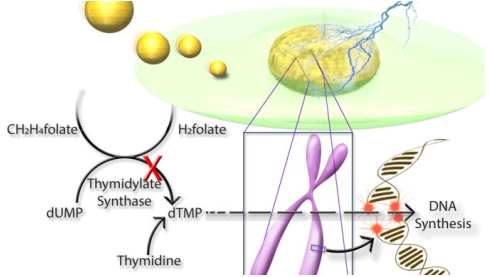
Tyron Turnbull, Ivan M. Kempson. et al. Cross-Correlative Single-Cell Analysis Reveals Biological Mechanisms of Nanoparticle Radiosensitization. ACS Nano. 2019
DOI: 10.1021/acsnano.8b07982
https://pubs.acs.org.ccindex.cn/doi/10.1021/acsnano.8b07982
21. CM:對(duì)光響應(yīng)的前藥超分子納米系統(tǒng)用于癌癥的聯(lián)合治療
光照引發(fā)的化療前藥隨需釋放已成為癌癥治療的研究熱點(diǎn)。南洋理工大學(xué)趙彥利團(tuán)隊(duì)和重慶大學(xué)羅忠團(tuán)隊(duì)合作設(shè)計(jì)了一種基于前藥的超分子納米顆粒(HA-aPS-aCPT),它是由(1)β-環(huán)糊精共軛的聚合物透明質(zhì)酸(HA-CD),(2)被ROS響應(yīng)的縮硫酮籠化的金剛烷改性的喜樹(shù)堿前藥(aCPT)籠和(3)金剛烷改性的光敏劑(aPS)組成,可用于進(jìn)行光動(dòng)力治療和光控化療。實(shí)驗(yàn)發(fā)現(xiàn),aCPT可通過(guò)裂解對(duì)ROS敏感的縮硫酮來(lái)釋放喜樹(shù)堿,而ROS是由aPS在光照射下產(chǎn)生的。HA-aPS-aCPT納米粒子在水溶液中具有良好的膠體穩(wěn)定性和單分散性。共聚焦和流式結(jié)果證實(shí)MDA-MB-231細(xì)胞可以對(duì)HA-aPS-aCPT進(jìn)行選擇性攝取,該過(guò)程是由于透明質(zhì)酸的靶向性和CD44受體介導(dǎo)的內(nèi)吞作用完成的。細(xì)胞存活實(shí)驗(yàn)表明,HA-aPS-aCPT納米粒子在黑暗中具有很小的細(xì)胞毒性,而在光照下具有較高的細(xì)胞毒性。體內(nèi)實(shí)驗(yàn)則表明HA-aPS-aCPT納米粒子可以在MDA-MB-231裸鼠腫瘤中有效地積累,而靜脈注射HA-aPS-aCPT納米顆粒并光照射后腫瘤則會(huì)明顯消退。

Soo Zeng Fiona Phua, Chencheng Xue, Zhong Luo, Yanli Zhao. et al. Light-Responsive Prodrug-Based Supramolecular Nanosystems for Site-Specific Combination Therapy of Cancer. Chemistry of Materials. 2019
DOI: 10.1021/acs.chemmater.9b00439
https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.chemmater.9b00439











