通過誘導細胞焦亡或激活cGAS-STING通路促進固有免疫是對抗免疫抑制性腫瘤微環境和誘導全身抗腫瘤免疫的有效方法。然而,目前的焦亡誘導藥物和STING激動劑往往存在不穩定性、潛在的副作用以及gasdermin和STING的細胞內表達不足等局限性。有鑒于此,中國科學院化學所肖海華研究員、中南大學劉昭前教授和毛小元教授構建了一個結合光動力治療(PDT)和表觀遺傳療法的腫瘤特異性納米診療平臺,其能夠通過光控方式同時激活細胞焦亡和cGAS-STING通路。
本文要點:
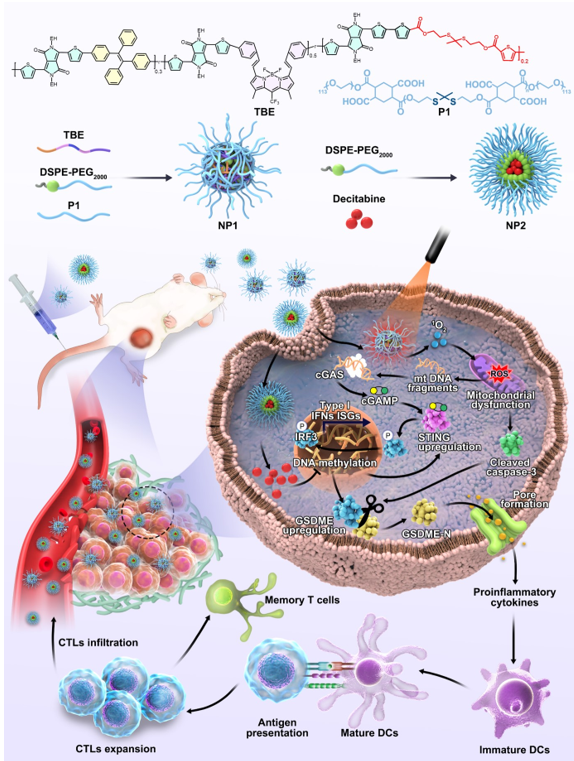
(1)實驗開發了負載光敏劑TBE的氧化敏感型納米顆粒(NP1)以及負載地西他濱(DNA甲基化酶抑制劑)的脂質體(NP2)。NP2能夠使STING和GSDME的表達恢復,而NP1介導的PDT則可促進損傷線粒體的DNA片段釋放,增強cGAS-STING通路,并促進caspase-3的活化,進而將上調的GSDME切割成為成孔的GSDME-N末端。
(2)隨后,釋放的炎性細胞因子會促進抗原提呈細胞的成熟,并觸發T細胞介導的抗腫瘤免疫。綜上所述,該研究設計了一種可同時光激活焦亡和cGAS-STING通路的新策略,可實現對免疫耐受腫瘤的靶向光-免疫治療。這一創新方法在克服現有治療策略的局限性方面具有重要的應用前景。
Feixiang Ding. et al. Simultaneous Activation of Pyroptosis and cGAS STING Pathway with Epigenetic/ Photodynamic Nanotheranostic for Enhanced Tumor Photoimmunotherapy. Advanced Materials. 2023
DOI: 10.1002/adma.202306419
https://onlinelibrary.wiley.com/doi/10.1002/adma.202306419




















