由于存在免疫抑制性腫瘤微環境(TME)和微弱的輻射吸收等問題,放射治療(RT)觸發的免疫反應會受到很大的限制。有鑒于此,南方醫科大學陳金香教授構建了一種具有核殼結構的納米增敏劑UiO@MnS(UM),其可通過整合MnS重編程的TME和基于Hf的UIO增敏的RT來增強放療效果和誘導免疫原性。
本文要點:
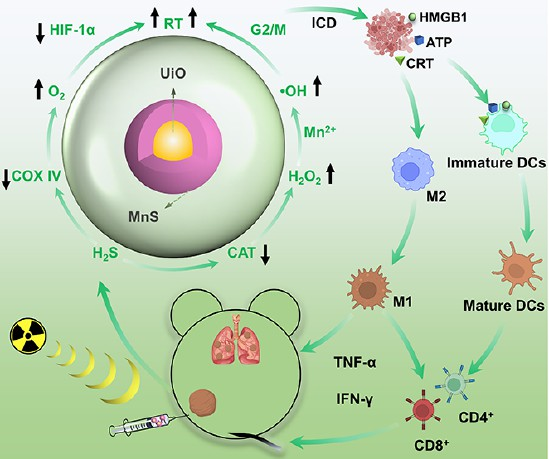
(1)對酸敏感的MnS會在酸性TME中會產生H2S,從而通過抑制線粒體呼吸和減少代謝氧消耗來改善氧合,導致HIF-1α表達降低,從而實現放射增敏。此外,H2S也可通過抑制過氧化氫酶活性提高H2O2水平,進而增強Mn2+介導的類芬頓反應,導致細胞周期G2/M期阻滯,以提高細胞對輻射的敏感性。
(2)實驗結果表明,增強的腫瘤氧合、細胞周期阻滯和放射增敏等過程不僅可以提高放療療效,也能夠產生強大的抗腫瘤免疫原性。綜上所述,該研究實現了免疫抑制性TME調節與放射增敏策略的充分結合,能夠顯著改善免疫原性放療的抗腫瘤效果。
Naihan Huang. et al. Immunogenic Radiation Therapy for Enhanced Antitumor Immunity via a Core?Shell Nanosensitizer-Mediated Immunosuppressive Tumor Microenvironment Modulation. ACS Nano. 2023
DOI: 10.1021/acsnano.3c04189
https://pubs.acs.org/doi/10.1021/acsnano.3c04189



















