開發協同治療策略以及預后監測膠質母細胞瘤對治療的免疫反應對于優化患者治療和改善臨床療效而言至關重要。然而,目前的替莫唑胺(TMZ)全身化療和用于體內免疫反應示蹤的影像學方法尚不完善。有鑒于此,廣東省人民醫院黃國家研究員和聶立銘教授開發了一種基于光聲-熒光成像的多合一納米診療探針(PEG/αCD25-Cy7/TMZ),并將其用于膠質瘤的精準化療和實時免疫反應示蹤。
本文要點:
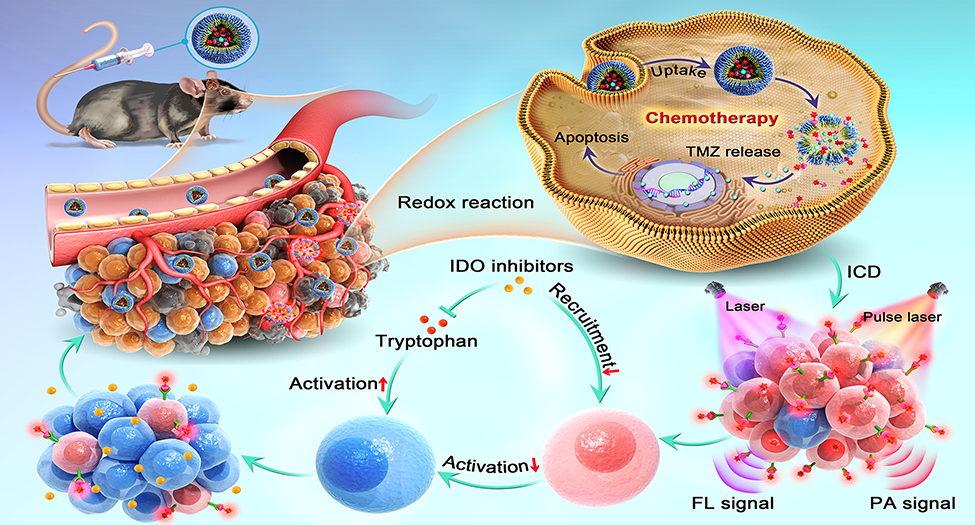
(1)該納米探針負載了TMZ和具有谷胱甘肽響應性的DSPE-SS-PEG2000包裹的靶向調節性T淋巴細胞的光學染料αCD25-Cy7。結果表明,該納米探針對調節性T淋巴細胞的靶向效率可達92.3%。谷胱甘肽激活的PEG/αCD25-Cy7/TMZ可將TMZ精確遞送至腫瘤微環境,以進行局部化療,并且能夠通過光聲-熒光成像實現對膠質母細胞瘤邊界的監測。研究發現,化療后應用吲哚胺2,3-雙加氧酶抑制劑進行免疫治療可顯著促進免疫應答,減少調節性T淋巴細胞浸潤,進而提高生存率。
(2)此外,基于該納米探針的光聲成像技術也能在微米尺度上實時、無創地對免疫反應的動態過程進行可視化,其結果也證明了化療后調節性T淋巴細胞的浸潤會發生增加,而IDO抑制劑治療后的調節性T淋巴細胞浸潤會減少。綜上所述,該研究設計的一體化診療策略能夠為精確遞送TMZ和通過長期動態示蹤調節性T淋巴細胞以評估原位免疫應答提供一種新的有效方法。
Fanchu Zeng. et al. Tumor Microenvironment Activated Photoacoustic-Fluorescence Bimodal Nanoprobe for Precise Chemoimmunotherapy and Immune Response Tracing of Glioblastoma. ACS Nano. 2023
DOI: 10.1021/acsnano.3c03378
https://pubs.acs.org/doi/10.1021/acsnano.3c03378



















