低溫光熱治療(PTT)是一種利用低溫光熱效應選擇性清除腫瘤細胞、同時保護正常組織、可最大限度地減少熱損傷和提高治療安全性的一種無創方法。研究人員在基因水平上評估了低溫光熱處理后腫瘤細胞的轉錄組,發現參與細胞周期和熱反應相關信號通路的基因會顯著富集。為了解決這一挑戰,重慶大學蔡開勇教授和杜克大學Ye He開發了一種工程化多功能納米平臺,從而為實現對低溫PTT的高效增敏提供了一種多合一的新策略。
本文要點:
(1)實驗使用MoS2納米粒子作為光熱核心來產生低溫光熱(40-48℃)。該納米平臺被DPA所包覆,以負載CPT-11和Fe2+,并進一步被PEG和iRGD修飾以增強其腫瘤特異性(MoS2/Fe@CPT-11-PEG-iRGD)。研究發現,激光和酸會觸發納米平臺釋放CPT-11,從而顯著增加細胞內的H2O2含量,進而協同Fe2+增加細胞內脂質ROS含量,激活鐵死亡。
(2)此外,CPT-11也會誘導細胞周期停滯在對溫度敏感的S期,并且增加的脂質ROS水平也有助于降解HSPs蛋白表達。這種協同作用可通過增敏的低溫PTT以及鐵死亡聯合的化療有效地誘導腫瘤細胞死亡。實驗結果表明,該納米平臺可以最大限度地清除腫瘤細胞,并顯著延長荷瘤小鼠的生存時間。綜上所述,該研究構建的多功能策略能夠為實現低溫PTT的臨床應用提供更多的可能性,并進一步推動多種腫瘤治療策略的發展。
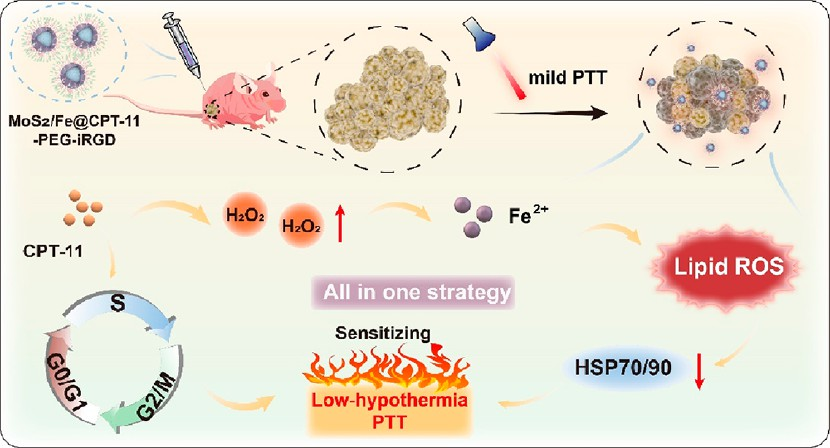
Ke Li. et al. All-in-One Engineering Multifunctional Nanoplatforms for Sensitizing Tumor Low-Temperature Photothermal Therapy In Vivo. ACS Nano. 2023
DOI: 10.1021/acsnano.3c05991
https://pubs.acs.org/doi/10.1021/acsnano.3c05991



















