代謝重編程是腫瘤的特征之一,其與腫瘤的發(fā)生、生長和轉移密切相關。調(diào)節(jié)腫瘤的代謝途徑已成為腫瘤治療的新途徑之一。然而,傳統(tǒng)的代謝介導的腫瘤細胞凋亡過程所產(chǎn)生的免疫原性和抗腫瘤免疫激活效率仍然較為有限。有鑒于此,中國科學院長春應化所林君研究員、馬平安研究員和丁彬彬博士成功制備了磷脂包被的檸檬酸鈉納米粒(PSCT NPs),該納米粒子可在腫瘤細胞中溶解并釋放出大量的檸檬酸離子和Na+離子。
本文要點:
(1)大量的離子會導致細胞內(nèi)滲透壓升高,從而激活caspase-1/gasdermin D(GSDMD)介導的細胞焦亡通路。與此同時,檸檬酸鹽也能夠誘導caspase-8/gasdermin C(GSDMC)通路的激活。
(2)實驗結果表明,這兩種通路的聯(lián)合作用能夠協(xié)同誘導強烈的細胞焦亡,從而表現(xiàn)出顯著的抗腫瘤免疫反應,有效抑制腫瘤的生長。綜上所述,該研究能夠為利用納米材料調(diào)節(jié)代謝和改變細胞死亡模式以增強抗腫瘤免疫治療提供新的借鑒和參考。
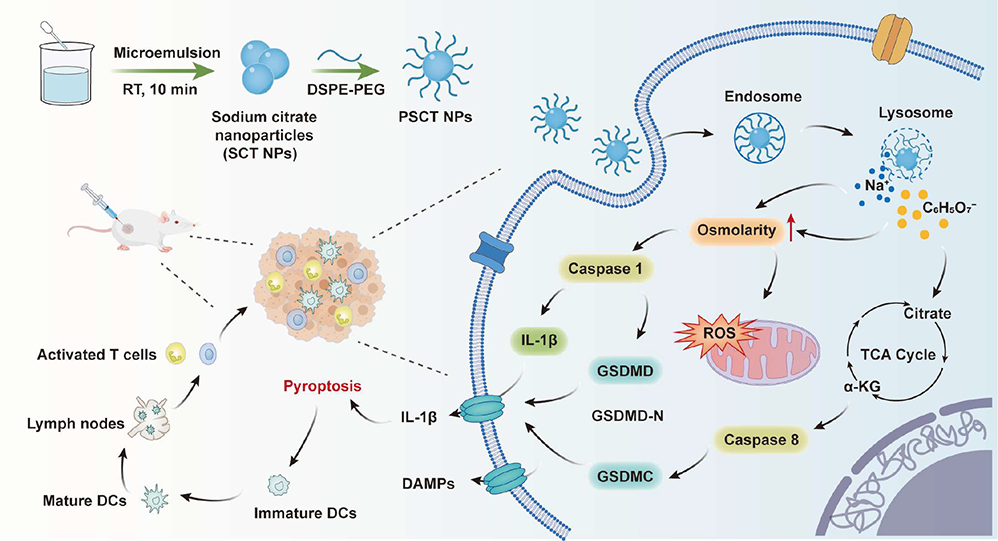
Jing Li. et al. Sodium Citrate Nanoparticles Induce Dual-Path Pyroptosis for Enhanced Antitumor Immunotherapy through Synergistic Ion Overload and Metabolic Disturbance. Nano Letters. 2023
DOI: 10.1021/acs.nanolett.3c03382
https://pubs.acs.org/doi/10.1021/acs.nanolett.3c03382



















