
影像引導的化學動力學治療被廣泛認為是個性化和精準癌癥治療的一種有前途的方式。將成像和化學動力學功能結合在一個系統中通常依賴于混合材料方法。然而,復合材料的異質性、不明確性和解離/崩解性質往往使其在生物環境中的作用過程變得復雜,從而使治療不精確和無效。
在此,復旦大學Qiaowei Li采用兩種具有不同功能的無機單元(活性氧生成和特征發射)的策略實現了兩種單晶金屬有機框架(MOF),展示了網狀化學在創建原子精度多功能材料方面的能力。
文章要點
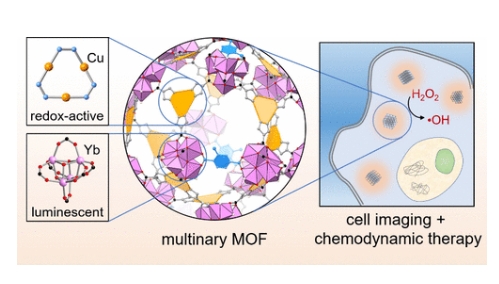
1)多元MOF不僅可以利用具有氧化還原活性的Cu基單元催化H2O2向羥基自由基的轉化,而且還可以通過支架中的Yb4簇發出特征性的組織穿透近紅外發光。
2)MOF 納米顆粒的雙重功能通過顯著的細胞成像信號、升高的細胞內活性氧水平、顯著的細胞凋亡以及被 HeLa 細胞攝取時細胞活力的降低進一步證明。 MOF 納米顆粒進一步功能化后,可實現體內近紅外成像。
3)完整MOF中獨立但互連的模塊可以在同一細胞位點同時運行,實現高度的時空一致性。總的來說,研究工作提出了一種新方法,可以在一種明確的材料中有效地容納成像和治療功能,以實現精確治療。
參考文獻
Lingyi Yang, et al, Target Design of Multinary Metal?Organic Frameworks for NearInfrared Imaging and Chemodynamic Therapy, J. Am. Chem. Soc., 2023
DOI: 10.1021/jacs.3c08611
https://doi.org/10.1021/jacs.3c08611



















