可激活的近紅外光學診療納米平臺(NP)具有靶向性強、可控性靈活、不良反應小和治療效果理想等優勢,被認為是一種高效可靠的腫瘤治療方法。有鑒于此,南華大學楊晴來教授、譚嘯峰教授和陳國棟教授構建了一種近紅外二區(NIR-II)熒光成像指導的有機光學診療NP(FTEP-TBFc NP)。
本文要點:
(1)分子工程化光學診療NP能夠靈敏地響應谷胱甘肽(GSH),以產生硫化氫(H2S)氣體,并在腫瘤微環境(TME)中遞送二茂鐵分子。在808 nm激光(0.33 W/cm2)的照射下,FTEP-TBFc不僅可以同時產生熒光、熱和單線態氧,而且可以顯著增強活性氧的產生,以改善化學動力學治療(CDT)和光動力治療(PDT)。研究發現,H2S可通過抑制過氧化氫酶和細胞色素c氧化酶(COX IV)的活性增強CDT和低溫光熱治療(HPTT)。
(2)此外,細胞內GSH濃度的降低也會進一步提高CDT的療效,并下調谷胱甘肽過氧化物酶4(GPX4),使脂質氫過氧化物發生積累,從而引起鐵死亡。綜上所述,該研究構建的多功能FTEP-TBFc納米粒子可以實現腫瘤成像指導的多模態腫瘤治療,能夠為可激活型光學診療平臺的設計和應用提供新的借鑒和參考。
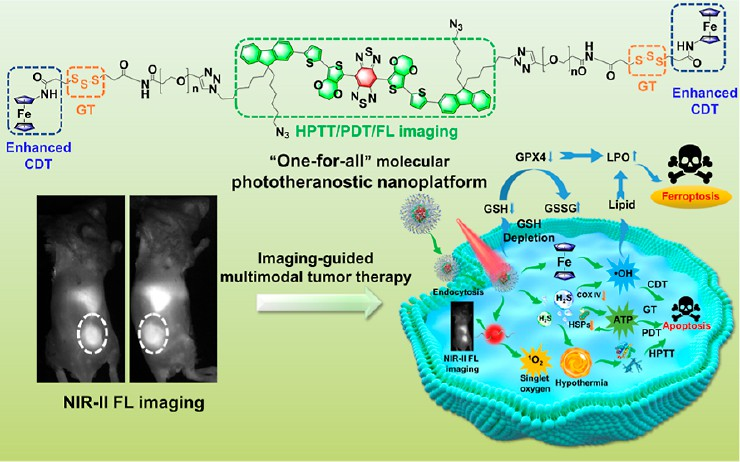
Gui-long Wu. et al. Tumor Microenvironment-Responsive One-for-All Molecular-Engineered Nanoplatform Enables NIR-II Fluorescence Imaging-Guided Combinational Cancer Therapy. Analytical Chemistry. 2023
DOI: 10.1021/acs.analchem.3c03827
https://pubs.acs.org/doi/10.1021/acs.analchem.3c03827



















