由可視化導(dǎo)航輔助、靶向病灶部位的可控藥物釋放對(duì)于實(shí)現(xiàn)腫瘤的精準(zhǔn)診療而言具有重要意義。由于聚集誘導(dǎo)發(fā)光(AIE)材料具有卓越的特性(聚集體的明亮發(fā)射和光學(xué)診療效應(yīng)),因此構(gòu)建基于AIE的多功能納米載體有望能夠通過(guò)多模態(tài)集成實(shí)現(xiàn)精準(zhǔn)診療。有鑒于此,香港中文大學(xué)(深圳)唐本忠院士、趙征教授和深圳大學(xué)熊玉教授開(kāi)發(fā)了一種具有同源靶向、可控藥物釋放和體內(nèi)雙模態(tài)成像和精準(zhǔn)化學(xué)-光熱協(xié)同治療等性能的智能納米平臺(tái)(P-TN-Dox@CM)。
本文要點(diǎn):
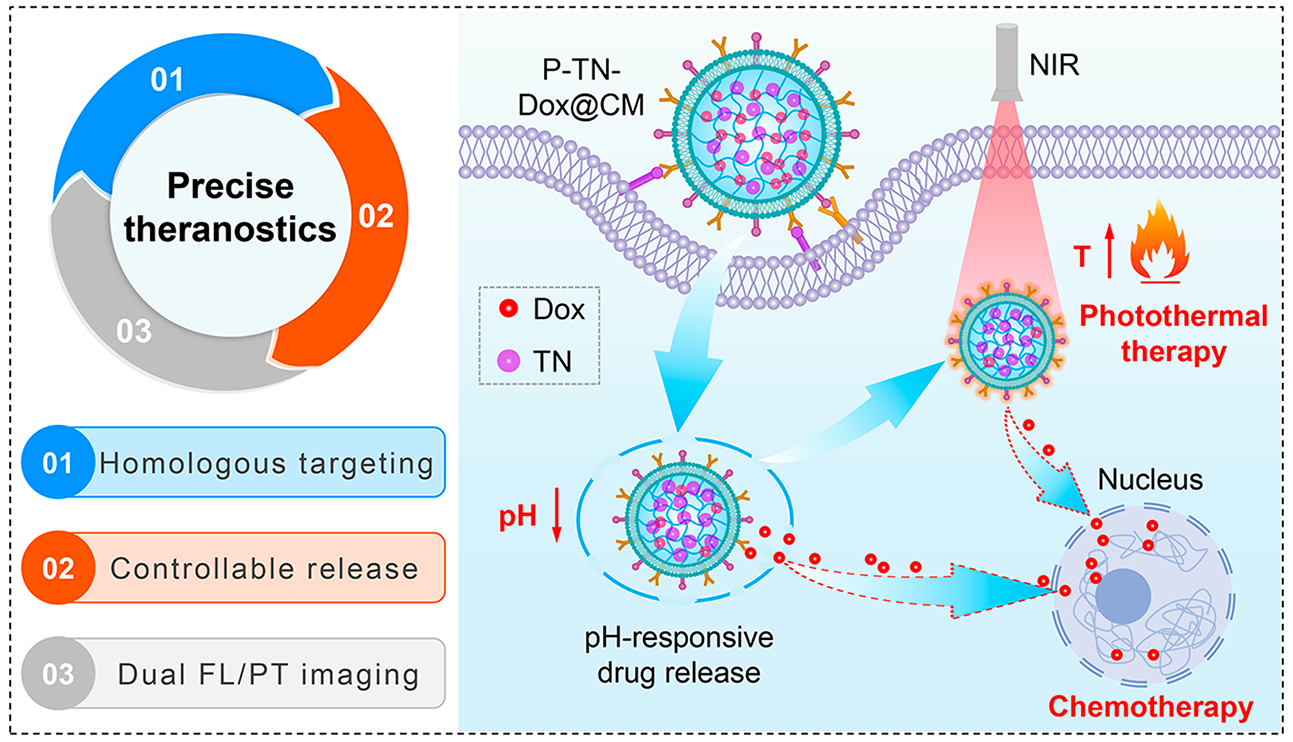
(1)實(shí)驗(yàn)將AIE光熱劑(TN)和抗癌藥物(Dox)包裹在對(duì)熱/pH響應(yīng)的納米凝膠(PNA)中,并將腫瘤細(xì)胞膜偽裝在納米凝膠表面,使其能夠通過(guò)同源效應(yīng)實(shí)現(xiàn)主動(dòng)靶向,有利于提高對(duì)腫瘤部位的特異性藥物遞送效率。被腫瘤細(xì)胞吞噬后,納米凝膠會(huì)在低pH條件下表現(xiàn)出爆發(fā)性藥物釋放的性能。此外,近紅外(NIR)光誘導(dǎo)的局部熱療能夠產(chǎn)生顯著的細(xì)胞毒性,并進(jìn)一步加速藥物的釋放,以實(shí)現(xiàn)協(xié)同增效的化學(xué)-光熱治療,徹底根除腫瘤。
(2)此外,該P(yáng)-TN-Dox@CM納米凝膠也可以實(shí)現(xiàn)近紅外熒光/光熱雙模態(tài)成像,以實(shí)時(shí)監(jiān)測(cè)藥物的動(dòng)態(tài)分布情況。綜上所述,該研究工作證明了智能型PTN-Dox@CM納米凝膠具有作為多功能納米平臺(tái)的巨大潛力,可通過(guò)多模態(tài)集成實(shí)現(xiàn)精準(zhǔn)的化學(xué)-光熱協(xié)同抗腫瘤治療。
Liping Zhang. et al. Multi-Stimuli-Responsive and Cell Membrane Camouflaged Aggregation-Induced Emission Nanogels for Precise Chemo-photothermal Synergistic Therapy of Tumors. ACS Nano. 2023
DOI: 10.1021/acsnano.3c08409
https://pubs.acs.org/doi/10.1021/acsnano.3c08409



















