基于免疫檢查點阻斷的免疫療法能夠顯著改善對癌癥的治療效果。CM-272是一種新型的G9a表觀遺傳抑制劑,可通過誘導免疫原性細胞死亡(ICD)恢復腫瘤對于anti-PD-1抗體的敏感性。然而,CM-272也會通過促進HIF-1α的轉錄活性以形成乏氧環境,進而極大地限制CM-272的療效。有鑒于此,哈爾濱醫科大學Yuanfei Yao和哈爾濱工程大學楊飄萍教授構建了基于Fe3+的納米級金屬有機框架(MIL-53),并將其用于負載CM-272(負載率高達56.4%),以制備MIL-53@CM-272納米平臺。
本文要點:
(1)進入膀胱癌細胞后,Fe3+不僅可以促進H2O2分解為O2以用于聲動力治療,而且能夠降低腫瘤微環境(TME)中高水平的谷胱甘肽,增強活性氧產生,誘導鐵死亡和細胞凋亡。研究發現,MIL-53載體會在TME中發生降解以加速CM-272的釋放,從而通過減弱耐藥性以在氧氣充足的TME中實現療效的最大化。
(2)研究者在使用RNA-seq研究膀胱癌細胞轉錄組中免疫相關通路的過程中發現,MIL-53@CM-272可以增強樹突狀細胞的成熟,并且能夠與抗程序性死亡蛋白1抗體相結合以發揮協同作用。綜上所述,該研究首次將納米藥物與CM-272進行結合,能夠實現誘導細胞凋亡、鐵死亡和ICD的"一箭三雕"的效果。
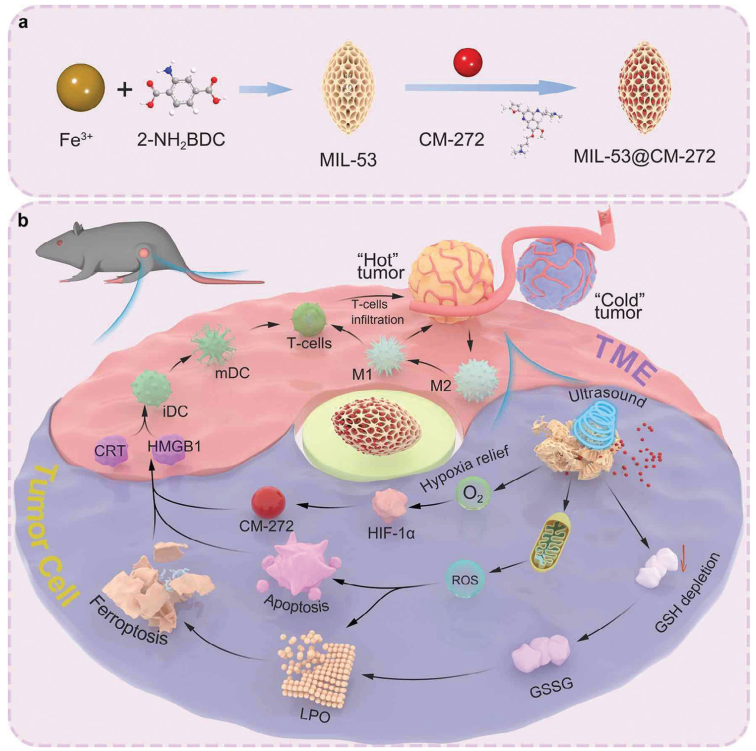
Ruiqi Liu. et al. A “One Arrow Three Eagle” Strategy to Improve CM-272 Primed Bladder Cancer Immunotherapy. Advanced Materials. 2023
DOI: 10.1002/adma.202310522
https://onlinelibrary.wiley.com/doi/10.1002/adma.202310522



















