肝細胞癌(HCC)術后常因復發(fā)和轉(zhuǎn)移而導致臨床療效不佳。因此,目前該領域的研究重點是建立有效的多模式治療模式。有鑒于此,鄭州大學韓新巍教授、任建莊教授、溫州醫(yī)科大學王周光教授和Ping Wu設計了一種由鍺磷(GeP)和安羅替尼(AL)組成的便攜式納米纖維補片,其能夠作為實現(xiàn)分子靶向的光熱-免疫檢查點阻斷(ICB)三模態(tài)聯(lián)合治療的多功能平臺。
本文要點:
(1)該補片具有親水性、良好的機械性能和優(yōu)良的光熱轉(zhuǎn)換性能,可以實現(xiàn)具有穿透性和持續(xù)性的藥物釋放。研究發(fā)現(xiàn),近紅外光輔助GeP誘導的溫度升高可以調(diào)節(jié)AL的釋放,下調(diào)血管相關因子受體的表達,觸發(fā)腫瘤細胞的免疫原性細胞死亡,并誘導樹突狀細胞成熟。
(2)與此同時,研究者也引入了ICB(程序性細胞死亡配體1,PD-L1)療法以提高治療效果。實驗結(jié)果表明,這種三模態(tài)聯(lián)合療法能夠顯著抑制血管的過度生長,增強效應T細胞浸潤,并增敏PD-L1抗體反應,從而改善免疫治療,有效抑制殘余HCC的復發(fā)和轉(zhuǎn)移。基因組測序結(jié)果也進一步驗證了與調(diào)節(jié)免疫效應相關的主要細胞通路。綜上所述,該研究開發(fā)了一種有效實用的納米纖維補片,其能夠改善對術后HCC的多模態(tài)治療效果,具有較高的臨床轉(zhuǎn)化價值。
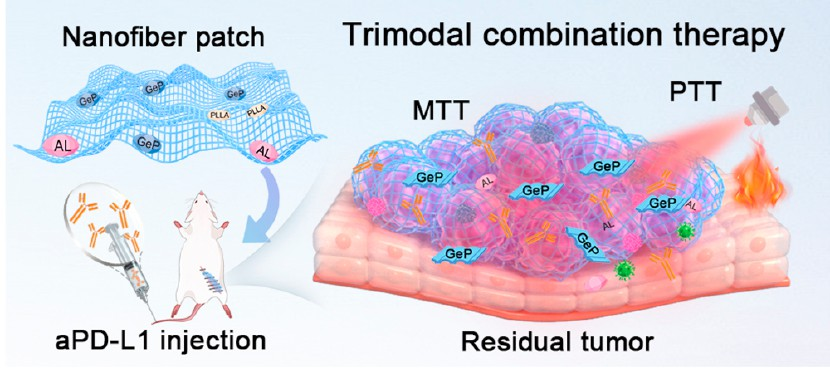
Yanan Zhao. et al. In Situ Nanofiber Patch Boosts Postoperative Hepatocellular Carcinoma Immune Activation by Trimodal Combination Therapy. ACS Nano. 2023
DOI: 10.1021/acsnano.3c05829
https://pubs.acs.org/doi/10.1021/acsnano.3c05829



















