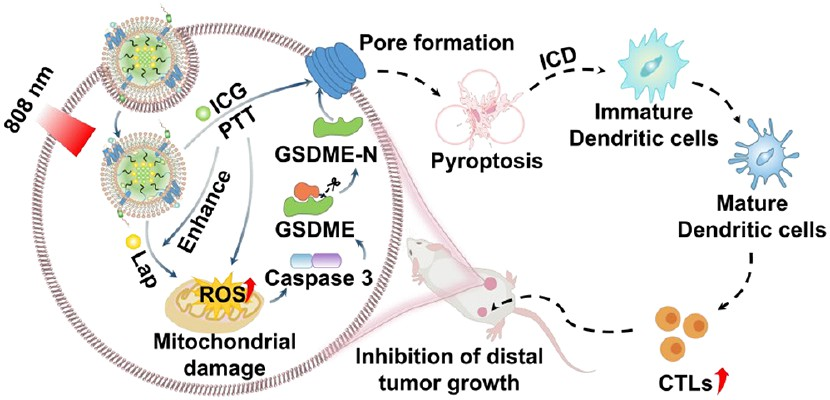
腫瘤微環境(TME)的異質性是導致腫瘤治療無效和腫瘤進展失控的主要原因。基于焦亡的免疫原性細胞死亡(ICD)治療是克服TME異質性以提高抗腫瘤效果的理想策略。然而,目前主要依賴于單一內源性或外源性刺激的焦亡治療方法的有效性仍會受到惡性細胞固有病理特征的限制。因此,開發一種具有高腫瘤特異性和可調性的協同策略是非常必要的。有鑒于此,安徽醫科大學何曉燕教授和贛南醫科大學Xiaoqing Yi通過將中性粒細胞偽裝殼和負載活性氧(ROS)供應體的自協同聚合物相結合,構建了一種具有協同功能的納米平臺。
本文要點:
(1)包覆的中性粒細胞膜使得該納米平臺具有“隱身”特性,并有利于其在腫瘤中實現有效的聚集。在激光照射下,光敏劑(吲哚菁綠)能夠觸發ROS的生成,并可將激光照射轉化為熱量,以上調NAD(P)H:醌氧化還原酶1。該酶可進一步催化β-拉帕酮以自產生充足的內源性ROS,實現增強的ICD。
(2)實驗結果表明,持續擴增產生的ROS不僅能夠消除原發腫瘤,同時也可以增強gasdermin E介導的細胞焦亡,啟動ICD級聯反應,“重新教育”異質性TME,促進全身免疫響應,以抑制遠端腫瘤的生長。綜上所述,該研究開發的自協同納米平臺能夠為調控免疫系統以實現對腫瘤的靶向抑制提供一種高效、持久的新方法。
Weiji Qin. et al. Advancing Precision: A Controllable SelfSynergistic Nanoplatform Initiating Pyroptosis-Based Immunogenic Cell Death Cascade for Targeted Tumor Therapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c09499
https://pubs.acs.org/doi/10.1021/acsnano.3c09499



















