cGAS-STING信號通路在放療介導的免疫調節過程中能夠發揮重要作用。然而,在安全的X射線劑量下,單純的放療往往不足以維持腫瘤中STING的激活。有鑒于此,陸軍軍醫大學田甘教授和卞修武院士設計了一種與cGAS刺激策略相協同的放療增敏方法,并開發了一種基于由氧化鉿(HfO2)內核和二氧化錳(MnO2)外殼組成的核-殼結構納米級放療增敏劑的cGAS-STING激動劑。
本文要點:
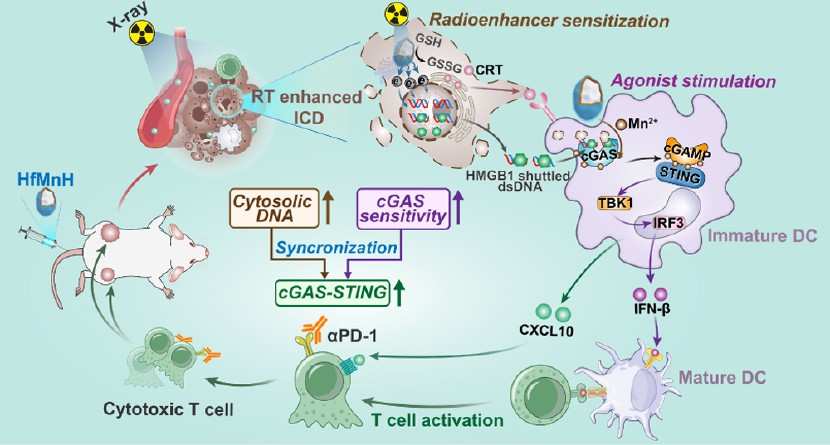
(1)HfO2介導的放療增敏可增強免疫原性細胞死亡,提供腫瘤相關抗原和足夠的胞質dsDNA。與此同時,能夠被GSH降解的MnO2可在腫瘤內持續釋放Mn2+,以提高cGAS的識別增敏作用。
(2)與免疫檢查點抑制劑聯合應用時,持續的Mn2+供應與累積的細胞質dsDNA損傷能夠協同增強輻照后腫瘤中的cGAS-STING激活,從而增強RT觸發的局部和系統效應。綜上所述,該研究證明了同步的放療增敏和持續性STING激活是一種能夠優化腫瘤放射免疫治療效果的有效策略。
Yuhua Cao. et al. An Immunocompetent Hafnium Oxide-Based STING Nanoagonist for Cancer Radioimmunotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c09293
https://pubs.acs.org/doi/10.1021/acsnano.3c09293



















