放射響應性遞送平臺的發展推動了新型的放射免疫聯合治療策略在腫瘤治療領域中的應用。然而,如何通過局部放療在體內控制免疫調節劑的釋放,以最大限度地減少脫靶毒性和輻射誘導的免疫抑制,并最大限度地提高放射免疫治療的協同效果仍然是一項嚴峻的挑戰。有鑒于此,蘇州大學汪勇教授和王楊云教授將內核交聯的聯硒化物納米顆粒(dSeNPs)作為載體,通過全身給藥實現對Toll樣受體7/8激動劑的放射響應性遞送,以用于對腫瘤的放射免疫聯合治療。
本文要點:
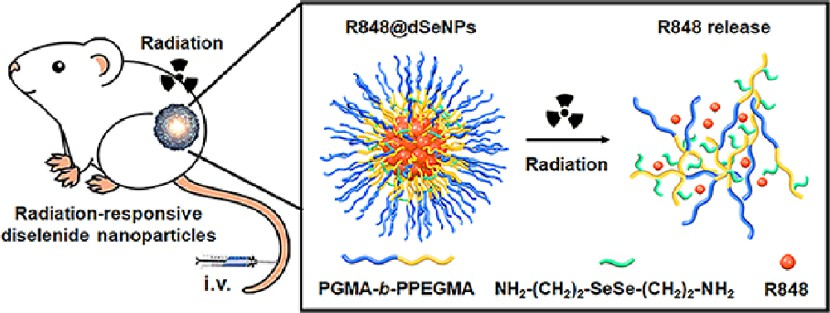
(1)實驗通過2,2'-二硒雙(乙胺)和兩親性嵌段共聚物的環氧乙烷基團之間的開環反應制備了dSeNPs。研究發現,自組裝納米結構的內核能夠保護二硒鍵,使得dSeNPs在生理環境中非常穩定。此外,dSeNPs也具有出劑量和時間依賴性的輻射敏感性,使得X射線可以在時間和空間上控制dSeNPs對R848的釋放。
(2)體內實驗結果表明,釋放的R848可通過程序化協同的免疫系統激活過程顯著提高放射免疫聯合治療的協同療效。該過程包括巨噬細胞極化、樹突狀細胞成熟和細胞毒性T細胞的活化等。綜上所述,該研究構建的內核交聯型dSeNPs能夠實現時空可控的輻射響應性藥物釋放,是一個具有重要潛力的聯合放療平臺。
Yanxian Wu. et al. Radioresponsive Delivery of Toll-like Receptor 7/8 Agonist for Tumor Radioimmunotherapy Enabled by Core-Cross-Linked Diselenide Nanoparticles. ACS Nano. 2024
DOI: 10.1021/acsnano.3c05882
https://pubs.acs.org/doi/10.1021/acsnano.3c05882



















