腫瘤細(xì)胞源性的腫瘤納米疫苗能夠?qū)⒛[瘤細(xì)胞來源的成分作為功能單位,使得該納米疫苗系統(tǒng)在提供所有潛在的腫瘤抗原方面具有顯著的優(yōu)勢(shì)。然而,現(xiàn)有腫瘤細(xì)胞衍生的腫瘤納米疫苗往往存在組裝步驟繁瑣、外源性佐劑的潛在風(fēng)險(xiǎn)、淋巴結(jié)靶向性和樹突狀細(xì)胞(DC)內(nèi)化不足等問題,從而極大地限制了它們的有效性和臨床轉(zhuǎn)化。有鑒于此,復(fù)旦大學(xué)陳鈞教授、黃建明教授和上海交通大學(xué)高小玲教授通過聚(D,L-丙交酯-co-乙交酯)納米粒子將內(nèi)質(zhì)網(wǎng)應(yīng)激誘導(dǎo)劑α-mangostin(αM)導(dǎo)入腫瘤細(xì)胞,并基于腫瘤細(xì)胞通過腫瘤源性外泌體(TEXs)胞吐納米粒子的生物學(xué)過程,構(gòu)建了生物自組裝的腫瘤細(xì)胞源性癌癥納米疫苗(αM-Exos)。
本文要點(diǎn):
(1)除了能夠提呈多種潛在抗原外,αM-Exos還遺傳了內(nèi)質(zhì)網(wǎng)應(yīng)激上調(diào)的70 kDa熱休克蛋白(hsp70),其不僅能夠作為內(nèi)源性佐劑,還可以改善LN靶向性和DC內(nèi)化。
(2)皮下注射后,αM-Exos可有效遷移至淋巴結(jié),并迅速被DC吞噬,進(jìn)而將腫瘤抗原和佐劑同步遞送至DC,以有效觸發(fā)抗腫瘤免疫反應(yīng),建立長期的免疫記憶。綜上所述,該研究構(gòu)建了一個(gè)多合一生物自組裝、腫瘤細(xì)胞衍生的腫瘤納米疫苗平臺(tái)。通過該平臺(tái)高效組裝的多功能腫瘤納米疫苗有望能夠?qū)崿F(xiàn)高效的腫瘤免疫治療。
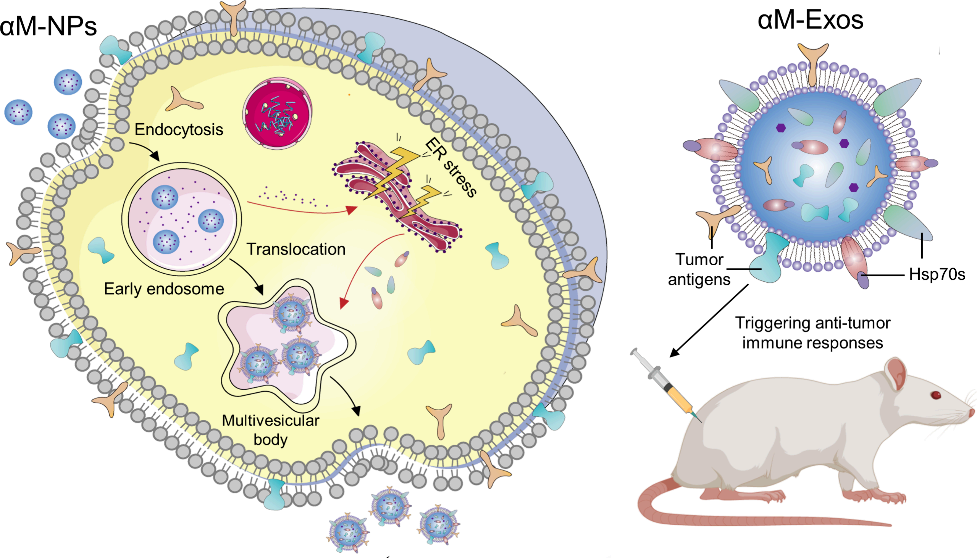
Kaifan Liang. et al. Biologically Self-Assembled Tumor Cell-Derived Cancer Nanovaccines as an All-in-One Platform for Cancer Immunotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.4c01050
https://pubs.acs.org/doi/10.1021/acsnano.4c01050



















