細胞內過量的Ca2+可誘導氧化應激、線粒體損傷和細胞凋亡,因此其在腫瘤治療領域中已被廣泛探索。然而,Ca2+基納米系統往往會導致較低的Ca2+蓄積,使其治療效果受到顯著的影響。有鑒于此,上海大學陳雨教授、Zeyu Wang、上海市第八人民醫院楊少玲教授和中國人民解放軍聯勤保障部隊第九八五醫院Tingting Zhang合理設計并構建了一種功能性植物多酚附加的酶動力納米酶系統CaFe2O4@BSA-curcumin(CFO-CUR),其可通過酶動力-Ca2+過載協同作用實現增強的Ca2+蓄積、活性氧(ROS)產生以及線粒體功能障礙。
本文要點:
(1)CaFe2O4納米酶在弱酸性的腫瘤微環境中釋放的外源性Ca2+和姜黃素抑制的Ca2+外排可增強由線粒體主導的抗腫瘤效應。研究發現,具有多種價態的鐵成分能夠通過類氧化酶、類過氧化物酶和類谷胱甘肽過氧化物酶等活性消耗內源性的谷胱甘肽,并產生大量的ROS。
(2)ROS爆發對Ca2+通道和Ca2+泵的調節能夠提高細胞內的Ca2+積累。與此同時,外源性的超聲刺激也能夠進一步增強線粒體損傷。體內外實驗結果表明,超聲增強的酶動力-鈣過載可實現協同的腫瘤抑制效果。綜上所述,該研究證明了超聲聯合功能性納米酶具有誘導線粒體穩態失衡和功能紊亂的作用,從而能夠為實現高效的腫瘤治療提供一個新的途徑。
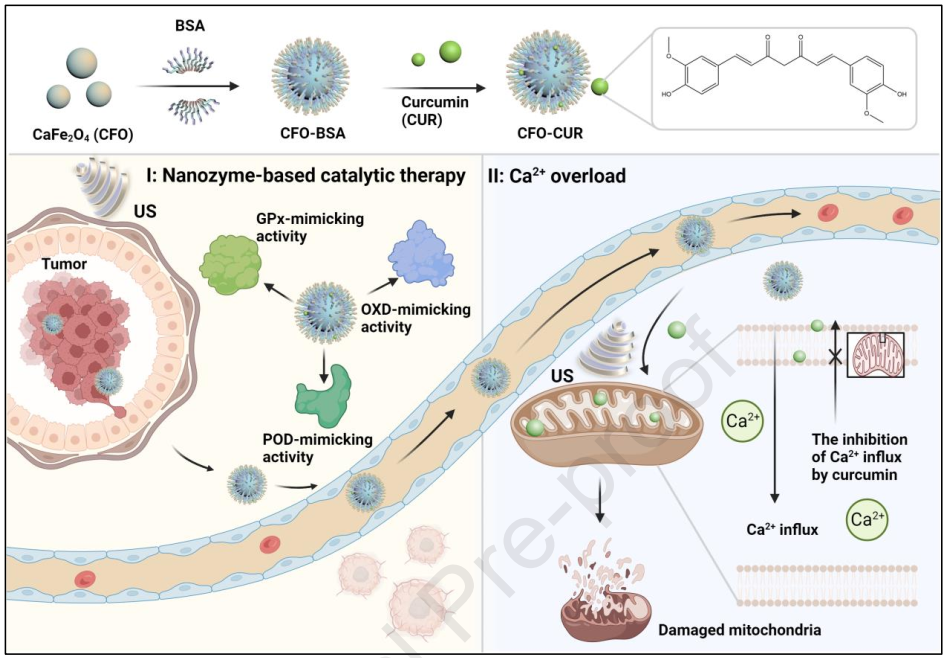
Meiqi Chang. et al. Ultrasound-augmented enzyodynamic-Ca2+ overload synergetic tumor nanotherapy. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224000474



















