利用納米藥物觸發(fā)溶酶體調(diào)節(jié)的免疫原性細(xì)胞死亡(ICD,如焦亡和壞死性凋亡)是一種實(shí)現(xiàn)腫瘤免疫“冷-熱”轉(zhuǎn)變的新方法。質(zhì)子海綿(如具有高分子量的支化型聚乙烯亞胺(PEI))能夠有效地破壞溶酶體,但其固定的電荷密度及其造成細(xì)胞死亡的機(jī)制不明確等問(wèn)題也會(huì)導(dǎo)致質(zhì)子海綿產(chǎn)生不可控制的毒性,使其治療應(yīng)用受到了嚴(yán)重的阻礙。有鑒于此,加州大學(xué)圣地亞哥分校Jesse V. Jokerst構(gòu)建了一系列具有自組裝可控表面電荷密度和細(xì)胞毒性的質(zhì)子海綿納米組裝體(PSNAs)。
本文要點(diǎn):
(1)實(shí)驗(yàn)通過(guò)將低分子量的支化型PEI與攜帶四苯基乙烯吡啶(PyTPE,一種聚集誘導(dǎo)發(fā)光分子)的自組裝肽進(jìn)行共價(jià)結(jié)合而構(gòu)建了PSNAs。研究發(fā)現(xiàn),自組裝肽-PyTPE輔助的PEI組裝可增強(qiáng)PSNAs的表面正電荷和細(xì)胞毒性。隨后,研究者通過(guò)調(diào)整多肽內(nèi)的親水和疏水成分進(jìn)一步優(yōu)化了PSNAs的自組裝趨勢(shì),從而構(gòu)建了具有最高的熒光、表面正電荷密度、細(xì)胞攝取和癌細(xì)胞細(xì)胞毒性的PSNAs。
(2)對(duì)細(xì)胞死亡機(jī)制的系統(tǒng)性研究表明,溶酶體破裂調(diào)控的細(xì)胞焦亡和壞死性凋亡是PSNAs導(dǎo)致細(xì)胞死亡的兩種主要原因。實(shí)驗(yàn)結(jié)果表明,腫瘤細(xì)胞在經(jīng)歷了PSNAs觸發(fā)的ICD后可激活免疫細(xì)胞,由此表明該研究構(gòu)建的PSNAs在觸發(fā)抗腫瘤免疫方面也具有巨大的應(yīng)用潛力。
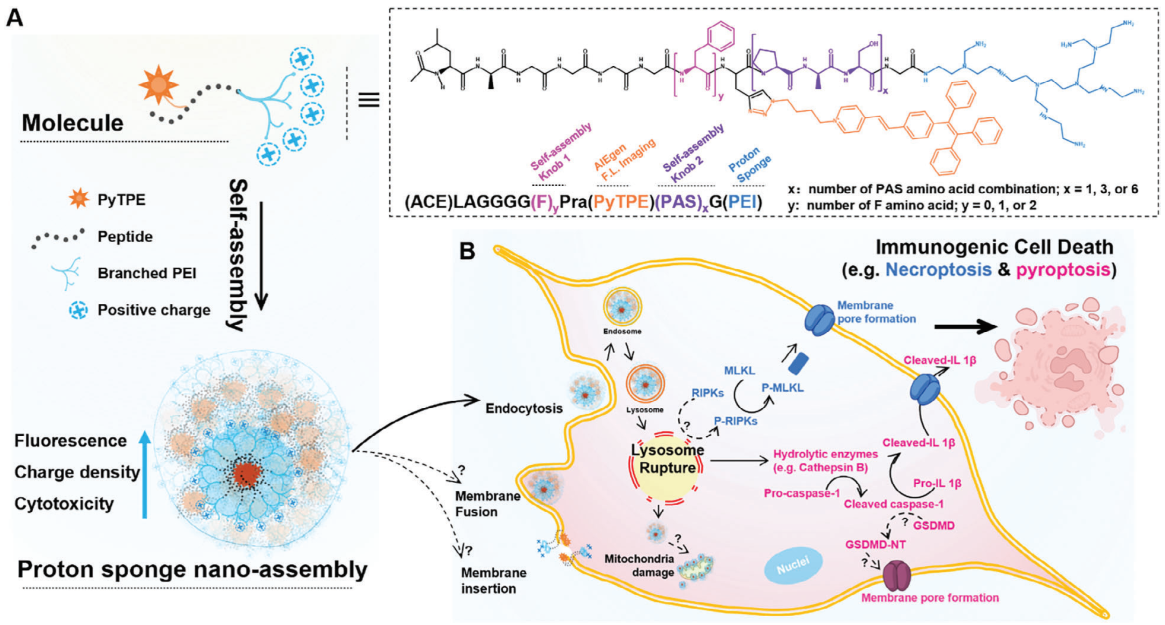
Tengyu He. et al. Peptide-Driven Proton Sponge Nano-Assembly for Imaging and Triggering Lysosome-Regulated Immunogenic Cancer Cell Death. Advanced Materials. 2024
DOI: 10.1002/adma.202307679
https://onlinelibrary.wiley.com/doi/10.1002/adma.202307679



















