個體腫瘤的復雜性和異質性會嚴重阻礙現有的治療性癌癥疫苗的效力。因此,研究者亟需開發更有效的原位癌癥疫苗。有鑒于此,南洋理工大學趙彥利教授、德克薩斯大學MD安德森癌癥中心Wen Jiang和中國科學院長春應化所林君研究員將FeAl層狀雙氫氧化物(LDH)作為載體,以二氫青蒿素(DHA)作為載荷,開發了一種用于實現活性氧增強的金屬免疫治療的癌癥納米疫苗。
本文要點:
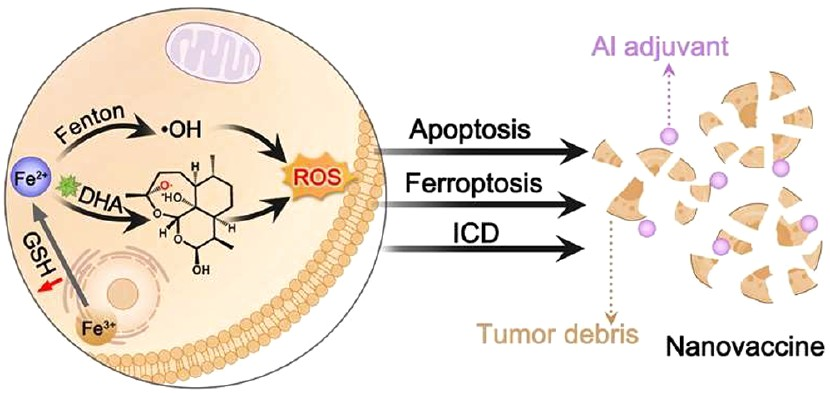
(1)LDH框架具有不穩定性,可在腫瘤微環境中降解,以釋放鐵離子、鋁離子和DHA。研究發現,鐵離子可通過協同的Fenton反應和DHA激活加重腫瘤內的氧化應激損傷,進而引起腫瘤細胞凋亡、鐵死亡和免疫原性細胞死亡。
(2)實驗結果表明,隨后釋放的腫瘤相關抗原可與Al佐劑形成癌癥納米疫苗,以產生顯著、長期的免疫應答,對抗癌癥的復發和轉移。此外,鐵離子激活的T1加權磁共振成像也有助于實現對腫瘤治療的實時監測。綜上所述,該研究設計的由癌癥納米疫苗介導的金屬免疫治療策略有望為實現精準免疫治療提供新的思路。
Mengyu Chang. et al. A Cancer Nanovaccine Based on an FeAlLayered Double Hydroxide Framework for Reactive Oxygen Species-Augmented Metalloimmunotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.3c11960
https://pubs.acs.org/doi/10.1021/acsnano.3c11960



















