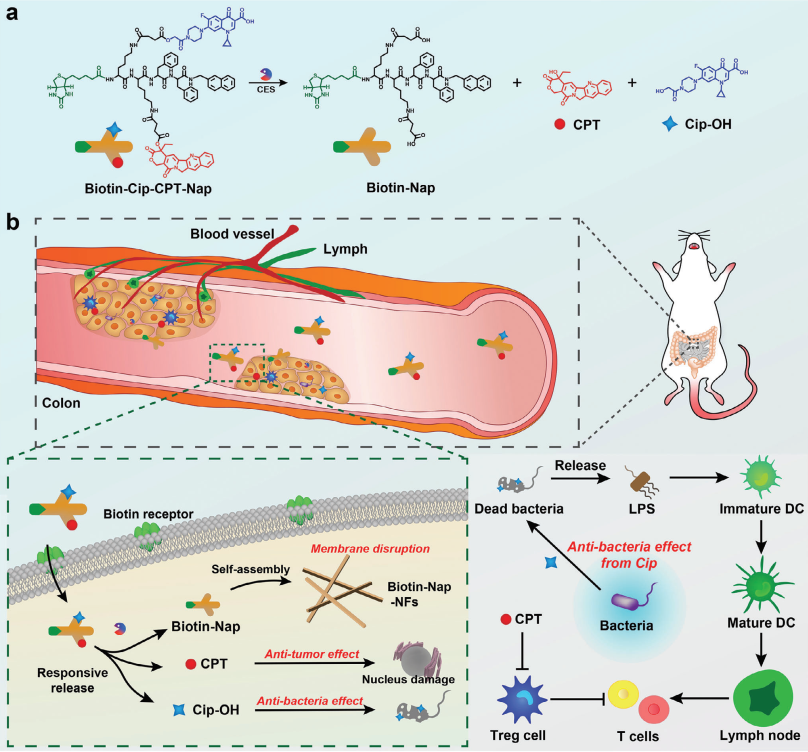
腫瘤內(nèi)細(xì)菌會導(dǎo)致結(jié)直腸癌對化療藥物產(chǎn)生耐藥性,并減弱免疫應(yīng)答。有鑒于此,徐州醫(yī)科大學(xué)王剛教授、鄭駿年教授和高歌教授設(shè)計了一種新型分子Biotin-Lys(SA-Cip-OH)-Lys(SACPT)-Phe-Phe-Nap(Biotin-Cip-CPT-Nap),其包含4個功能基序(用于靶向的生物素基序、用于實現(xiàn)自組裝的Phe-Phe(-Nap)基序、用于抗菌的環(huán)丙沙星衍生物(Cip-OH)基序和用于化療的喜樹堿(CPT)基序)。
本文要點:
(1)研究發(fā)現(xiàn),實驗設(shè)計的分子能夠?qū)崿F(xiàn)胞內(nèi)酶促納米纖維的形成和協(xié)同抗菌增強的化療及免疫治療。在結(jié)直腸癌細(xì)胞膜高表達(dá)的生物素受體介導(dǎo)的內(nèi)吞作用和在胞質(zhì)中高表達(dá)的羧酸酯酶的催化作用下,該新型分子可轉(zhuǎn)化為生物素-Nap,并自組裝成納米纖維。
(2)與此同時,抗生素Cip-OH和化療藥物CPT會被釋放,以克服細(xì)菌誘導(dǎo)的耐藥和提高結(jié)直腸癌免疫治療的療效。綜上所述,該研究能夠為設(shè)計新型多功能前藥以提高對結(jié)直腸癌的治療效率提供一種新的策略。
Ge Gao. et al. Three-in-One Peptide Prodrug with Targeting, Assembly and Release Properties for Overcoming Bacterium-Induced Drug Resistance and Potentiating Anti-Cancer Immune Response. Advanced Materials. 2024
DOI: 10.1002/adma.202312153
https://onlinelibrary.wiley.com/doi/10.1002/adma.202312153



















