
放射治療誘導前藥活化為降低癌癥治療的化療過程出現的全身毒性提供一種非常理想的解決方案,但是通常放射活化能夠保護的范圍很有限。
有鑒于此,北京大學劉志博等發現通過光誘導電子轉移化學能夠用于開發可輻射去除的多功能保護基團。
本文要點
(1)
作者使用基因分析的功能報告,發現N-烷基-4-吡啶(NAP)是一種能夠釋放通訊分子從而表現對輻射有非常好響應能力的籠官能團。將NAP與其他光輻照脫除的保護基團相比,NAP比迄今為止發現的其他可去除輻射的保護基團更有效。
(2)
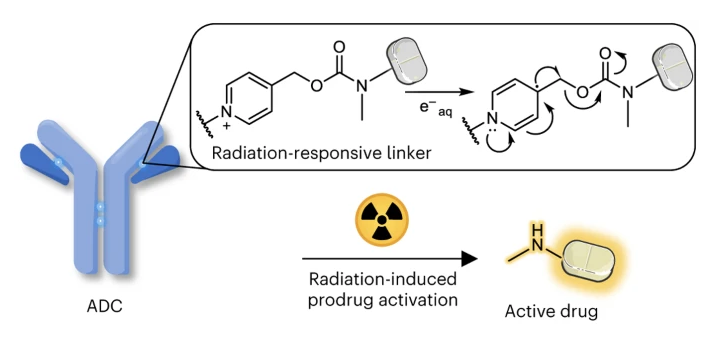
通過NAP的優異性質,作者開發了一種NAP衍生的萘基甲酸酯(carbamate)官能團,通過設計讓官能團受到輻照作用下能夠釋放熒光團和毒素,作者將這種萘基甲酸酯官能團引入到抗體-藥物偶聯物(ADC,Antibody-drug conjugate)。設計的這些ADC在活體細胞和荷瘤小鼠中表現活性,說明使用這種輻射可去除的保護基為發展具有穩定性和更好治療效果的下一代ADC的潛力。
參考文獻
Fu, Q., Gu, Z., Shen, S. et al. Radiotherapy activates picolinium prodrugs in tumours. Nat. Chem. (2024)
DOI: 10.1038/s41557-024-01501-4
https://www.nature.com/articles/s41557-024-01501-4




















