金屬生物材料可通過放大氧化應激實現對腫瘤鐵死亡的激活,但其在腫瘤微環境中的療效仍會受到很大的限制。雖然干擾素γ(IFN-γ)可通過抑制抗氧化系統和促進脂質蓄積來增強腫瘤對鐵死亡的敏感性,但這種作用也會受到腫瘤中的IFN-γ蓄積有限等問題的影響。有鑒于此,重慶醫科大學郭大靜教授開發了一種近紅外(NIR)響應性HCuS納米復合物(HCuS-PE@TSL-tlyp-1),其可以通過外源性氧化應激刺激免疫原性細胞死亡(ICD)介導的IFN-γ分泌,從而通過相互促進的鐵死亡和全身免疫實現級聯鐵治療。
本文要點:
(1)在激光照射下,熱敏包覆層的分解以及引入的銅離子和哌嗪-erastin(PE)可同時通過活性氧(ROS)/脂質過氧化物(LPO)的積累誘導氧化應激,并消耗胱氨酸-谷氨酸轉運體(xCT)/GSH。研究發現,氧化應激介導的鐵死亡能夠觸發ICD,從而顯著地促進細胞毒性T細胞(CTL)的浸潤以分泌IFN-γ。
(2)IFN-γ可通過抑制xCT抗氧化通路和增強ACSL4-脂肪酸募集通路誘導免疫原性腫瘤鐵死亡,從而進一步增強腫瘤細胞對鐵死亡的敏感性。實驗結果表明,HCuS納米復合物聯合aPD-L1可有效抑制腫瘤的轉移和復發。綜上所述,該研究構建的HCuS生物材料有望進一步拓展級聯鐵治療的應用。
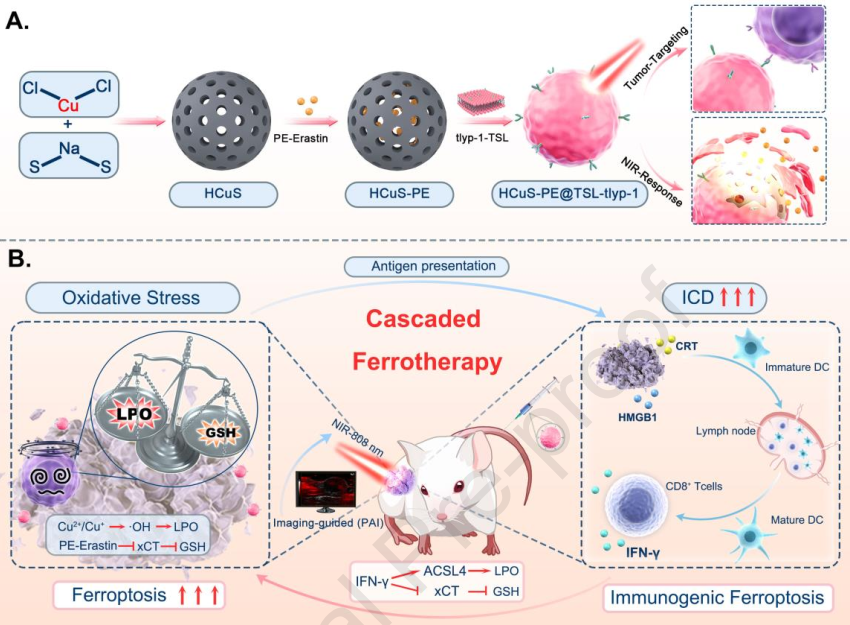
Junrui Wang. et al. NIR-Responsive Copper Nanoliposome Composites for Cascaded Ferrotherapy via Ferroptosis actived ICD and IFN-γ released. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224001042



















