細胞內的DNA感應器可調節先天免疫,并且能夠為適應性免疫原性提供橋梁。然而,雙鏈DNAs或環核苷酸等天然激動劑對抗原提呈細胞(APCs)中的感應器的激活仍會受到細胞內遞送不良、血清穩定性不足、酶降解和快速的全身清除等因素的影響。得克薩斯大學安德森癌癥中心Betty Y. S. Kim和Wen Jiang通過研究發現,螺旋多肽的疏水性、靜電電荷和二級構象能夠被優化以通過內質網應激刺激APCs的先天免疫通路。
本文要點:
(1)三種工程化多肽的其中之一可通過促進線粒體DNA的釋放優先激活APCs中兩種主要的胞內DNA感應通路(cGAS-STING和Toll樣受體9),從而實現效應T細胞的有效啟動。
(2)在局部晚期和轉移性乳腺癌的同系小鼠模型中,該多肽能夠通過單藥靜脈注射或與免疫檢查點抑制劑的聯合給藥產生由DNA感應器介導的強效抗腫瘤應答。綜上所述,該研究構建的工程化陽離子多肽可激活多種先天免疫通路,其在產生抗腫瘤免疫應答方面具有顯著的治療優勢。
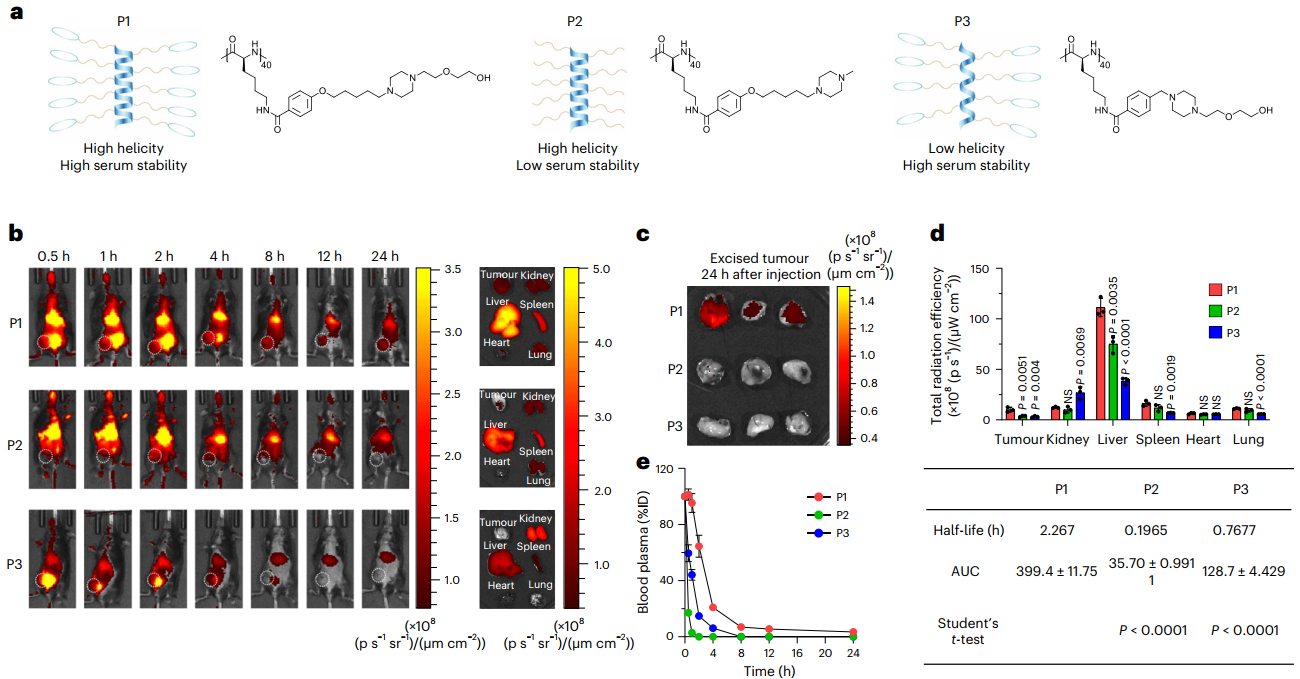
DaeYong Lee. et al. Synthetic cationic helical polypeptides for the stimulation of antitumour innate immune pathways in antigen-presenting cells. Nature Biomedical Engineering. 2024
https://www.nature.com/articles/s41551-024-01194-7



















