原位膠質母細胞瘤(GBM)具有侵襲性的生長方式和復雜的發病機制,是最常見、最致命的中樞神經系統(CNS)腫瘤之一。RNA療法的出現為GBM的治療帶來了新的希望。然而,如何在具有高度細胞異質性的腦內將RNA藥物高效、精準地遞送到特定的腫瘤細胞中仍是一項嚴峻的挑戰。有鑒于此,南開大學劉書琳教授設計了一種新的策略,即利用脂質納米環境來調節蛋白質構象,從而定制設計具有優異的細胞選擇性靶向能力的病毒模擬納米顆粒(VMNs),并將其用于高效、精準地遞送小干擾RNA(siRNA),以實現對GBM的有效治療。
本文要點:
(1)研究發現,優化后的VMNs不僅保留了像天然病毒一樣穿過血腦屏障并通過溶酶體逃逸釋放RNA的能力,而且可以在GBM區域實現精準富集。
(2)綜上所述,該研究工作為定制設計具有卓越的細胞選擇性靶向能力的VMNs奠定了概念基礎,有望為利用RNA療法實現對GBM和CNS腫瘤的有效治療提供新的見解。
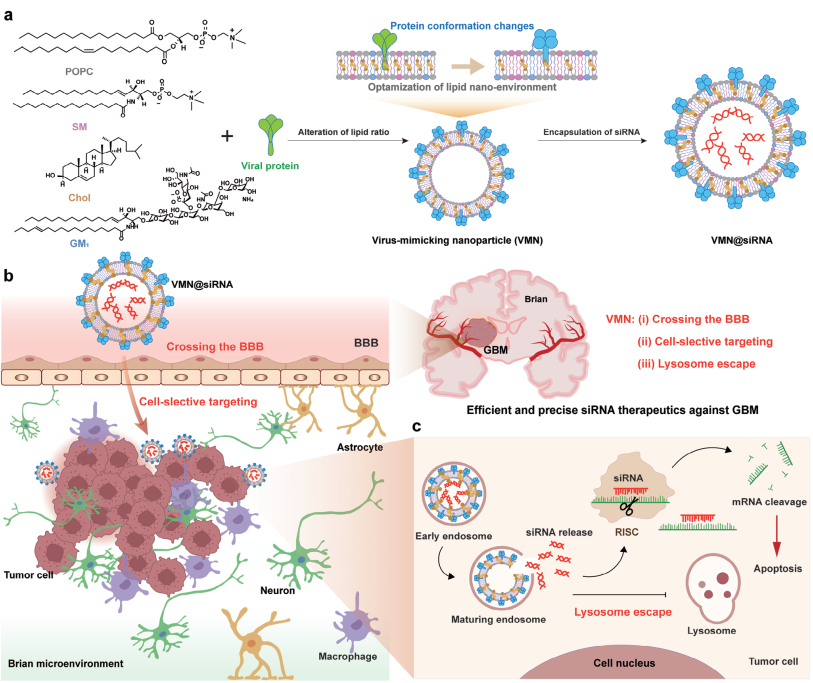
Han Zhu. et al. Regulation of Protein Conformation Enables Cell-Selective Targeting of Virus-Mimicking Nanoparticles for siRNA Therapy of Glioblastoma. Advanced Materials. 2024
DOI: 10.1002/adma.202401640
https://onlinelibrary.wiley.com/doi/10.1002/adma.202401640



















