三陰性乳腺癌(TNBC)是一種具有高度侵襲性的惡性腫瘤,目前尚缺乏有效的靶向治療方法。誘導腫瘤細胞發(fā)生免疫原性細胞死亡(ICD)可通過促進抗腫瘤免疫來提高治療效果。紫杉醇(Paclitaxel,PTX)是治療TNBC的常用化療藥物,可誘導ICD,但該策略產(chǎn)生的免疫原性較為有限。因此,亟需探索通過聯(lián)合免疫調(diào)節(jié)劑來提高ICD在TNBC中的有效性的新策略。有鑒于此,浙江大學王偉林教授、Yang Du、毛崢偉教授和丁元研究員發(fā)現(xiàn)塞來昔布(CXB)可通過阻斷PGE2在腫瘤細胞中的生物合成來增強PTX誘導ICD的性能。
本文要點:
(1)研究發(fā)現(xiàn),CXB和PTX的聯(lián)合應用可促進樹突狀細胞的成熟,并啟動T細胞依賴性免疫應答,從而能夠在疫苗接種試驗中產(chǎn)生增強的腫瘤排斥反應。為了進一步優(yōu)化體內(nèi)藥物遞送,研究者開發(fā)了cRGD修飾的脂質(zhì)體以用于CXB和PTX的靶向共遞送。
(2)實驗結(jié)果表明,該遞送系統(tǒng)能夠在TNBC原位小鼠模型中顯著改善藥物的腫瘤富集,并觸發(fā)產(chǎn)生強大的抗腫瘤免疫。此外,該系統(tǒng)也可作為原位疫苗以抑制腫瘤的復發(fā)和肺轉(zhuǎn)移。綜上所述,該研究工作揭示了CXB和PTX聯(lián)合治療的機制,能夠為實現(xiàn)高效的三陰性乳腺癌免疫治療提供新的見解。
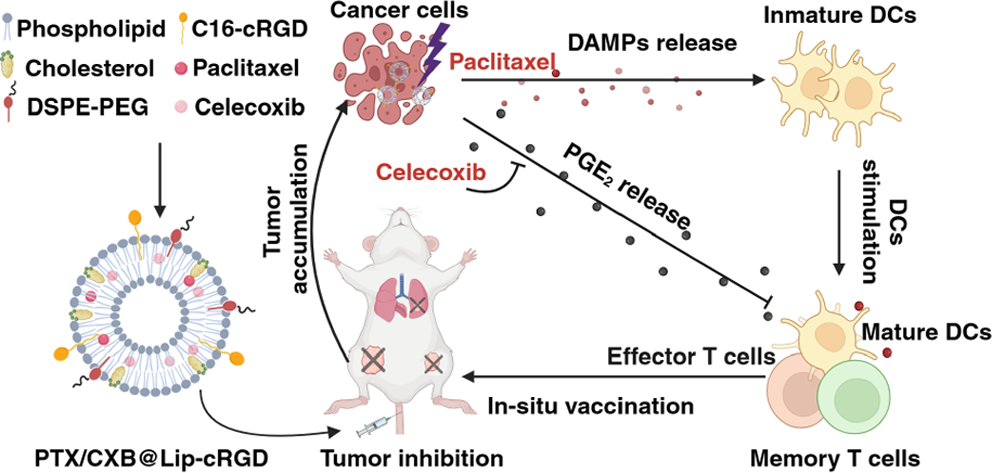
Xiaohui Qian. et al. Celecoxib Augments Paclitaxel-Induced Immunogenic Cell Death in Triple-Negative Breast Cancer. ACS Nano. 2024
DOI: 10.1021/acsnano.4c02947
https://pubs.acs.org/doi/10.1021/acsnano.4c02947



















