心臟移植能夠挽救終末期心力衰竭患者的生命。然而,該策略也面臨著缺血再灌注損傷(IRI)以及免疫排斥反應等嚴峻挑戰。目前的治療方法主要針對于適應性免疫,而能夠解決IRI和先天免疫激活的方法則較為有限。雖然植物源性類囊泡納米顆粒在疾病治療領域中表現出了重要潛力,但它們在治療器官移植并發癥中的應用還尚未被探索。有鑒于此,中山大學陳紅波教授、程芳教授和南方醫科大學Qipeng Sun開發了一種負載雷帕霉素的活性氧(ROS)響應性多功能融合細胞外納米囊泡(FNVs@RAPA),并將其用于治療心臟移植中的早期IRI和Ly6C+Ly6G-炎性巨噬細胞介導的排斥反應。
本文要點:
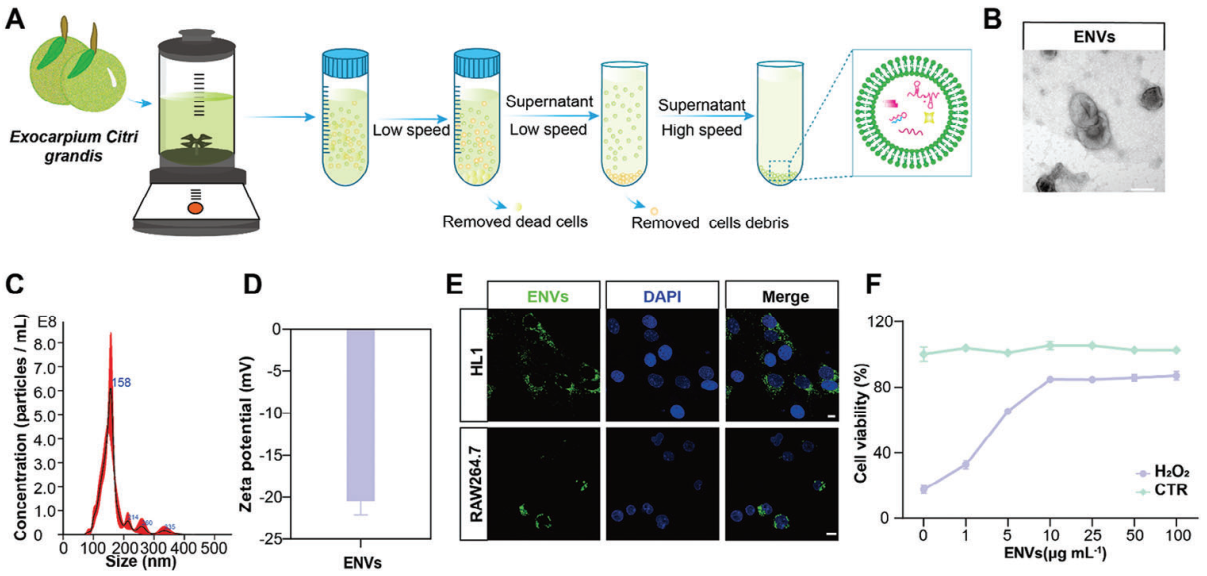
(1)FNVs包括源自化橘紅、具有抗炎和抗氧化特性的細胞外納米囊泡以及源自間充質干細胞膜、表達鈣網蛋白并具有巨噬細胞靶向性的納米囊泡。研究發現,實驗設計的新型ROS響應性生物正交化學方法有助于FNVs@RAPA實現對心臟移植部位的主動靶向遞送,進而可以有效緩解IRI,并且能夠促進Ly6C+Ly6G-炎癥巨噬細胞向抗炎表型極化。
(2)實驗結果表明,FNVs@RAPA能夠為減輕早期移植并發癥和免疫排斥反應提供一種有效的治療方法。綜上所述,該研究設計的融合靶向遞送策略具有優越的心臟移植部位富集效果和巨噬細胞特異性靶向作用,有望能夠改善心臟移植的治療效果。
Xingyu Lu. et al. Reactive Oxygen Species Responsive Multifunctional Fusion Extracellular Nanovesicles: Prospective Treatments for Acute Heart Transplant Rejection. Advanced Materials. 2024
DOI: 10.1002/adma.202406758
https://onlinelibrary.wiley.com/doi/10.1002/adma.202406758
![]()



















