靶向CD47/SIRPα軸的免疫檢查點阻斷是一個重要的癌癥免疫治療策略。然而,傳統的抗CD47抗體在體內的有效性和安全性不足等問題仍會嚴重阻礙其實現廣泛的臨床應用。有鑒于此,深圳灣實驗室葛韻研究員和饒浪研究員在抗CD47的納米抗體(HM-nCD47)中引入了單一類型的高甘露糖聚糖,并隨后在細胞囊泡(CVs)上展示HM-nCD47以增強腫瘤免疫治療。
本文要點:
(1)在該平臺中,CVs可顯著改善HM-nCD47-CVs的循環時間,nCD47可阻斷CD47/SIRPα軸,HM則能夠增強對甘露糖結合凝集素的識別。研究發現,這些作用能夠協同激活巨噬細胞介導的抗腫瘤免疫。
(2)在皮下和轉移性小鼠腫瘤模型中,HM-nCD47-CVs能夠表現出顯著延長的半衰期和增加的腫瘤富集效率,以實現具有巨噬細胞依賴性的腫瘤生長抑制、免疫反應的轉錄組重塑和生存時間的改善。綜上所述,該研究開發的HM-nCD47-CVs能夠將化學生物學工具箱與細胞膜納米技術相結合,有望為癌癥和其他疾病提供一個新的免疫治療平臺。
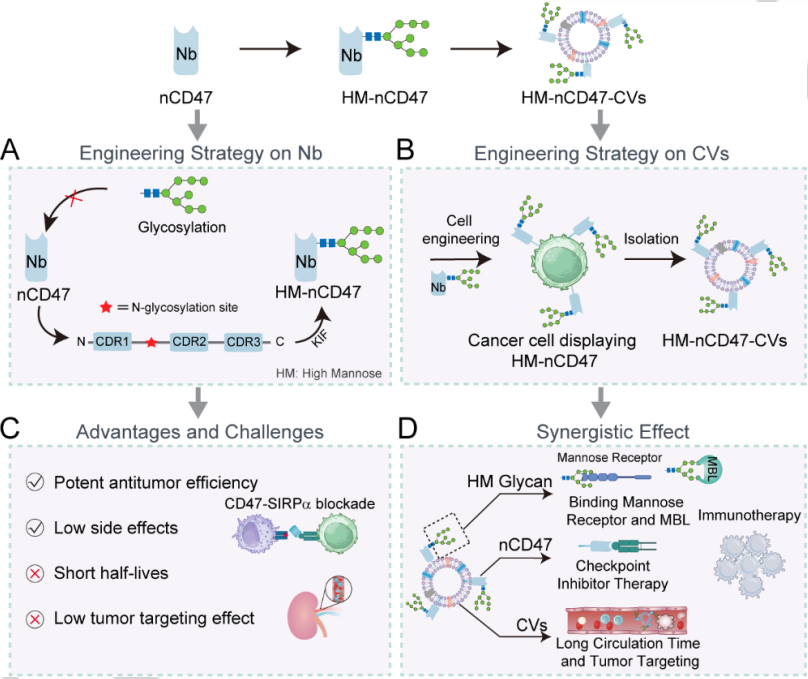
Jicheng Wu. et al. Engineered Cellular Vesicles Displaying Glycosylated Nanobodies for Cancer Immunotherapy. Angewandte Chemie International Edition. 2024
DOI: 10.1002/anie.202404889
https://onlinelibrary.wiley.com/doi/10.1002/anie.202404889




















