由于腫瘤局部放療啟動的抗原大量釋放可引起腫瘤特異性免疫應答,因此放療誘導的原位疫苗接種極大地促進了個性化腫瘤疫苗的發展。然而,抗原交叉呈遞不良、應答率低和療效持續時間短等因素仍會嚴重阻礙該策略在腫瘤治療中的廣泛應用。有鑒于此,蘇州大學史海斌教授和程俠菊教授制備了由金納米顆粒、3,5-環己二酮(CHD)和免疫佐劑CpG組成的腫瘤抗原捕獲納米系統dAuNPs@CpG,并將其用于增強RT誘導的疫苗接種。
本文要點:
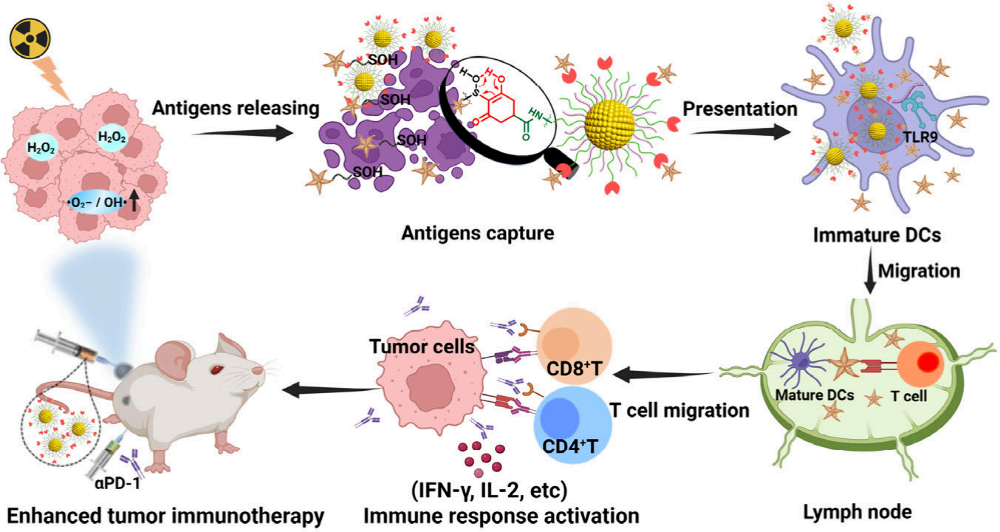
(1)該納米平臺能夠利用CHD與抗原蛋白的次磺酸之間的特異性共價結合捕獲RT誘導的亞磺酰化腫瘤衍生蛋白抗原(TDPAs),從而產生原位疫苗效應,
(2)實驗結果表明,該研究設計的方法能夠聯合PD-1阻斷以顯著抑制原發和遠端腫瘤的生長。綜上所述,該研究工作為增強腫瘤放射免疫協同治療提供了一個新的有效手段。
Jinfeng Zhu. et al. S?Sulfenylation Driven Antigen Capture Boosted by Radiation for Enhanced Cancer Immunotherapy. ACS Nano. 2024
DOI: 10.1021/acsnano.4c02206
https://pubs.acs.org/doi/10.1021/acsnano.4c02206



















