盡管可激活的化療具有廣闊的應(yīng)用前景,但如何在深部組織中實(shí)現(xiàn)時(shí)空可控的前藥激活策略仍是一項(xiàng)極具挑戰(zhàn)性的難題。有鑒于此,澳門大學(xué)陳美婉教授和華南理工大學(xué)邵丹研究員設(shè)計(jì)了一種基于金納米團(tuán)簇的新策略,該策略可利用X射線照射觸發(fā)鉑(Pt)基前藥偶聯(lián)物的釋放,從而實(shí)現(xiàn)以放療為導(dǎo)向的化療。
本文要點(diǎn):
(1)機(jī)制研究發(fā)現(xiàn),激發(fā)態(tài)金納米團(tuán)簇到Pt(IV)中心的光電子轉(zhuǎn)移過程會導(dǎo)致具有細(xì)胞毒性的Pt(II)藥物被釋放,從而實(shí)現(xiàn)前藥的輻射激活。與傳統(tǒng)的放化療相比,這種以放療為導(dǎo)向的化療策略能夠在腫瘤部位實(shí)現(xiàn)時(shí)空協(xié)同作用,因此具有更好的抗腫瘤療效和安全性。
(2)實(shí)驗(yàn)結(jié)果表明,該策略能夠引起有效的免疫原性細(xì)胞死亡,以實(shí)現(xiàn)對乳腺癌的聯(lián)合免疫治療。綜上所述,該研究設(shè)計(jì)的多功能策略能夠?yàn)閷?shí)現(xiàn)輻射介導(dǎo)的化學(xué)控制藥物遞送和生物過程精確調(diào)控提供新的借鑒和參考。
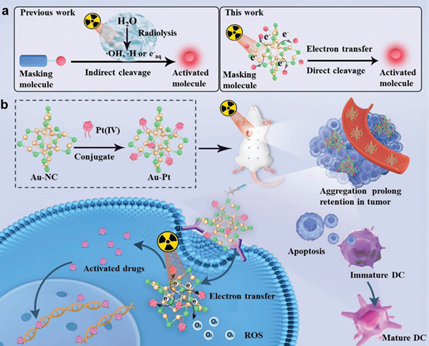
Fangman Chen. et al. Gold Nanocluster: A Photoelectric Converter for X-Ray-Activated Chemotherapy. Advanced Materials. 2024
DOI: 10.1002/adma.202402966
https://onlinelibrary.wiley.com/doi/10.1002/adma.202402966




















