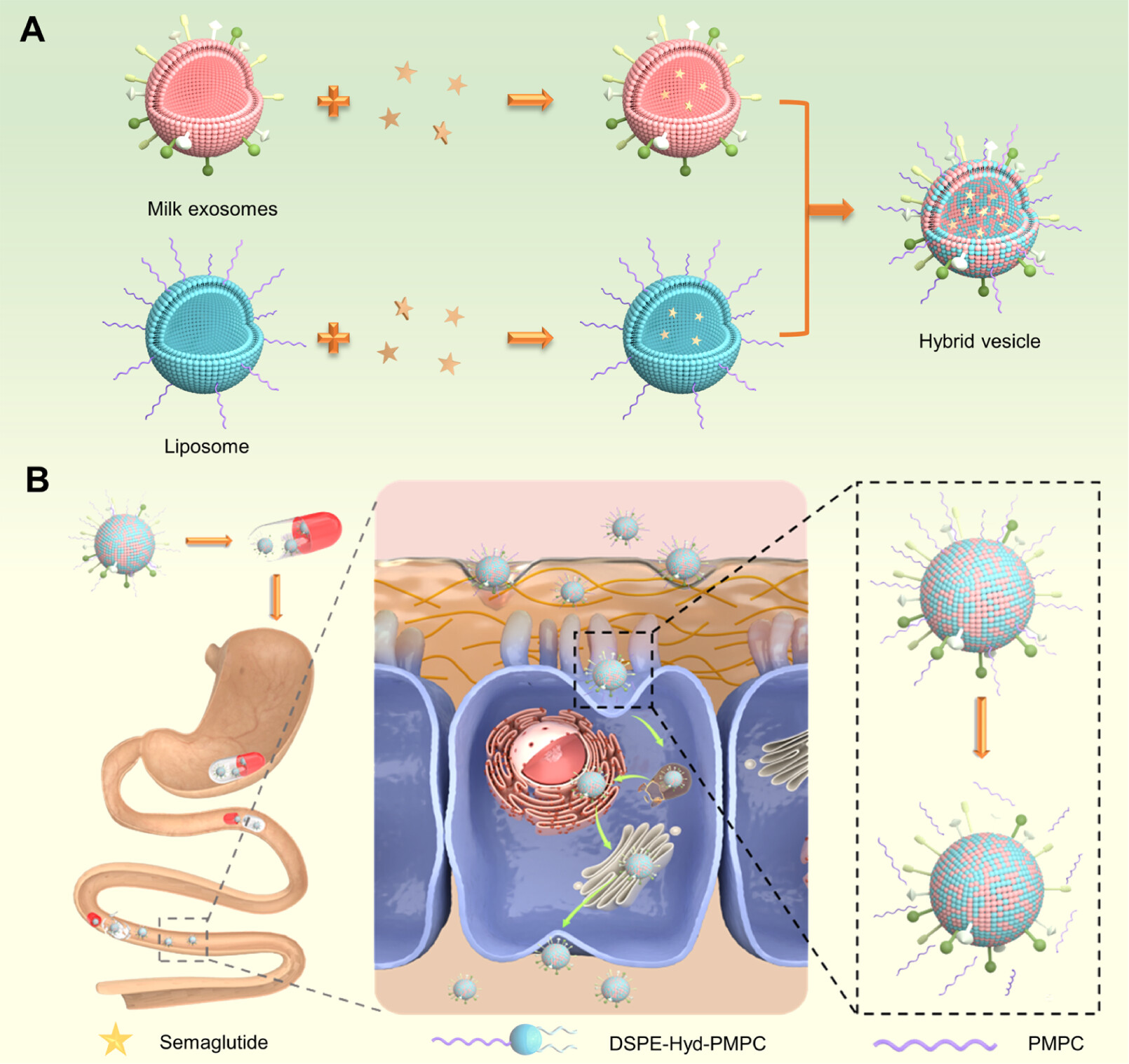
牛奶外泌體(mExos)由于其穿越上皮屏障的優越能力,已被證明是口服蛋白質和肽藥物的載體。然而,由于其內在特征,某些挑戰仍然存在,包括藥物裝載效率欠佳、粘液滲透能力不足以及易受膜蛋白損失的影響。鑒于此,沈陽藥科大學茍靖欣、唐星等人介紹了一種具有自適應表面特性的雜化囊泡(mExos@DSPE-Hyd-PMPC)通過將功能化脂質體與天然mExos融合而設計,旨在克服與mExos相關的局限性,并釋放其在口服肽遞送中的全部潛力。
本文要點:
1)表面性質轉變mExos@DSPE-Hyd-PMPC通過利用空腸表面的pH微環境在高度親水的兩性離子聚合物和磷脂之間引入pH敏感的腙鍵來實現。與天然mExos相比,雜化囊泡的semaglutide(SET)包封效率提高了2.4倍。
2)親水性和帶中性電荷的表面mExos@DSPE-Hyd-PMPC空腸腔內的細胞表現出膜蛋白保存的改善和粘液屏障的有效穿越。到達空腸上皮細胞表面后,高度保留的膜蛋白和雜交囊泡的帶正電表面有效地克服了頂端屏障、細胞內運輸屏障和基底外側胞吐屏障。雜化囊泡的自適應表面特性導致口服生物利用度為8.7%,顯著增強了藥理治療效果。這項研究成功地解決了天然mExos的一些局限性,并有望克服與肽口服遞送相關的連續吸收障礙。
參考文獻:
Peifu Xiao, Hanxun Wang, Hongbing Liu, Haoyang Yuan, Chen Guo, Yupeng Feng, Pan Qi, Tian Yin, Yu Zhang, Haibing He, Xing Tang, and Jingxin Gou. Milk Exosome–Liposome Hybrid Vesicles with Self-Adapting Surface Properties Overcome the Sequential Absorption Barriers for Oral Delivery of Peptides. ACS Nano 2024 18 (32), 21091-21111
DOI: 10.1021/acsnano.4c02560
https://pubs.acs.org/doi/10.1021/acsnano.4c02560


















