鐵代謝是一個(gè)重要的癌癥治療靶點(diǎn)。然而,癌細(xì)胞的先天代謝代償能力會(huì)顯著限制鐵代謝治療的有效性。有鑒于此,蘇州大學(xué)程亮教授和Guanghui Hou成功開發(fā)了具有生物活性的硫化鎵納米點(diǎn)(GaSx),其具有“重編程”和“干擾”鐵代謝通路的雙重功能,可用于腫瘤鐵代謝治療。
本文要點(diǎn):
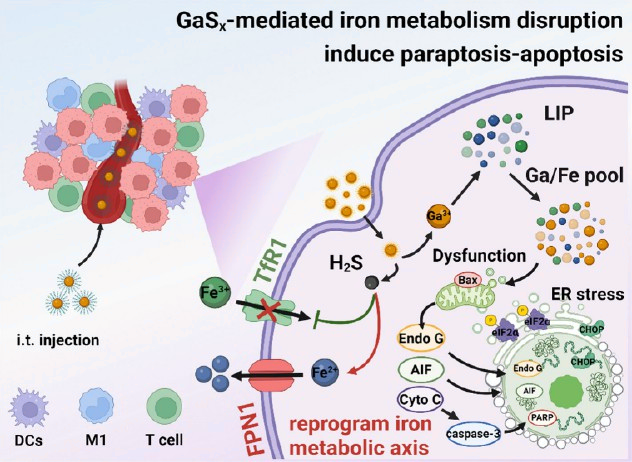
(1)實(shí)驗(yàn)構(gòu)建的GaSx納米點(diǎn)可巧妙利用在腫瘤微環(huán)境中響應(yīng)釋放的硫化氫(H2S)氣體,以重編程癌細(xì)胞中固有的轉(zhuǎn)鐵蛋白受體1 (TfR1)-鐵轉(zhuǎn)運(yùn)蛋白1 (FPN1)鐵代謝軸。與此同時(shí),GaSx衍生的鎵離子(Ga3+)可作為生化“特洛伊木馬”,其不僅能夠模擬鐵的作用,并且可以取代生物分子結(jié)合位點(diǎn)上的鐵,進(jìn)而影響癌細(xì)胞的命運(yùn)。
(2)實(shí)驗(yàn)結(jié)果表明,GaSx可通過Ga3+介導(dǎo)的鐵擾亂和 H2S促進(jìn)的鐵代謝途徑重編程的雙重機(jī)制促進(jìn)癌細(xì)胞中副凋亡-凋亡混合通路的啟動(dòng),以顯著抑制腫瘤增殖。此外,GaSx誘導(dǎo)的鐵代謝失調(diào)也可以顯著增加腫瘤細(xì)胞對(duì)化療和免疫檢查點(diǎn)阻斷(ICB)治療的敏感性。綜上所述,該研究設(shè)計(jì)的基于氣體干預(yù)和金屬離子干擾腫瘤代謝的治療策略具有非常廣闊的應(yīng)用前景。
Huali Lei. et al. A Two-Pronged Nanostrategy of Iron Metabolism Disruption to Synergize Tumor Therapy by Triggering the Paraptosis?Apoptosis Hybrid Pathway. ACS Nano. 2024
DOI: 10.1021/acsnano.4c06199
https://pubs.acs.org/doi/10.1021/acsnano.4c06199



















