在局部晚期頭頸部鱗狀細(xì)胞癌(HNSCC)患者中,放療/放化療聯(lián)合免疫檢查點(diǎn)阻斷療法的策略往往會導(dǎo)致預(yù)后不良。倫敦癌癥研究所Emmanuel C. Patin通過研究發(fā)現(xiàn),ATR抑制(ATRi)聯(lián)合放療(RT)可增加HNSCC動物模型中活化的NKG2A+PD-1+ T細(xì)胞的頻率。
本文要點(diǎn):
(1)與單獨(dú)的ATRi/RT治療方案相比,在輔助、放療后的ATRi/RT治療方案中同時(shí)引入NKG2A和PD-L1阻斷劑可誘導(dǎo)產(chǎn)生強(qiáng)大的、由腫瘤微環(huán)境中細(xì)胞毒性T細(xì)胞的更高浸潤和活化所驅(qū)動的抗腫瘤反應(yīng)。
(2)實(shí)驗(yàn)結(jié)果表明,這種組合療法的療效依賴于CD40/CD40L共刺激和浸潤活化的增殖記憶CD8+和CD4+ T細(xì)胞,它們分別具有持續(xù)或新的T細(xì)胞受體(TCR)信號。此外,研究者也觀察到了TCR庫的豐富度發(fā)生增加,并且出現(xiàn)了許多大的TCR克隆型,這些克隆型能夠?qū)崿F(xiàn)基于響應(yīng)NKG2A/PD-L1/ATRi/RT的抗原特異性的聚集。綜上所述,該研究工作能夠?yàn)橹委烪NSCC提供一個(gè)新的聯(lián)合策略。
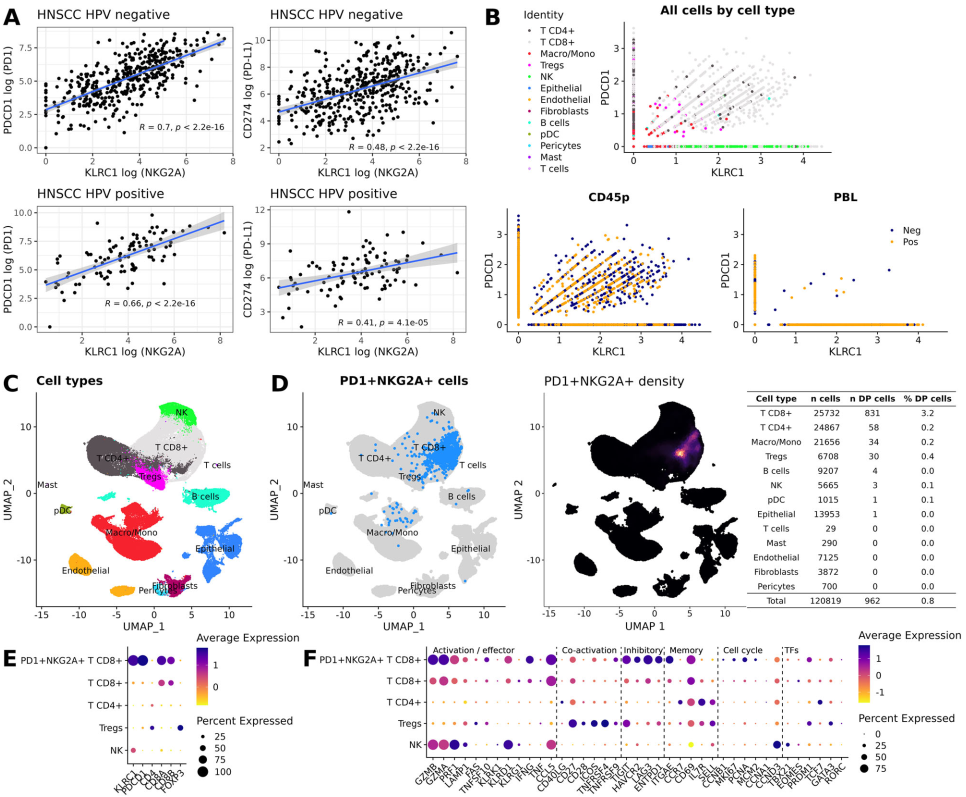
Emmanuel C. Patin. et al. Sculpting the tumour microenvironment by combining radiotherapy and ATR inhibition for curative-intent adjuvant immunotherapy. Nature Communications. 2024
https://www.nature.com/articles/s41467-024-51236-6



















