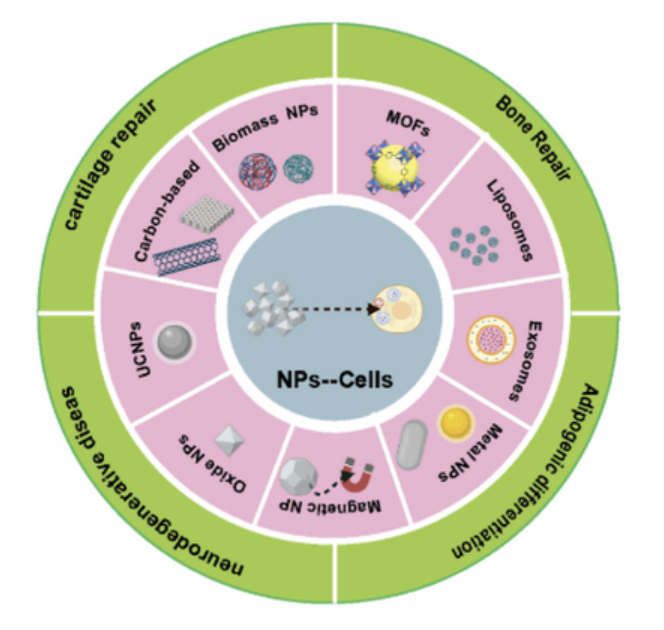
干細(xì)胞是組織修復(fù)和再生的理想選擇,具有多向分化和自我更新的能力。然而,有限的自發(fā)分化潛力使得在沒有外部干預(yù)的情況下利用它們進(jìn)行組織修復(fù)極具挑戰(zhàn)性。盡管使用生物分子、小有機分子和離子的傳統(tǒng)方法顯示出有效的功能,但它們面臨著體內(nèi)擴散和降解、內(nèi)化不良以及對鄰近細(xì)胞的副作用等挑戰(zhàn)。近日,山東大學(xué)周文娟、劉宏、濟南大學(xué)孫春輝對用于干細(xì)胞治療的納米工程內(nèi)細(xì)胞生物材料進(jìn)行了綜述研究。
干細(xì)胞是組織修復(fù)和再生的理想選擇,具有多向分化和自我更新的能力。然而,有限的自發(fā)分化潛力使得在沒有外部干預(yù)的情況下利用它們進(jìn)行組織修復(fù)極具挑戰(zhàn)性。盡管使用生物分子、小有機分子和離子的傳統(tǒng)方法顯示出有效的功能,但它們面臨著體內(nèi)擴散和降解、內(nèi)化不良以及對鄰近細(xì)胞的副作用等挑戰(zhàn)。近日,山東大學(xué)周文娟、劉宏、濟南大學(xué)孫春輝對用于干細(xì)胞治療的納米工程內(nèi)細(xì)胞生物材料進(jìn)行了綜述研究。
本文要點:
1) 納米工程生物材料通過固化和納米化這些可溶性調(diào)節(jié)分子和離子,促進(jìn)其被干細(xì)胞吸收,從而提供了一種有效的解決方案。一旦進(jìn)入溶酶體,這些納米粒子就會在受控的“分子或離子風(fēng)暴”中釋放其內(nèi)容物,并有效地改變細(xì)胞內(nèi)的生物和化學(xué)微環(huán)境,以調(diào)節(jié)干細(xì)胞的分化。
2) 作者綜述了納米工程生物材料的設(shè)計原理,討論了納米粒子的種類和特征,總結(jié)了納米粒子在組織修復(fù)和再生中的應(yīng)用,并討論了納米粒子增強干細(xì)胞治療的方向及其在再生醫(yī)學(xué)中的臨床應(yīng)用前景。
Yingxue Wang et.al Nanoengineered Endocytic Biomaterials for Stem Cell Therapy AFM 2024
DOI: 10.1002/adfm.202410714
https://doi.org/10.1002/adfm.202410714