放療(RT)激活干擾素基因刺激因子(STING)通路對于引發抗腫瘤免疫應答而言具有重要作用。羥基自由基(·OH)風暴的產生和STING相關催化反應的敏化可以改善放射增敏介導的STING激活。有鑒于此,廣州醫科大學侯智堯教授構建了具有氧空位和模擬酶活性的多功能放射增敏劑,其能夠產生更多的dsDNA,有利于細胞內2',3'-環GMP-AMP(cGAMP)的生成,并同時引入了外源性cGAMP以激活免疫反應。
本文要點:
(1)由于誘導的氧空位可通過金屬間電荷轉移加速從Ce4+到Ce3+的氧化還原循環,因此MnO2@CeOx納米酶能夠表現出增強的類超氧化物歧化酶(SOD)和類過氧化物酶(POD)等活性。研究發現,CeOx殼不僅能夠作為放射增敏劑,還可以為AMP/GMP提供結合位點,以形成MnO2@CeOx-GAMP(MCG)。
(2)在X射線照射下,具有類SOD活性的MCG可在腫瘤微環境(TME)內促進Ce增敏產生的超氧陰離子轉化為H2O2。隨后,下游的類POD活性可催化H2O2形成大量的·OH,以產生更多的損傷DNA片段。實驗結果表明,響應TME的MCG分解可以提供外源性cGAMP,并同時釋放Mn2+以提高環GMP-AMP合酶對dsDNA的敏感性,產生更多的cGAMP,有效促進STING通路的激活。
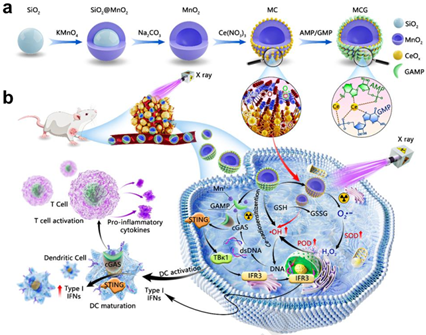
Meiling Tan. et al. MnO2@CeOx-GAMP radiosensitizer with oxygen vacancies depended mimicking enzyme-like activities for radiosensitization-mediated STING pathway activation. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224003314



















