在長期接受血液凈化治療的患者中,蛋白質的大量損失很常見,死亡風險與血清白蛋白濃度之間存在很強的負相關關系。在血液凈化領域,清除毒素并留下白蛋白是一項艱巨的任務。受腎小管中蛋白質結合毒素解離運輸過程的啟發(fā),四川大學趙偉鋒、魏然等人提出了多點光解結合吸附策略作為血液灌流中的一種新型治療方式。
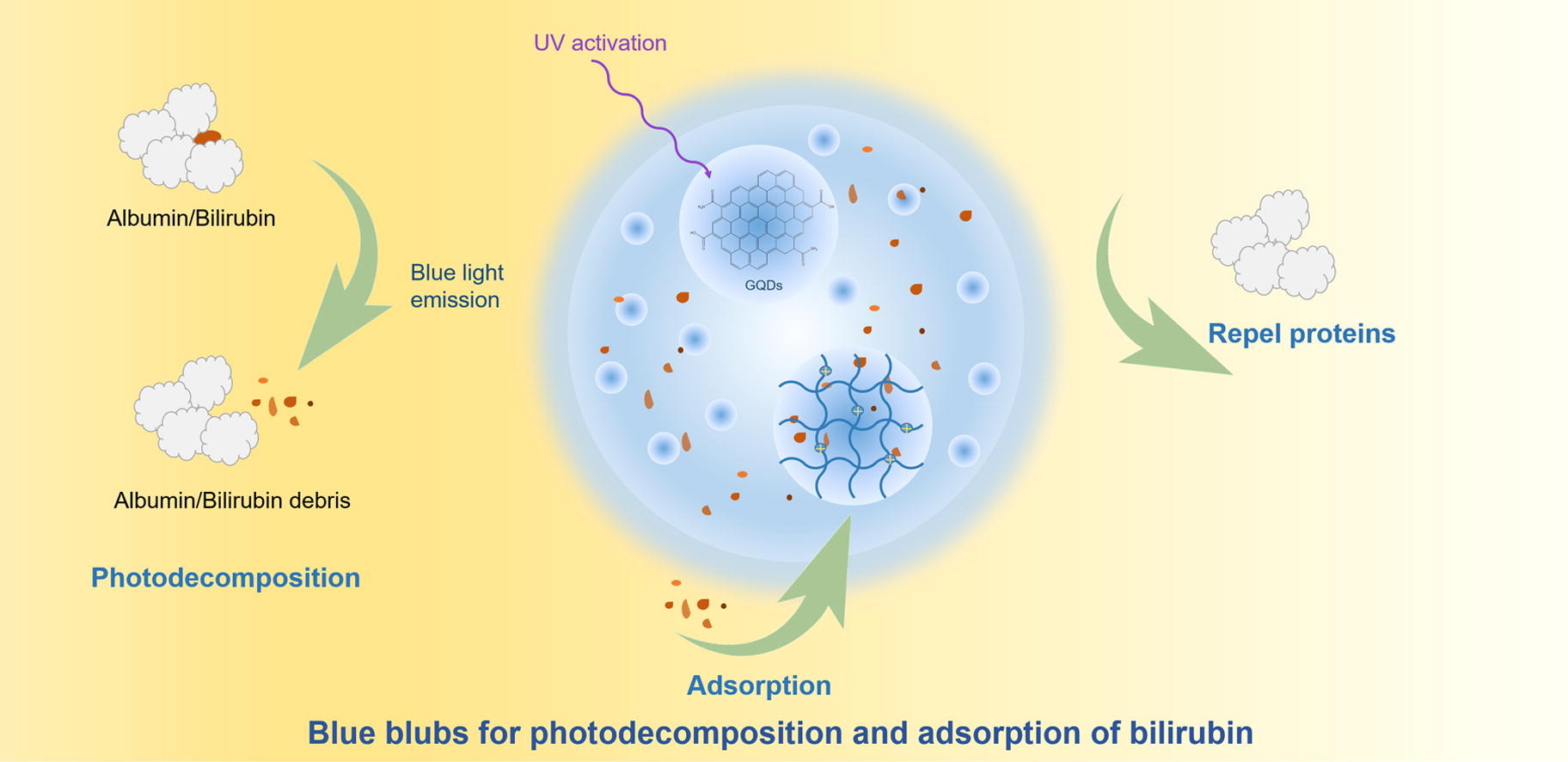
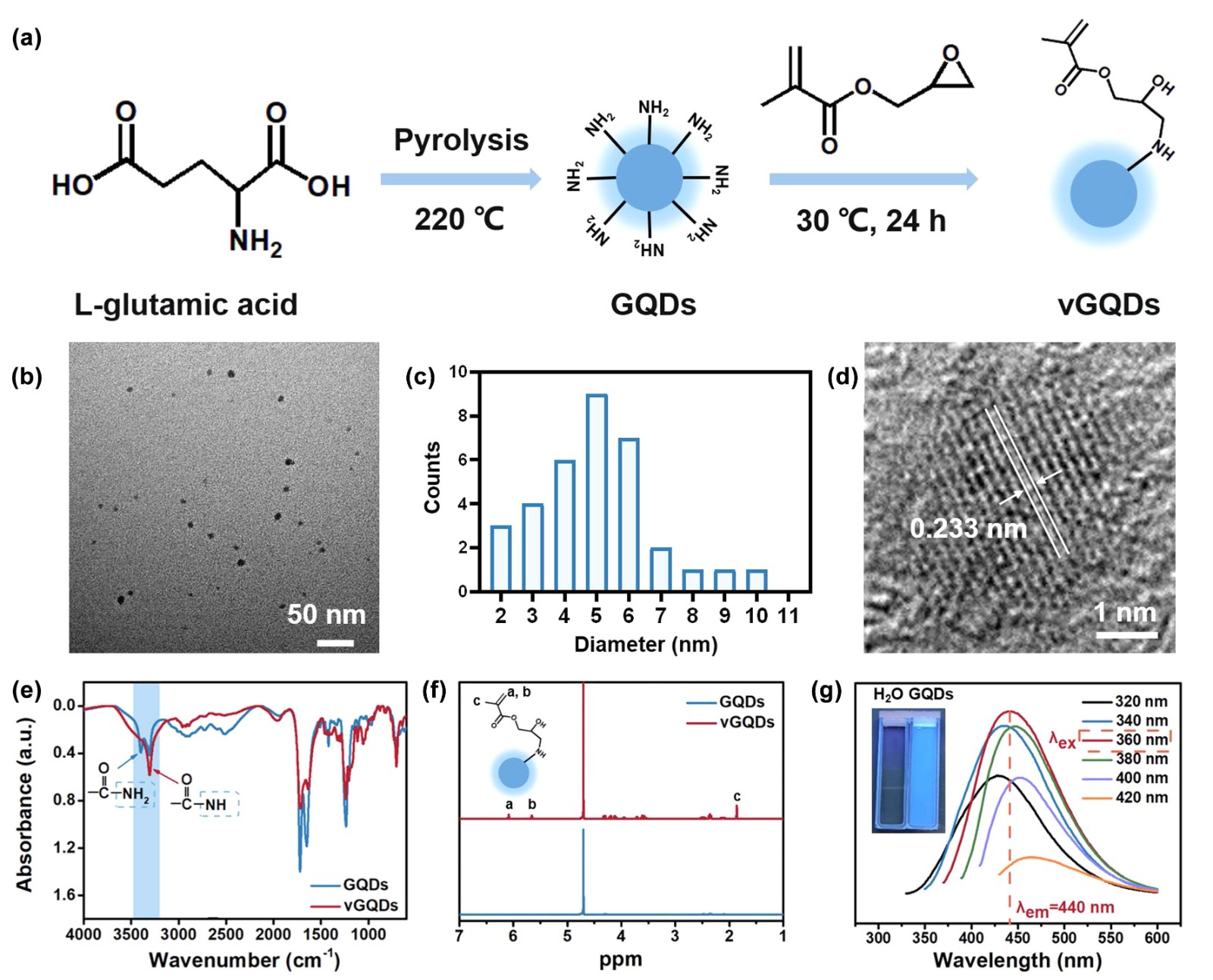
作為概念驗證,膽紅素被選為研究對象,因為它是一種典型的蛋白質結合毒素,需要在血液環(huán)境中通過與白蛋白的強結合進行運輸。有趣的是,藍光可以有效地將膽紅素分解成一些高極性的水溶性重氮化合物,膽紅素的分解產物是水溶性的,與白蛋白結合松散。于此,石墨烯量子點(GQD)和聚合物科學在納米建筑工藝中結合在一起。“光分解-吸附”平臺是通過將GQDs嵌入聚(二烯丙基二甲基氯化銨-丙烯酰胺)(聚(DDAC-AAm)水凝膠(PDMG)微球中而設計的。
為了減少陽離子聚合物對血液成分的影響,透明質酸(HA)被涂覆在PDMG的表面(PDMG@HA)通過靜電相互作用形成微球。由于GQDs的發(fā)光特性PDMG@HA微球在紫外線激活下發(fā)出藍光,將膽紅素分解成水溶性重氮化合物,就像許多“藍色燈泡”一樣。水溶性膽紅素碎片可以從白蛋白中解離出來,被“藍球”吸附,大大減輕了身體的代謝負擔。
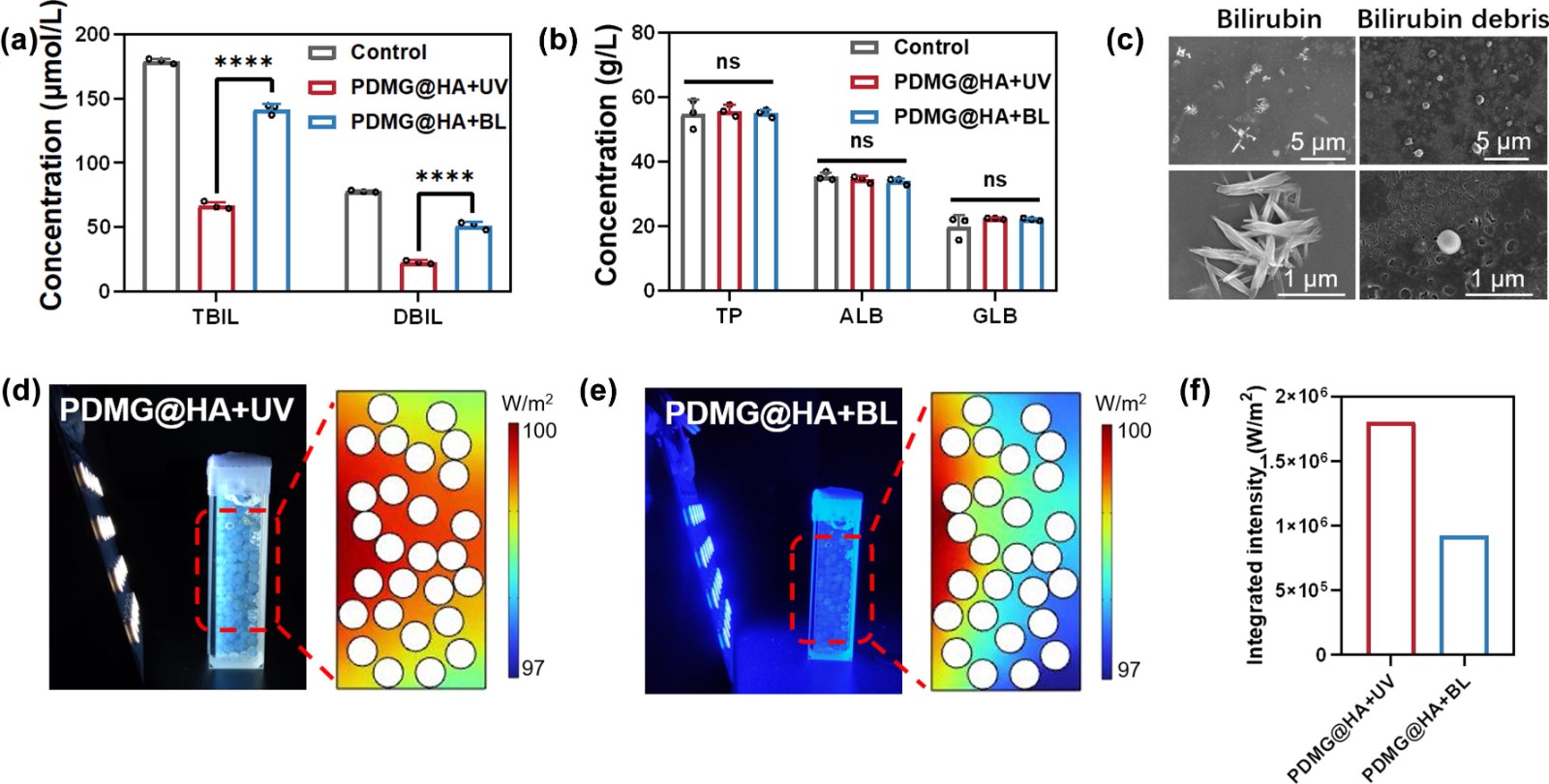
體外生物相容性結果表明PDMG@HA微球顯示出比PDMG微球更低的蛋白質吸附和血細胞毒性。膽紅素在體外的光解和吸附量為187.8mg/g。在高膽紅素血癥兔血液灌流中,“藍球”從血漿中去除70.9%的總膽紅素(TBIL),延緩膽道梗阻的肝損傷。值得注意的是,膽紅素的光解持續(xù)到治療結束,一些膽紅素碎片已被“藍色燈泡”吸附。結合光解和吸附的策略為治療血液相關疾病開辟了一條新途徑。
參考文獻:
UV-activated “blue bulbs” for photodecomposition and adsorption of bilirubin: Strategic nanoarchitectonics to remove protein-bound toxins. Materials Today 2024.
https://doi.org/10.1016/j.mattod.2024.09.010


















