病原體和宿主對錳的競爭以及復雜的免疫刺激通路嚴重影響了抗菌免疫治療對骨植入物相關生物膜感染的療效。有鑒于此,中國科學技術大學朱晨教授、蘇政教授、中國藥科大學范文培教授和上海交通大學Wanbo Zhu開發了一種時空聲金屬免疫治療(SMIT)策略,即設計了一種仿生金屬有機框架(PCN-224)包被的二氧化錳-繡球花納米顆粒(MnPM),并將其作為金屬抗生素以有效地消融生物膜。
本文要點:
(1)到達富含H2O2的酸性生物膜微環境后,MnPM可以將豐富的H2O2轉化為氧氣,以顯著增強超聲(US)觸發的聲動力治療(SDT)的療效,并暴露細菌相關抗原(BAAs)。此外,MnPM也能夠破壞細菌的體內平衡,從而進一步殺死更多的細菌。研究發現,MnO2降解釋放的Mn離子可以給免疫細胞充電,增強BAAs的cGAS-STING信號通路感知,以進一步改善免疫應答,通過生物膜特異性T細胞應答抑制生物膜生長。
(2)在US停止后,持續的氧合可促進成纖維細胞的存活和遷移,刺激血管生成生長因子的表達和血管生成,并有效中和過度的炎癥。實驗結果表明,MnPM可作為一種免疫共刺激金屬抗生素實現對cGAS-STING信號通路的調節。綜上所述,該研究為治療骨生物膜感染和促組織修復提供了一種新的抗生素替代策略。
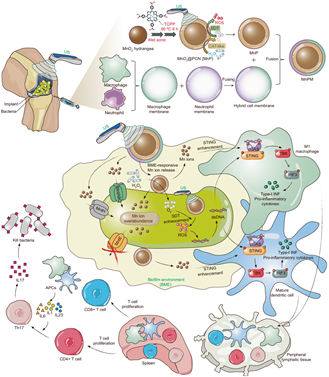
Zheng Su. et al. Biodegradable oxygen-evolving metalloantibiotics for spatiotemporal sonometalloimmunotherapy against orthopaedic biofilm infections. Nature Communications. 2024
https://www.nature.com/articles/s41467-024-52489-x



















