光籠是一種能夠精確控制生物活性的空間和時間行為的新興技術(shù)。然而,由紅光/近紅外光觸發(fā)的光籠光解過程目前主要依賴于單線態(tài)氧(1O2),并且與其他活性氧(ROS)激活技術(shù)缺乏兼容性,因此難以實現(xiàn)高效、精準(zhǔn)的治療。有鑒于此,北京師范大學(xué)邢國文教授利用超氧陰離子自由基(O2??)斷裂的硫酮鍵將喜樹堿(CPT)共價結(jié)合到雜化的BODIPY-TPE熒光基團(tuán)中,開發(fā)了一種乳糖化光籠BT-LRC,以實現(xiàn)I型光動力治療(PDT)和抗癌藥物釋放。
本文要點(diǎn):
(1)由于納米聚集體中相鄰乳糖單位之間的碳水化合物相互作用(CCIs)的調(diào)節(jié),該兩親性BT-LRC可以自組裝形成具有聚集誘導(dǎo)發(fā)光(AIE)活性的納米粒子(BT-LRCs)。研究發(fā)現(xiàn),BT-LRCs能夠通過乳糖相互作用調(diào)節(jié)的聚集產(chǎn)生豐富的O2??,并有效釋放DNA損傷劑CPT。
(2)實驗結(jié)果表明,I型PDT和CPT化療可在HepG2細(xì)胞和荷瘤小鼠模型中產(chǎn)生協(xié)同增強(qiáng)的治療效果。此外,BT-LRCs固有的AIE特性也使得該光籠化前藥具有優(yōu)越的生物成像能力,從而能夠為實現(xiàn)對PDT的實時示蹤和精細(xì)調(diào)控以及光激活藥物釋放提供一個有效的工具。
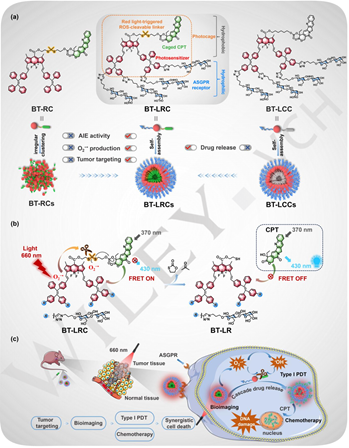
Wei Zhou. et al. Glycosylated AIE-active Red Light-triggered Photocage with Precisely Tumor Targeting Capability for Synergistic Type I Photodynamic Therapy and CPT Chemotherapy. Angewandte Chemie International Edition. 2024
DOI: 10.1002/anie.202413350
https://onlinelibrary.wiley.com/doi/10.1002/anie.202413350




















