冷暴露(CE)療法可以通過棕色脂肪組織(BAT)產(chǎn)熱快速誘導(dǎo)腫瘤饑餓。探索CE與傳統(tǒng)療法(如放療(RT))的聯(lián)合抗腫瘤機(jī)制具有重要的研究和應(yīng)用價(jià)值。有鑒于此,廣西醫(yī)科大學(xué)寧峙彭教授、新加坡國立大學(xué)陳小元院士和沈陽藥科大學(xué)王開元博士研究了CE聯(lián)合一氧化氮(NO)氣體治療對腫瘤RT的增敏作用及其增強(qiáng)腫瘤放射免疫治療的效果。
本文要點(diǎn):
(1)實(shí)驗(yàn)首先構(gòu)建了負(fù)載NO前藥S-亞硝基-N-乙酰青霉胺(SNAP)的脂質(zhì)體(SL)。當(dāng)SL被注射后,腫瘤區(qū)域內(nèi)的谷胱甘肽(GSH)可以促進(jìn)SNAP釋放NO。隨后,RT產(chǎn)生的超氧陰離子能夠與NO反應(yīng)生成過氧亞硝酸鹽(ONOO?)。ONOO?具有很強(qiáng)的氧化特性,可誘導(dǎo)細(xì)胞死亡。
(2)與此同時(shí),研究者將小鼠暴露于4°C的CE環(huán)境中。實(shí)驗(yàn)結(jié)果表明,CE介導(dǎo)的BAT產(chǎn)熱可誘導(dǎo)腫瘤饑餓,進(jìn)而導(dǎo)致腫瘤內(nèi)的ATP和GSH含量降低,并且能夠改善腫瘤乏氧微環(huán)境,減少髓源性抑制細(xì)胞,以增強(qiáng)RT的有效性,激活全身抗腫瘤免疫。在雙側(cè)腫瘤模型中,對原發(fā)腫瘤進(jìn)行聯(lián)合治療也能夠抑制遠(yuǎn)端腫瘤的生長,并促進(jìn)CD8+ T細(xì)胞向腫瘤的浸潤。綜上所述,該研究證明了CE、NO氣體治療和RT的協(xié)同作用可以產(chǎn)生高效的抗癌效果,從而為個(gè)性化癌癥治療提供了一個(gè)新的策略。
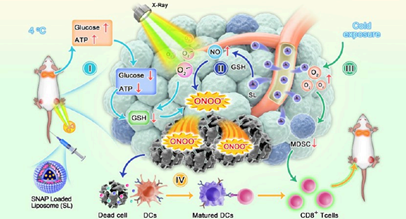
Kun Qiao. et al. Cold Exposure Therapy Sensitizes Nanodrug-Mediated Radioimmunotherapy of Breast Cancer. ACS Nano. 2024
DOI: 10.1021/acsnano.4c09021
https://pubs.acs.org/doi/10.1021/acsnano.4c09021



















