武漢大學(xué)陳效教授和Yong-Hong Xu利用血小板負載基于攜帶Ce6的功能化氮化硼納米顆粒(BNPD-Ce6)聲敏劑,設(shè)計了一種靶向膠質(zhì)母細胞瘤(GBM)的聲動力治療(SDT)策略。
本文要點:
(1)體外研究表明,BNPD-Ce6介導(dǎo)的聲動力作用(SDA)可在GBM細胞(GBCs)而非巨噬細胞中顯著誘導(dǎo)細胞活力喪失、DNA損傷和細胞死亡。暴露于SDA的GBCs會表現(xiàn)出鐵死亡表型,而暴露于SDA的巨噬細胞則能夠發(fā)生免疫刺激性自噬,并增強SDA對GBCs的毒性。研究發(fā)現(xiàn),SDA誘導(dǎo)的鐵死亡GBCs具有準(zhǔn)免疫原性,能夠釋放警報素,如ATP、HSP90和CRT,但不會產(chǎn)生強效的內(nèi)源性佐劑HMGB1。因此,SDA應(yīng)激的GBCs無法刺激BMDMs。有趣的是,將血小板作為HMGB1的供體能夠修復(fù)這一缺陷,其可以顯著增強BNPD-Ce6對GBCs的聲毒性。
(2)在體內(nèi)研究中,研究者利用負載BNPD-Ce6的血小板實現(xiàn)了超聲觸發(fā)的靶向顱內(nèi)GBMs的BNPD-Ce6遞送以及聲動力腫瘤損傷。實驗結(jié)果表明,該SDT治療策略能夠減緩顱內(nèi)GBMs的生長,并顯著提高宿主動物的存活率。病理檢查結(jié)果顯示,SDT處理會導(dǎo)致GBMs組織發(fā)生壞死。最后,研究者也發(fā)現(xiàn)消耗巨噬細胞會使SDT在皮下GBC模型中失效。綜上所述,該研究設(shè)計的基于BNPD-Ce6@Plt的SDT是一種可行有效的抗GBM治療方法,其治療機制主要包括SDA誘導(dǎo)的腫瘤細胞鐵死亡、巨噬細胞刺激和血小板活化等協(xié)同作用。
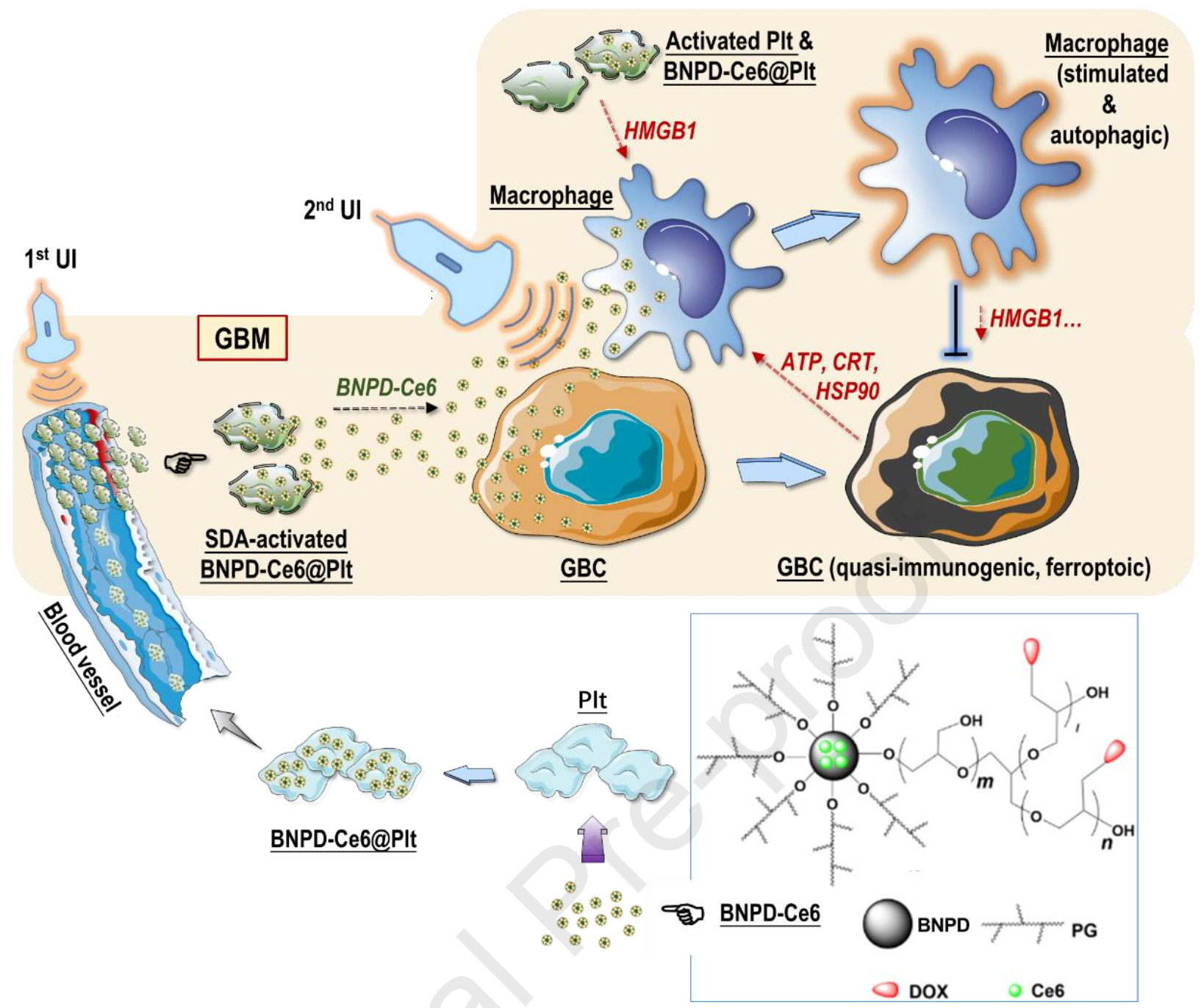
Meng-Fei Wang. et al. Targeted sonodynamic therapy induces tumor cell quasi-immunogenic ferroptosis and macrophage immunostimulatory autophagy in glioblastoma. Biomaterials. 2024
https://www.sciencedirect.com/science/article/pii/S0142961224004472



















