mRNA疫苗在預防和治療傳染病等方面的成功應用彰顯了它們作為治療性癌癥疫苗的重要潛力。然而,與感染性疾病不同的是,抗腫瘤治療(特別是對實體瘤而言)需要激活更強大的細胞和體液免疫才能產生良好的臨床療效。有鑒于此,中國科學院動物研究所魏妥研究員和北京大學程強研究員開發了一種脾臟靶向mRNA疫苗(Mn@mRNA-LNP),其能夠將編碼腫瘤抗原的mRNA和錳佐劑(Mn2+)同時遞送到脾臟的樹突狀細胞(DCs)。
本文要點:
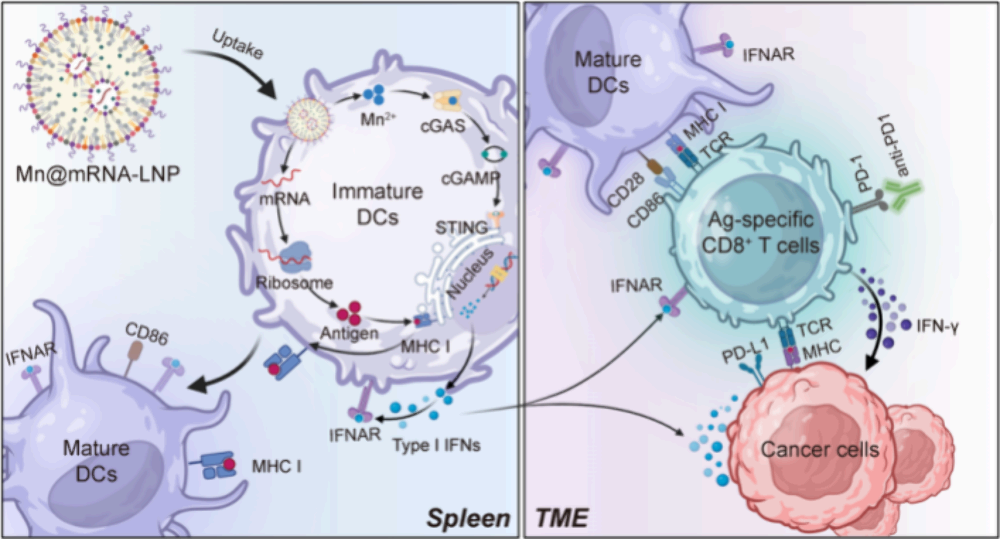
(1)該遞送系統可促進DC成熟和表面抗原呈遞,并刺激細胞毒性T細胞的產生。在系統中共遞送的Mn2+能夠作為安全有效的免疫佐劑,激活干擾素基因刺激因子(STING)信號通路,促進I型干擾素的分泌,以進一步增強抗原特異性T細胞應答。在已建立的黑色素瘤和結腸腫瘤模型以及腫瘤切除術后復發模型中,Mn@mRNA-LNP能夠有效抑制腫瘤進展。
(2)實驗結果表明,Mn@mRNA-LNP聯合免疫檢查點抑制劑能夠實現對小鼠腫瘤的完全抑制,并顯著延長小鼠的總體生存期。綜上所述,該研究設計的“All-in-One”mRNA疫苗可通過改善脾臟靶向和免疫激活顯著增強抗腫瘤免疫應答,有望為治療性mRNA疫苗的臨床轉化提供一個新的策略。
Zijin Luo. et al. Spleen-Targeted mRNA Vaccine Doped with Manganese Adjuvant for Robust Anticancer Immunity In Vivo. ACS Nano. 2024
DOI: 10.1021/acsnano.4c09902
https://pubs.acs.org/doi/10.1021/acsnano.4c09902



















