具有類過氧化物酶活性和光熱轉(zhuǎn)化效率的納米材料能夠產(chǎn)生細(xì)胞毒性羥基自由基和協(xié)同的抗腫瘤治療效果,因此受到了研究者的廣泛關(guān)注。選擇具有合適性質(zhì)和載體的納米酶是實(shí)現(xiàn)酶效最大化的關(guān)鍵。雖然粘蛋白家族以其粘附性和能夠提高藥物的生物利用度及靶向性的糖基化結(jié)構(gòu)而聞名,但其在納米酶領(lǐng)域中的應(yīng)用仍未得到充分的開發(fā)。有鑒于此,中國科學(xué)院生物物理研究所范克龍研究員和福建醫(yī)科大學(xué)陳偉教授利用粘蛋白-2促進(jìn)鋨納米團(tuán)簇(Os@Mucin),構(gòu)建了一種蛋白冠狀納米酶。
本文要點(diǎn):
(1)該構(gòu)型使得Os@Mucin具有優(yōu)異的類過氧化物酶活性(769 U/mg)和光熱轉(zhuǎn)換效率(22.83%,808 nm)。Mucin-2可促進(jìn)細(xì)胞對Os的攝取,使Os@Mucin能夠表現(xiàn)出對腫瘤環(huán)境敏感的類過氧化物酶活性。研究發(fā)現(xiàn),光熱能夠進(jìn)一步增強(qiáng)Os@Mucin的酶活性,從而提高其靶向細(xì)胞毒性和協(xié)同作用。
(2)體內(nèi)實(shí)驗(yàn)結(jié)果表明,Os@Mucin能夠?qū)崿F(xiàn)對三陰性乳腺癌的有效治療。綜上所述,該研究不僅闡明了粘蛋白家族在納米酶領(lǐng)域中的重要應(yīng)用潛力,也能夠?yàn)閷?shí)現(xiàn)Os納米酶的腫瘤治療應(yīng)用提供新的見解。
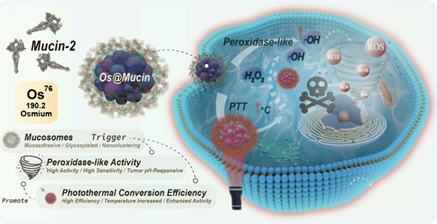
Shaobin He. et al. Mucin-Triggered Osmium Nanoclusters as Protein Corona-Like Nanozymes with Photothermal-Enhanced Peroxidase-Like Activity for Tumor-Specific Therapy. Nano Letters. 2024
DOI: 10.1021/acs.nanolett.4c04026
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c04026




















