鐵死亡具有激活抗腫瘤免疫的重要潛力。然而,狡猾的腫瘤細胞可以通過增加鐵的外排和促進還原劑谷胱甘肽的產生等機制緩解氧化應激,從而避免鐵死亡。有鑒于此,西南交通大學周紹兵教授和趙靜雅教授開發了一種負載錳摻雜氧化鐵納米顆粒(MnIO)、GW4869和L-丁硫氨酸亞砜胺(BSO)的多功能外泌體,其能夠破壞鐵代謝穩態和氧化還原穩態,以增強腫瘤免疫治療。
本文要點:
(1)外泌體對MnIO的有效轉運以及GW4869對鐵胞吐的抑制會導致腫瘤中的鐵保留率高達29.57% ID/g。研究發現,高效的鐵保留和BSO誘導的氧化還原穩態的破壞可以有效地促進腫瘤細胞發生鐵死亡。
(2)實驗結果表明,該多功能外泌體能夠通過雙重穩態破壞顯著增強鐵死亡,進而激發產生基于cGAS-STING的抗腫瘤免疫應答,有效抑制原位乳腺癌的腫瘤生長和肺轉移。
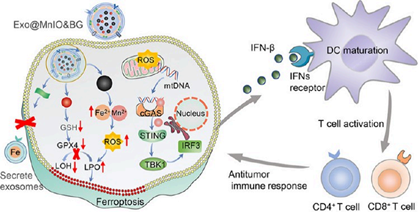
Xiaoqing Wei. et al. A Multifunctional Exosome with Dual Homeostasis Disruption Augments cGAS-STING-Mediated Tumor Immunotherapy by Boosting Ferroptosis. Nano Letters. 2024
DOI: 10.1021/acs.nanolett.4c03862
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c03862



















