放射治療(XRT)常被用于改善癌癥治療中的免疫檢查點阻斷應答。這種聯合治療策略可以增強遠端效應,產生長期、持久的全身應答。然而,目前仍只有少數患者能夠響應這種治療方法,因此研究者亟需開發能夠改善遠端效應的新策略。有鑒于此,德克薩斯大學西南醫學中心Andrew Z. Wang和Kin Man Au設計了一種可瘤內(i.t)注射、基于納米纖維(NF)的腫瘤免疫生態位(TIN),其能夠將XRT治療的腫瘤轉化為原位癌癥疫苗,進而引發強大的全身抗腫瘤免疫。
本文要點:
(1)NF基免疫生態位結合了氧化還原降解的抗CTLA-4(α-CTLA-4)納米凝膠(NGs)和白細胞介素-2(IL-2) NGs,其在乏氧的受輻照腫瘤中能夠實現可控釋放,進而可將免疫抑制性腫瘤微環境逆轉為促炎微環境,并進一步擴增在腫瘤中浸潤的CD8+ T細胞群。此外,研究者也進一步利用聚肌苷-聚胞苷酸(poly(I:C))對其進行功能化,以促進抗原呈遞細胞成熟和啟動新抗原特異性CD8+ T細胞。
(2)在體外研究中,TIN能夠在免疫抑制條件下啟動抗原特異性CD8+ T細胞,并提高抗原特異性細胞殺傷效率。體內研究表明,TIN能夠在小鼠黑色素瘤和結直腸癌模型中產生強大的全身抗癌活性,并且不會造成嚴重的免疫相關不良事件。
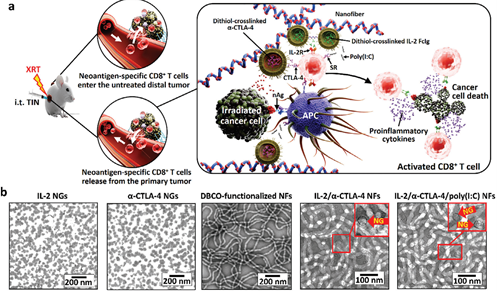
Kin Man Au. et al. Intratumoral Injectable Redox-Responsive Immune Niche Improves the Abscopal Effect in Radiotherapy. Advanced Materials. 2024
DOI: 10.1002/adma.202411330
https://onlinelibrary.wiley.com/doi/10.1002/adma.202411330



















